Аденокарцинома low grade без признаков dmmr msi h что это значит
Аденокарцинома low grade без признаков dmmr msi h что это значит
Иммунная система является ключевым медиатором в процессе гибели опухоли. Однако злокачественные клетки могут уклоняться от иммунного ответа через ряд механизмов, включая активацию иммуносупрессии, приводя к нерегулируемому росту опухоли. Блокада контрольных иммунных точек высвобождает Т-клеточно-негативную костимуляцию, что позволяет активировать противоопухолевый T клеточный ответ, в результате которого происходит распознавание и уничтожение опухоли [1]. Цитотоксический Т-лимфоцит-ассоциированный антиген-4 (CTLA-4) и рецептор запрограммированной гибели клеток 1 (PD-1) действуют как отрицательные регуляторы, ослабляя нормальную активацию Т-клеток. Рецептор PD-1 экспрессируется на поверхности активированного Т-лимфоцита и ингибирует иммуносупрессивные лиганды PD-1 (PD-L1/PD-L2), которые экспрессируются опухолевыми клетками [2]. В отличие от меланомы, рака легкого и колоректального рака 4, иммунотерапия в монорежиме не демонстрирует высокую противоопухолевую активность при распространенных опухолях гинекологического тракта 7.
Что такое микросателлитная нестабильность
У человека существует сложная система, исправляющая нарушения в ДНК, которые возникают достаточно часто. Одним из таких механизмов является система репарации неспаренных оснований ДНК (mismatch repair system – MMR), которая ответственна за распознавание и удаление неправильно спаренных оснований, образованных в результате ошибок в процессе репликации ДНК. За работу системы репарации неспаренных оснований ДНК отвечают 6 генов: MSH2, MLH1, PMS2, MSH3, MSH6 и MLH3. Наличие герминальных мутаций в этих генах приводит к развитию синдрома Линча. Чаще встречается другой, ненаследственный механизм формирования дефицита MMR (dMMR), в подавляющем большинстве случаев заключающийся в метилировании промотера MLH1 в самой опухоли. В результате dMMR появляется большое число мутаций со сдвигом рамки считывания, что приводит к формированию стоп-кодонов и синтезу нефункциональных белков. Микросателлиты представляют собой короткие последовательности в ДНК из 1-5 оснований, повторяющиеся до нескольких десятков раз. Микросателлиты встречаются и в норме, однако при dMMR их число увеличивается, что и может быть выявлено. Понятия dMMR и микросателлитная нестабильность (MSI) описывают один и тот же процесс. Микросателлитную нестабильность оценивают двумя методами – методом ПЦР и иммуногистохимическим [9].
При определении методом ПЦР выделяются 3 варианта MSI: MSI-Н (высокий уровень MSI), когда ≥2 маркеров нестабильны, MSI-L (низкий уровень MSI), когда нестабилен 1 маркер, и MSS (стабильный уровень), когда стабильны все маркеры. Значение низкого уровня MSI до сих пор четко не установлено, и этих пациентов расценивают как больных с MSS опухолями. Вторым вариантом диагностики dMMR является иммуногистохимическое исследование (ИГХ), когда в опухоли изучается экспрессия белков MSH2, MLH1, PMS2, MSH6. В случае отсутствия окрашивания хотя бы одного белка устанавливается дефицит MMR. Обе методики демонстрируют высокую (>95%) конкордантность и являются в сложных случаях взаимодополняющими, так как существуют редкие варианты нарушения MMR, диагностируемые только ПЦР или только ИГХ.
При раке эндометрия MSI-h/dMMR встречается у 48,2% пациенток с метастатическим процессом и может отличаться от первичной опухоли. В основном в таких опухолях отмечаются недифференцированные или смешанные гистологические варианты с высоким уровнем содержания опухоль-инфильтрирующих лимфоцитов. Часто опухоль локализуется в нижних сегментах матки. Но по данным многочисленных исследований прогноз пациенток с MSI-h/dMMR не отличается от больных с опухолями без нарушений в системе репарации ДНК [10,11].
Рак эндометрия и иммунотерапия
По данным статистики, в 2019 г. было диагностировано 62 000 новых случаев рака эндометрия в мире и, что особо настораживает, прогнозируется рост как заболеваемости, так и смертности со скоростью 1-2% в год [12].
Рак эндометрия – генетически гетерогенное злокачественное новообразование, состоящее из четырех различных фенотипов: POLE ультрамутации, гипермутация микросателлитной нестабильности (MSI), низкая копийность генов и высокая копийность генов [13]. Молекулярная характеристика рака эндометрия имеет большое значение для обоснования использования ингибиторов контрольных точек в этой злокачественной опухоли. В результате дефектной системы репликации ДНК, появления POLE-инактивирующих мутаций и дефекта в системе репарации неспаренных оснований ДНК (MMR) (MLH1, MSH2, MSH6, PMS2) происходит значительное увеличение мутационной нагрузки опухоли [14], котороое коррелирует с высоким уровнем неоантигенов и опухоль-инфильтрирующих лимфоцитов (TIL). Это создает определенное микроокружение опухоли, которое является благоприятным для иммунологического ответа [15]. Большинство рецидивов рака эндометрия имеют либо низкую копийность генов, либо высокую копийность с высокой микросателлитной стабильностью (MSS) опухоли, которые часто являются резистентными для лечения. И разработка новых подходов к лечению именно этой группы больных на сегодня является самой актуальной.
Монотерапия ингибиторами иммунных контрольных точек
В 2017 году в рамках 2 фазы исследования изучали активность пембролизумаба при 12 различных типах опухолей с дефицитом репарации ДНК (dMMR), в том числе были и больные раком эндометрия (N=15), где эффективность терапии была очень впечатляющей и составила 53% [8]. Это исследование также показало, что дефицит MMR является биомаркером ответа на лечение, предлагая новый вариант терапии для злокачественных опухолей с дефицитом MMR.
С 2017 года пембролизумаб одобрен для лечения распространенных форм опухолей с dММR/MSI-H, ранее получавших лечение, включая и рак эндометрия [16]. Также пембролизумаб и анти-PD-L1 препарат атезолизумаб изучались при раке эндометрия у 24 пациенток с PD-L1-положительном статусом опухоли, независимо от MSI статуса, и эффективность этих препаратов составила всего 13% [17, 18]. Во 2 фазе исследования при распространенном раке эндометрия (N=23) применяли монотерапию ниволумабом с эффективность лечения в 23%, независимо от MSI статуса [19].
Также в 1/2 фазе исследования изучался препарат достарлимаб (анти-PD-1) у 125 больных прогрессирующим раком эндометрия, где клинический ответ независимо от MSI статуса составил 29,6%. Частота ответов в группе MSI-H и MSS составила 48,8% и 20,3% соответственно. С последующим наблюдением в течение 10 месяцев 84% пациенток все еще находились на лечении, и медиана продолжительности ответа (DOR) не была достигнута [20].
Во 2 фазе исследования ингибиторы PD-L1 авелумаб (N=31) и дурвалумаб (N=70) показали объективный ответ 26,7% и 43% у пациенток с dММR и 6,25% и 3% со стабильным статусом MMR у пациенток распространенным раком эндометрия соответственно [21, 22]. Также в настоящее время продолжаются исследования монотерапии ингибиторов контрольных точек при рецидивирующем раке эндометрия – ниволумаба и пембролизумаба. В обоих исследованиях производится селекция пациентов в соответствии с MSI, POLE, или dMMR статусом.
Скромные ответы монотерапии ингибиторов контрольных точек подчеркивают общий принцип, что иммуногенность и противоопухолевые ответы зависят в значительной степени от мутагенности опухоли и, следовательно, изменить иммунологический ответ можно в сочетании иммунотерапии с комбинированной терапией.
Комбинация ингибиторов контрольных точек с другими методами лечения
В настоящее время проводится 3 фаза исследования ленватиниба с пембролизумабом в сравнении с доксорубицином или еженедельным паклитакселом в поздних линиях лечения рака эндометрия, а также в первой линии лечения продолжается исследование ленватиниба с пембролизумабом в сравнении с карбоплатином и паклитакселом.
Промежуточные результаты продолжающегося исследования 2 фазы дурвалумаба и тремелимумаба (анти-CTLA-4) в сравнении с одним дурвалумабом при рецидивирующем раке эндометрия независимо от статуса MMR (86% пациентов в каждой когорте были со стабильным статусом MMR) демонстрируют скромные результаты лечения: объективный ответ монотерапии дурвалумабом составил 14,8% и 11,1% при комбинации дурвалумаба с тремелимумабом [23].
До недавнего времени стандартом лечения распространенных форм рака эндометрия и рецидивов являлись монотерапия цитостатиками и гормонотерапия с медианой выживаемости без прогрессирования всего 1,0-3,2 месяца. Но с выявлением ряда биомаркеров подход к лечению такого резистентного к терапии рака, как рак эндометрия, существенно изменился: при опухолях с высокой мутационной нагрузкой (dММR/MSI-H) ингибитор контрольных точек пембролизумаб продемонстрировал высокую эффективность лечения.
Но доля пациентов со стабильным статусом MMR остается очень высокой, и для этой группы больных лечение комбинированной терапией ленватиниба с пембролизумабом является очень перспективным.
Что такое аденокарцинома кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Мешечкина В. Г., онколога со стажем в 8 лет.
Определение болезни. Причины заболевания
Аденокарцинома толстой кишки — это самая распространённая форма рака прямой кишки, опухоль развивается в толстой кишке и может метастазировать, как и большинство злокачественных новообразований.
Распространённость аденокарциномы толстой кишки
Факторы риска
Основной фактор риска аденокарциномы толстой кишки — возраст старше 65 лет. Риск развития аденокарциномы толстой кишки также возрастает при наличии некоторых наследственных синдромов:
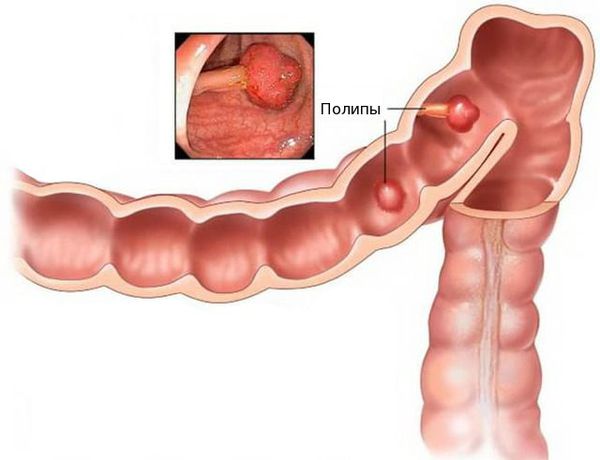
Благоприятным фоном для злокачественного перерождения клеток являются единичные или множественные полипы толстой кишки. Высокий риск перерождения в раковую опухоль имеют аденоматозные полипы. Отказ от их удаления может привести к развитию аденокарциномы.
Хронические воспалительные заболевания толстой кишки, такие как неспецифический язвенный колит и болезнь Крона, также повышают риск развития аденокарциномы.
К дополнительным факторам риска относят:
Симптомы аденокарциномы кишки
Клинические проявления аденокарциномы толстой кишки зависят от расположения опухоли, её типа, темпа роста и наличия сопутствующей патологии. Ранние формы рака являются случайной находкой, так как могут никак себя не проявлять. Их выявляют при эндоскопическом исследовании кишечника по поводу других заболеваний (например, колита, дивертикулита, холецистита, гастрита и др.) или при полостных или гинекологических операциях — аппендэктомии, миомэктомии и кесаревом сечении.
Наиболее частые симптомы аденокарциномы толстой кишки:
Опухоли левого фланка (сигмовидной и прямой кишки, селезёночного угла, нисходящего отдела) чаще манифестируют с запоров, примеси прозрачной или розоватой слизи и тёмной крови в кале, болезненных позывов, отдающих в промежность.
Поиск причины анемии невыясненной этиологии часто приводит к обнаружению рака правой половины толстой кишки.
Патогенез аденокарциномы кишки
Аденокарцинома — это злокачественная опухоль, возникающая из железистых клеток и способная образовывать метастазы (вторичные очаги опухолевого роста). Чаще всего заболевание развивается на фоне длительно существующих полипов, или разрастаний слизистой.
При хроническом повреждении полипов плотными каловыми массами и воспалении развивается дисплазия эпителия (нарушение деления и дифференцировки клеток), переходящая в рак. У кого-то этот процесс может занять десятки лет, у других развивается за два-три года.
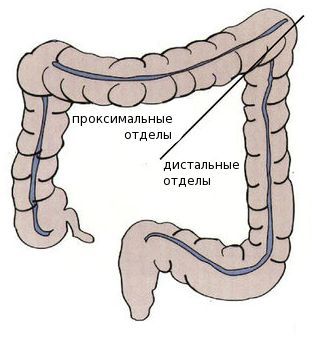
Среди пациентов с раком проксимальных отделов толстой кишки преобладают женщины — вероятно, это связано с наличием гормональных рецепторов эстрогенов в этих отделах. Дистальный рак толстой кишки более характерен для мужчин.
Классификация и стадии развития аденокарциномы кишки
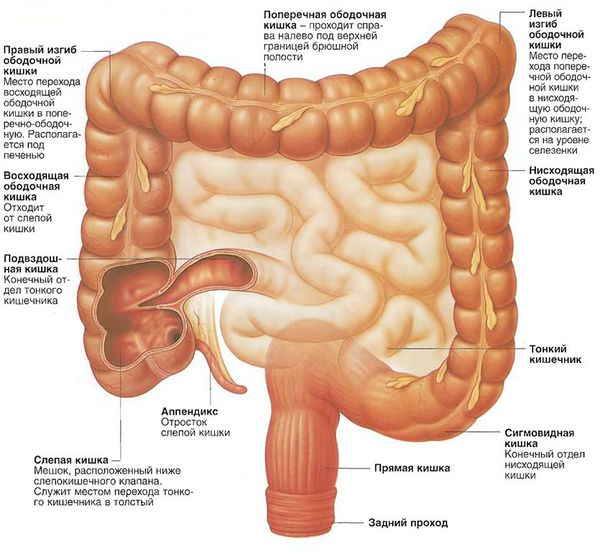
Виды аденокарциномы толстой кишки в зависимости от локализации:
Согласно последней классификации ВОЗ, гистологически выделяют две степени злокачественности аденокарциномы толстой кишки, опираясь на долю железистых структур в составе опухоли: высокую и низкую.
Стадирование новообразований толстой кишки по системе TNM-8 (2017 г.) представлено схемой:
Исходя из этих данных, опухоли присваивают определенную стадию, и далее она уже не меняется. Дальнейшее распространение процесса обозначается как прогрессирование.
Осложнения аденокарциномы кишки
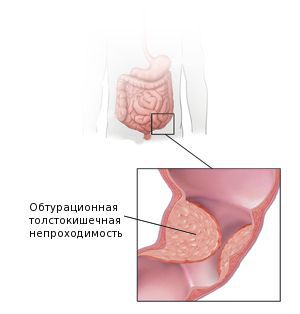
Также среди частых причин осложнений выделяют перфорацию и кровотечение из повреждённой опухоли. Это может явиться первым симптомом заболевания. Часто таких пациентов экстренно оперируют в условиях многопрофильного стационара, а не специализированного учреждения, и только при обследовании органов брюшной полости становится понятна причина перфорации.
Диагностика аденокарциномы кишки
Сбор анамнеза
Помимо описанных выше жалоб, с которыми первично обращаются пациенты, важны данные анамнеза. На первичном осмотре терапевту или онкологу следует отметить наличие наследственных синдромов, ассоциированных с раком толстой кишки, и хронических неспецифических воспалительных процессов толстой кишки, например неспецифического язвенного колита или болезни Крона.
Физикальное обследование
При физикальном обследовании, помимо общего осмотра и пальпации брюшной полости, обязательно проведение ректального пальцевого исследования, выявляющего изменения в области прямой кишки. Это один из самых простых диагностических приёмов, не требующий дополнительной подготовки и оборудования.
Лабораторная диагностика
Лабораторная диагностика включает:
Это анализы необходимы для исключения возможной сопутствующей патологии.
Биопсия
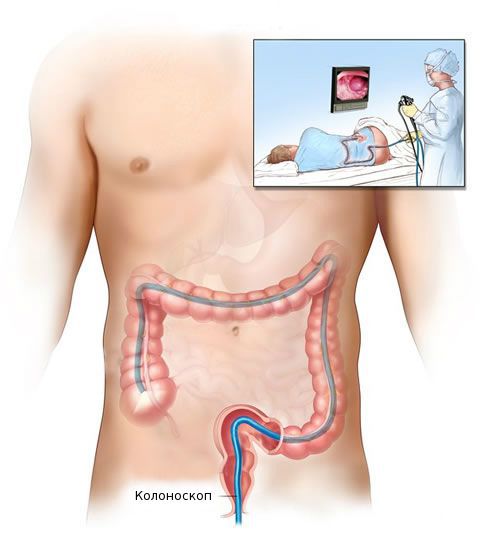
После общеклинического обследования проводят уточняющее исследование (биопсию) для определения гистологической структуры опухоли. Чаще всего биопсия выполняется во время колоноскопии — процедуры, при которой врач с помощи эндоскопа осматривает внутреннюю поверхность толстой кишки.
Ирригоскопия и КТ-колонография
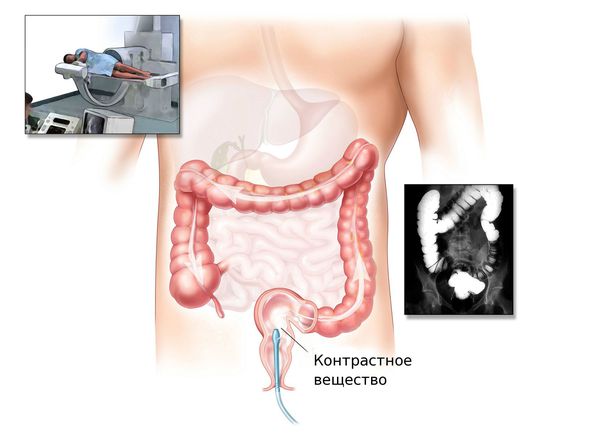
При невозможности проведения колоноскопии врач может назначить ирригоскопию или КТ-колонографию.
Ирригоскопия — это рентгенологический метод обследования толстого кишечника с помощью контрастного вещества, вводимого через прямую кишку.
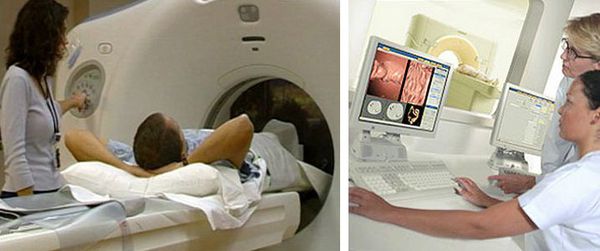
КТ-колонография — разновидность компьютерной томографии, проводимая при помощи компьютерного томографа.
Компьютерная томография (КТ)
КТ органов грудной клетки и брюшной полости с контрастом — стандарт обследования при раке ободочной кишки. Компьютерную томографию проводят для исключения метастазов в лёгких, лимфоузлах средостения, брюшной полости, канцероматоза (переноса раковых клеток из первичного очага), асцита (скопления жидкости в брюшной полости) и вторичного поражения печени.
Магнитно-резонансная томография (МРТ)
МРТ органов брюшной полости с внутривенным контрастированием применяют для планирования операции на печени при её вторичном поражении.
Для точной оценки размеров опухоли перед операцией и правильного стадирования по TNM проводится МРТ малого таза c применением контраста.
Дополнительно, при наличии болевого синдрома или изменений по КТ, проводится остеосцинтиграфия (ОСГ) — исследование состояния костей скелета.
При подозрении на вторичное поражение головного мозга (исходя из жалоб, осмотра и анамнеза) назначается МРТ головного мозга с внутривенным контрастированием.
Позитронно-эмиссионная томография, совмещённая с компьютерной томографией (ПЭТ/КТ)
ПЭТ-КТ не применяется как рутинный метод при первичной диагностике. Обследование проводят при подозрении на вторичные изменения по данным КТ или МРТ для получения дополнительных данных.
Лечение аденокарциномы кишки
Выбор метода лечения аденокарциномы толстой кишки обусловлен стадией онкологического процесса и наличием или отсутствием соматической патологии.
0-I стадия
На ранних стадиях рака ободочной кишки проводятся органосохраняющие операции, например эндоскопическую резекцию слизистой с удалением в подслизистом слое. При поражении краёв резекции, сосудистой, лимфатической или периневральной инвазии (проникновении раковых клеток в периневрий — слои соединительной ткани, образующие оболочку вокруг пучков нервных волокон), как факторах неблагоприятного прогноза, рекомендуется проведение расширенной операции — повторной резекции краёв.
II–III стадия
При резектабельном (c возможностью удаления) локализованном и местнораспространённом раке ободочной кишки II–III стадий на первом этапе предпочтительно оперативное лечение. Объём хирургического вмешательства определяется индивидуально.
Химиотерапия проводится при поражении лимфатических узлов, прорастании опухолью серозной оболочки и соседних органов, наличии факторов риска.
При распространённом раке ободочной кишки с резектабельными или потенциально резектабельными синхронными метастазами в печени или лёгких выполняют R0-резекцию (в пределах здоровых тканей).
Радиочастотная абляция и стереотаксическая лучевая терапия применяются как дополнительные методы к резекции печени и как самостоятельные методы лечения. Действие радиочастотной абляции основано на нагревании с помощью радиоволн поражённых тканей до высоких температур (90–100 °С).
Стереотаксическая лучевая терапия — это один из видов радиохирургии, который состоит в применении высокоточного излучения, воздействующего на опухоли.
При резектабельных очагах рекомендуется их одномоментное хирургическое удаление.
На послеоперационном этапе при резектабельных метастатических очагах показано проведение адъювантной (следующей за операцией) химиотерапии. Также возможно проведение дооперационной химиотерапии до шести циклов, удаление метастазов и первичной опухоли с дальнейшим продолжением химиотерапии до достижения шестимесячной суммарной продолжительности лечения.
IV стадия
Основная цель лечения на IV стадии заболевания — перевод при помощи химиотерапии нерезектабельных метастазов в резектабельные. Хороший эффект даёт добавление к основному лечению таргетной терапии ( целенаправленно воздействующей на специфические мишени в опухолевых клетках) и иммунотерапии.
При проведении нерадикальной резекции возможно продолжение терапии предоперационной комбинацией химиопрепаратов и моноклональных антител (препаратов, избирательно воздействующих на определённую молекулу, от которой зависит развитие болезни ) до достижения суммарной шестимесячной продолжительности лечения.
При генерализованном раке ободочной кишки с нерезектабельными метастазами применяют комбинацию химиопрепаратов. Возможно добавление таргетных препаратов. Цель лечения — максимально долго контролировать развитие заболевания при сохранении качества жизни.
При проведении химиотерапии каждые 1,5-2 месяца оценивают резектабельность опухоли (по данным КТ, МРТ). При преобладании метастатического поражения печени проводят:
Прогноз. Профилактика
Меры профилактики:
Микросателлитная нестабильность MSI
Микросателлитная нестабильность не обнаружена. Что это значит? Что такое MSI и MSS? Объясняет специалист
Что такое MSI и MSS?
Микросателлитная нестабильность чаще всего встречается при колоректальном раке, раке желудка и раке эндометрия, но может также обнаруживаться при многих других типах рака. Знание результата анализа на msi при онкологии поможет спланировать лучшее лечение.
Анализ на определение микросателлитной нестабильности MSI
Если у вас или вашего близкого человека диагностирован колоректальный рак, то важно знать опухолевый статус MSI-H. Чтобы его определить, необходимо направить опухолевый материал на молекулярно-генетическое исследование. Забор материала часто происходит во время операции по удалению опухоли, но это может быть сделано и с помощью биопсии. Результат вашего теста покажет статус MSI как MSI-H, или MSS (microsatellite stability, «микросателлитная нестабильность не обнаружена»).
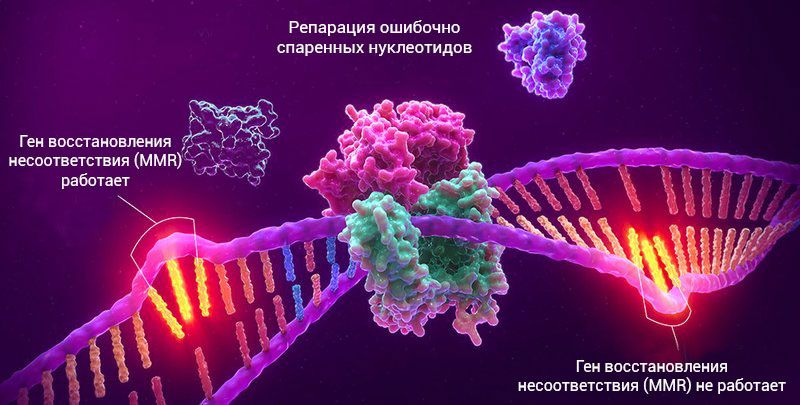
MSI-H приводит к тому, что гены, регулирующие ДНК (называемые генами восстановления несоответствия), не работают правильно. Гены восстановления несоответствия (MMR – mismatched repair) работают как генетические “проверки орфографии”, исправляя ошибки в ДНК по мере деления клеток, подобно тому, как исправляются опечатки в тексте.
Когда гены MMR перестают функционировать, то некоторые области ДНК могут стать нестабильными из-за накопления ошибок. Скрининговый тест MSI ищет изменения в последовательности ДНК между нормальной тканью и опухолевой тканью и может определить, существует ли высокая степень микросателлитной нестабильности, которая встречается примерно в 15% опухолей колоректального рака. Это часто происходит в опухолях, связанных с наследственным синдромом, синдромом Линча, хотя многие опухоли с высоким уровнем MSI являются спорадическими.
Дополнительный иммуногистохимический тест часто используется, чтобы сделать различие между наследственным и ненаследственным положительным анализом на микросателлитную нестабильность. Если MSI-H наследственная, то есть риск, что члены семьи онкологического больного также могут иметь синдром Линча, поэтому повышается вероятность развития колоректальных или других опухолей.
MSI-Н опухоли могут привлечь внимание иммунной системы. Под микроскопом в этих опухолях часто можно увидеть большое количество клеток иммунной системы. Иммунные клетки просто блокируются от полного выполнения своей работы. Поэтому пациенты с высоким уровнем микросателлитной нестабильности имеют положительный ответ на иммунотерапию. Таким образом, знание вашего состояния MSI чрезвычайно важно для выбора тактики противоопухолевого лечения.
MSS или микросателлитная стабильность обнаруживается приблизительно у 80-85% пациентов с колоректальным раком. Опухоли с мутацией MSS называются” холодными» и с точки зрения количества опухолевых генетических мутаций являются одним из наиболее сильно мутированных типов опухолей.