Адреногенетический синдром у детей что это
Адреногенитальный синдром: симптомы, лечение
Содержание
Какая связь между недостатком в организме гормона, контролирующего обмен углеводов и опосредующего стресс-реакции, и множественными нарушениями полового развития? Самая прямая. Примером служит т.н. адреногенитальный синдром у детей и взрослых. Этот довольно редкий наследственный недуг поражает людей обоего пола (в среднем — одного на пять–шесть тысяч) и уже в юном возрасте имеет свои характерные проявления.
Чем характеризуется? Кора надпочечников — важных «игроков» на «сцене» обмена веществ, процессов роста, развития, приспособления к меняющимся условиям и др., не поставляет организму должное количество химических регуляторов и координаторов этих процессов — кортизолаи, в некоторых случаях, альдостерона. Почему? Потому что в наличии врожденное нарушение образование необходимых для синтеза этих гормонов ферментов.
В результате, желая скомпенсировать эти недостатки, организм запускает каскад взаимодействий между различными органами, имеющий патологические следствия. Если более конкретно:
Формы врожденного адреногенитального синдрома определяются тем, какого (и в какой степени) фермента (или ферментов) организму не хватает. И, соответственно, какой конкретно гормон (или гормоны) находятся в дефиците. Чаще всего диагностируется т.н. вирильная форма. В самом названии (переводится как «мужская») кроется и комплекс сопутствующих ей симптомов — наличие вторичных мужских половых признаков у девочек и преждевременных гипертрофированных атрибутов сильного пола у мальчиков. В остальном недуг этой формы протекает довольно легко (т.н. компенсированная форма), поскольку работа фермента нарушена лишь частично, и при своевременном обнаружении хорошо поддается корректировке.
Две другие формы (редкие) — гипертоническая и сольтеряющая — более тяжелые. Настолько, что без их раннего выявления существует высокий риск гибели детей от сердечной и почечной недостаточности, и кровоизлияния в мозг.
Симптомы адреногенитального синдрома
Адреногенитальный синдром у новорожденных
Поскольку надпочечники под руководством мозговых центров (в ответ на нехватку кортизола) начинают усиленно трудиться еще внутриутробно, ребенок рождается на свет, уже имея избыток половых гормонов. В результате у новорожденных девочек регистрируют симптомы т.н. ложного гермафродитизма (наличия признаков обоих полов). А у новорожденных мальчиков — увеличенный копулятивный орган. Кроме того, аномальное количество половых стероидов приводит к избыточной пигментации наружных половых органов, кожи вокруг ануса и сосков. Перечисленные признаки характерны для самой распространенной (вирильной) формы адреногенитального синдрома.
При более редкой и тяжелой форме (сольтеряющей) к ним добавляются следствия потери организмом натрия и хлора, и задержки калия (из-за недостатка альдостерона):
Адреногенитальный синдром у девочек и мальчиков
С возрастом вышеуказанные признаки сохраняются (если не поставлен ранний диагноз и не начата заместительная терапия). К двум-четырем годам появляются симптомы преждевременного полового созревания с признаками маскулинизации (от латинского слова «мужчина, «самец») у девочек:
Касательно последнего пункта: высокие темпы роста характерны только для юного возраста. Довольно рано (к двенадцати годам) зоны роста закрываются, рост сильно притормаживается или останавливается вовсе. В результате в подростковом периоде наблюдается уже отставание в росте от сверстников.
Другими (неспецифическими) признаками не выявленных в очень раннем детстве гипертонической и сольтеряющей форм адреногенитального синдрома могут стать:
Длительная гипертензия рискует осложниться ухудшением зрения, сердечно-сосудистыми, почечными и мозговыми нарушениями (вплоть до инсульта).
Для правильной (и ранней) диагностики помимо осмотра и опроса необходимы лабораторные и инструментальные исследования:
Лечение адреногенитального синдрома
Чем раньше поставлен правильный диагноз, тем эффективнее лечение.
Прежде всего, оно состоит в заместительной терапии недостающими гормонами (на протяжении всей жизни человека). Хорошим подспорьем медикаментозным методам служат: диета с учетом формы патологии и индивидуальными особенностями организма и психотерапевтические сеансы. Возможно хирургическое вмешательство — удаление клитора, пластика влагалища.
Врожденная дисфункция коры надпочечников
Адреногенитальный синдром Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены. Синтез кортизола в надпочечниках плода под вли
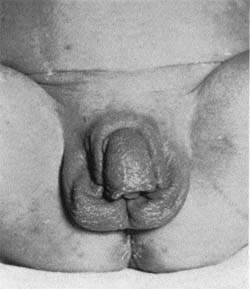 |
| Адреногенитальный синдром |
Hадпочечники секретируют кортикостероиды, которые по биологическим свойствам можно разделить на 4 группы: глюкокортикоиды, минералокортикоиды, андрогены и эстрогены.
Синтез кортизола в надпочечниках плода под влиянием адренокортикотропного гормона (АКТГ) начинается рано, в связи с этим дефект ферментных систем приводит к вирилизации до рождения ребенка. Так как к этому сроку формирование внутренних половых органов заканчивается, вирилизация затрагивает наружные половые органы.
Из различных ферментных дефектов недостаточность 21-гидроксилазы встречается наиболее часто и протекает в виде двух клинических форм: вирильного и сольтеряющего синдромов.
Вирильная форма связана с частичной недостаточностью 21-гидроксилазы. Как правило, при этом наблюдается компенсация функции коры надпочечников в результате повышенной секреции АКТГ, то есть уровень кортизола определяется на нижней границе нормы. Компенсаторное выделение АКТГ приводит к образованию значительного количества андрогенов, прогестерона, 17-гидроксипрогестерона, которые угнетают сользадерживающую активность на уровне канальцев почек, что ведет к значительному увеличению продукции альдостерона. У девочек с вирильной формой с рождения имеются признаки ложного гермафродитизма. Клитор гипертрофирован, напоминает по строению половой член, имеющий единое мочеполовое отверстие — урогенитальный синус, открывающийся у корня клитора, мошонкообразные большие половые губы.
| Врожденная дисфункция коры надпочечников является наследственным заболеванием, характеризующимся нарушением синтеза кортикостероидов, в основном кортизола, в результате дефицита ферментных систем коры надпочечников с одновременной избыточной продукцией андрогенов в надпочечниках |
У мальчиков с рождения отмечается увеличение полового члена, кожа мошонки морщинистая, выражена пигментация шва полового члена, кожи мошонки, передней линии живота, ареолы сосков.
В постнатальном периоде продолжается избыточная секреция андрогенов, усиливаются явления вирилизации. Дети быстрее растут, имеют развитую мускулатуру. Вначале больные обгоняют в росте сверстников, в дальнейшем же, после 9-10 лет, в связи с закрытием зон роста остаются низкорослыми. В возрасте 2–4 лет появляется преждевременное оволосение на лобке, подмышках, туловище, лице. У некоторых мальчиков значительно увеличивается половой член и появляются эрекции. Телосложение девочек мускулинного типа. В пубертатный период менструации не наступают, молочные железы не развиваются, так как повышенная секреция андрогенов надпочечниками по принципу обратной связи тормозит образование и выделение гонадотропинов. У мальчиков по этой причине угнетается развитие яичек — они остаются маленькими.
При сольтеряющей форме дефицит 21-гидроксилазы более глубокий, поэтому наряду с дефицитом образования кортизола происходит резкое снижение биосинтеза альдостерона. Если при вирильной форме потеря натрия, обусловленная избыточной продукцией прогестерона, 17-гидроксипрогестерона, компенсируется избыточной секрецией альдостерона, то при сольтеряющей форме снижено образование альдостерона. Результатом такого комбинированного действия является развитие клинической картины по типу острой надпочечниковой недостаточности.
| Заболевание наследуется по аутосомно-рецессивному типу и проявляется в гомозиготном состоянии. Распространенность составляет в среднем 1:4000-5000, а гетерозиготное носительство — 1:35-40 человек |
У новорожденных при этом синдроме резко выражены симптомы вирилизации, особенно у детей женского пола — полное заращение половой щели и появление мошоночноподобного образования. На 5–10-й день наступает быстрое ухудшение состояния, связанное с частой рвотой, жидким стулом. Развивается дегидратация, ребенок становится вялым, снижается масса тела. В сыворотке крови нарастает уровень кальция и снижается содержание натрия и хлора.
Гипертоническая форма дисфункции коры надпочечников, связанная с дефицитом 11b-гидроксилазы, встречается реже. В клинической картине, помимо признаков андрогенизации в раннем возрасте, характерно повышение артериального давления. При этой патологии отсутствует гиперплазия юкстагломерулярного аппарата почки и уровень ренина в плазме не повышен.
Дифференциальный диагноз врожденной дисфункции коры надпочечников у девочек первых лет жизни следует проводить с дисгенезией гонад, анорхизмом, истинным гермафродитизмом; у мальчиков — с преждевременным половым развитием различного генеза, в том числе с опухолью яичка, с андрогенпродуцирующей опухолью надпочечника (андростерома). Сольтеряющую форму у новорожденных дифференцируют с пилороспазмом и пилоростенозом.
У девочек старшего возраста при подозрении на врожденную дисфункцию коры надпочечников требуется исключить такие заболевания, как андрогенпродуцирующая опухоль яичника, стромальный текоматоз, поликистоз яичников.
Наиболее приемлемым средством заместительной терапии является преднизолон, который в течение длительного срока сохраняет достаточную концентрацию и обладает некоторым минералокортикоидным действием. Суточная доза его подбирается индивидуально и колеблется в зависимости от возраста: от 1,5–3 мг (для детей младше 3 лет) до 5 мг для детей старшего возраста. Реже применяют преднизолон, кортизон, дексаметазон. Соответственно суточному физиологическому ритму 17-гидроксипрогестерона принимать преднизолон рекомендуется рано утром, в 6-7 часов (причем в это время следует принять 2/3–1/2 дозы) и поздно вечером (23–24 часа). Глюкокортикоиды больные должны получать постоянно, так как отмена препарата ведет к декомпенсации заболевания.
При лечении больных с сольтеряющей формой врожденной дисфункции коры надпочечников к кортикостероидам добавляют минералкортикоиды. Это либо масляный раствор дезоксикортикостерона ацетата (ДОКА), либо таблетированный препарат кортинеф (0,1 мг), который в 5–10 раз активнее первого. Препараты назначаются в течение 1–2 недель ежедневно (ДОКА по 1–2 мл, кортинеф по 1 таб.) с последующим постепенным снижением дозы до оптимальной. Возможно поддерживающую терапию проводить через каждые 1–2 дня. У некоторых больных дефицит минералкортикоидов можно компенсировать добавлением в пищу поваренной соли. Обязательный контроль за весом, артериальным давлением, калием, натрием, ЭКГ.
Начальные дозы кортикостероидов должны быть в два раза выше физиологических.
При адекватном лечении у детей уменьшается мышечная гипертрофия, перераспределяется подкожножировая клетчатка, половое оволосение не прогрессирует. Если лечение начинают до закрытия ядер окостенения, то увеличивается темп роста. В случаях же поздней терапии эти дети так и остаются низкорослыми.
Гипертоническая форма заболевания лечится аналогично вирильной.
При присоединении интеркуррентных заболеваний дозу глюкокортикоидов увеличивают в 1,5–2 раза.
В случае развития острого криза недостаточности коры надпочечников показано внутривенное капельное введение жидкости (физиологический раствор и 5%-ный раствор глюкозы 100-200 мл/кг массы тела в сутки) в 4 приема, ДОКА 2–3 мг/кг массы тела в сутки. В последующие дни доза глюкокортикоидов быстро снижается и больной переводится на пероральный прием преднизолона.
Важное место в лечении врожденной дисфункции коры надпочечников занимает психотерапия, особенно в случае необходимости перемены пола ребенка.
Большинство девочек с этим заболеванием нуждается в проведении феминизирующей пластики наружных гениталий, удалении клитора и формировании малых половых губ после вскрытия урогенитального синуса. Коррекцию наружных гениталий рекомендуется проводить через год после назначения кортикостероидной терапии.
Публикации в СМИ
Синдром адреногенитальный
Адреногенитальный синдром — врождённое патологическое состояние, обусловленное дисфункцией коры надпочечников с чрезмерной секрецией андрогенов и проявляющееся признаками вирилизации.
Этиология и патогенез. Синдром обусловлен недостаточностью одного из ферментов, необходимых для синтеза кортизола. Дефицит кортизола стимулирует выработку АКТГ, что приводит к гиперплазии коры надпочечников и избыточной продукции АКТГ-зависимых стероидов, синтез которых при данной недостаточности фермента не нарушен (в основном, надпочечниковых андрогенов — дегидроэпиандростерона, андростендиона и тестостерона).
Генетические аспекты
• Недостаточность 21-гидроксилазы (*201910, КФ 1.14.99.10, 6p21.3, мутации генов CYP21, CA2, CYP21P, r ) наблюдают в 95% случаев адреногенитального синдрома •• При умеренном дефиците фермента развивается вирильная (неосложнённая) форма синдрома, при которой придают значение исключительно симптомам избытка андрогенов (глюкокортикоидная и минералокортикоидная недостаточность не проявляется) •• При полном блоке фермента развивается сольтеряющая (тяжёлая) форма (синдром Дебре–Фибигера). Наряду с уменьшением синтеза кортизола снижена продукция альдостерона; дефицит минералокортикоидов приводит к гипонатриемии, гиперкалиемии, дегидратации и артериальной гипотензии. Эта форма проявляется в первые месяцы жизни, чаще у мальчиков. Без лечения, как правило, заканчивается летально. Сольтеряющая форма может развиваться в результате недостаточности и других ферментов.
• Недостаточность 18-оксидазы (*124080, кортикостерон метил оксидаза I, r ) проявляется изолированным нарушением синтеза альдостерона с развитием сольтеряющей формы заболевания. Больные умирают в раннем детстве.
• Недостаточность 20,22-десмолазы (*201710, r ) проявляется нарушением синтеза кортизола, альдостерона и андрогенов. Это приводит к потере солей, глюкокортикоидной недостаточности и задержке полового маскулинизирующего развития у плодов мужского пола. Развивается так называемая врождённая липоидная гиперплазия коры надпочечников. Больные погибают в раннем детстве.
Клиническая картина
• Вирильная форма проявляется главным образом избытком андрогенов •• У девочек часто наблюдают врождённые изменения наружных половых органов (пенисообразный клитор, урогенитальный синус, мошонкообразные большие половые губы). В постнатальном периоде вирилизация продолжается (рост мышечной массы по мужскому типу, грубый голос, гирсутизм, аменорея, атрофия грудных желёз) •• У младенцев мужского пола следствие избытка андрогенов во время развития плода — макрогенитосомия. В постнатальном периоде наступает преждевременное половое созревание на фоне недоразвития яичек (сперматогенез отсутствует).
• Сольтеряющая форма наблюдается обычно у новорождённых и детей первого года жизни. Проявляется срыгиванием, рвотой, диареей, похуданием, артериальной гипотензией и судорогами. Дефицит кортизола обычно не имеет значительных клинических проявлений, т.к. несмотря на недостаточность конкретного фермента, стимуляция АКТГ и гиперплазия надпочечников поддерживают уровень кортизола на нижней границе нормы.
• Гипертензивная форма. Наряду с вирилизацией у девочек и макрогенитосомией у мальчиков отмечается стойкая артериальная гипертензия.
Дифференциальная диагностика. Её проводят с надпочечниковой недостаточностью, гермафродитизмом другого генеза, различными вариантами преждевременного полового созревания, андроген-продуцирующей опухолью надпочечников. Сольтеряющую форму следует также дифференцировать с пилоростенозом, кишечными инфекциями и интоксикациями.
ЛЕЧЕНИЕ
Лекарственная терапия. ГК пожизненно (подавляют гиперпродукцию АКТГ, а также надпочечниковых андрогенов). При натрий-дефицитной форме может оказаться необходимой заместительная терапия минералокортикоидами (флудрокортизон). Симптоматическое лечение (восстановление концентрации хлорида натрия).
Хирургическое лечение. В первые несколько лет жизни проводят реконструктивную операцию на наружных половых органах девочек.
Синонимы • Врождённая дисфункция коры надпочечников • Синдром Апера–Галле • Синдром Крука–Апера–Галле.
Сокращение. 17-ОКС — 17-оксикортикостероиды.
Код вставки на сайт
Синдром адреногенитальный
Адреногенитальный синдром — врождённое патологическое состояние, обусловленное дисфункцией коры надпочечников с чрезмерной секрецией андрогенов и проявляющееся признаками вирилизации.
Этиология и патогенез. Синдром обусловлен недостаточностью одного из ферментов, необходимых для синтеза кортизола. Дефицит кортизола стимулирует выработку АКТГ, что приводит к гиперплазии коры надпочечников и избыточной продукции АКТГ-зависимых стероидов, синтез которых при данной недостаточности фермента не нарушен (в основном, надпочечниковых андрогенов — дегидроэпиандростерона, андростендиона и тестостерона).
Генетические аспекты
• Недостаточность 21-гидроксилазы (*201910, КФ 1.14.99.10, 6p21.3, мутации генов CYP21, CA2, CYP21P, r ) наблюдают в 95% случаев адреногенитального синдрома •• При умеренном дефиците фермента развивается вирильная (неосложнённая) форма синдрома, при которой придают значение исключительно симптомам избытка андрогенов (глюкокортикоидная и минералокортикоидная недостаточность не проявляется) •• При полном блоке фермента развивается сольтеряющая (тяжёлая) форма (синдром Дебре–Фибигера). Наряду с уменьшением синтеза кортизола снижена продукция альдостерона; дефицит минералокортикоидов приводит к гипонатриемии, гиперкалиемии, дегидратации и артериальной гипотензии. Эта форма проявляется в первые месяцы жизни, чаще у мальчиков. Без лечения, как правило, заканчивается летально. Сольтеряющая форма может развиваться в результате недостаточности и других ферментов.
• Недостаточность 18-оксидазы (*124080, кортикостерон метил оксидаза I, r ) проявляется изолированным нарушением синтеза альдостерона с развитием сольтеряющей формы заболевания. Больные умирают в раннем детстве.
• Недостаточность 20,22-десмолазы (*201710, r ) проявляется нарушением синтеза кортизола, альдостерона и андрогенов. Это приводит к потере солей, глюкокортикоидной недостаточности и задержке полового маскулинизирующего развития у плодов мужского пола. Развивается так называемая врождённая липоидная гиперплазия коры надпочечников. Больные погибают в раннем детстве.
Клиническая картина
• Вирильная форма проявляется главным образом избытком андрогенов •• У девочек часто наблюдают врождённые изменения наружных половых органов (пенисообразный клитор, урогенитальный синус, мошонкообразные большие половые губы). В постнатальном периоде вирилизация продолжается (рост мышечной массы по мужскому типу, грубый голос, гирсутизм, аменорея, атрофия грудных желёз) •• У младенцев мужского пола следствие избытка андрогенов во время развития плода — макрогенитосомия. В постнатальном периоде наступает преждевременное половое созревание на фоне недоразвития яичек (сперматогенез отсутствует).
• Сольтеряющая форма наблюдается обычно у новорождённых и детей первого года жизни. Проявляется срыгиванием, рвотой, диареей, похуданием, артериальной гипотензией и судорогами. Дефицит кортизола обычно не имеет значительных клинических проявлений, т.к. несмотря на недостаточность конкретного фермента, стимуляция АКТГ и гиперплазия надпочечников поддерживают уровень кортизола на нижней границе нормы.
• Гипертензивная форма. Наряду с вирилизацией у девочек и макрогенитосомией у мальчиков отмечается стойкая артериальная гипертензия.
Дифференциальная диагностика. Её проводят с надпочечниковой недостаточностью, гермафродитизмом другого генеза, различными вариантами преждевременного полового созревания, андроген-продуцирующей опухолью надпочечников. Сольтеряющую форму следует также дифференцировать с пилоростенозом, кишечными инфекциями и интоксикациями.
ЛЕЧЕНИЕ
Лекарственная терапия. ГК пожизненно (подавляют гиперпродукцию АКТГ, а также надпочечниковых андрогенов). При натрий-дефицитной форме может оказаться необходимой заместительная терапия минералокортикоидами (флудрокортизон). Симптоматическое лечение (восстановление концентрации хлорида натрия).
Хирургическое лечение. В первые несколько лет жизни проводят реконструктивную операцию на наружных половых органах девочек.
Синонимы • Врождённая дисфункция коры надпочечников • Синдром Апера–Галле • Синдром Крука–Апера–Галле.
Сокращение. 17-ОКС — 17-оксикортикостероиды.
Врожденная дисфункция коры надпочечников у детей: этиопатогенез, клиника, лечение
В статье освещены принципы регуляции стероидогенеза в надпочечниках в норме и патологии. Приводятся современные данные о этиологии, патогенезе, клинике, лечении врожденной дисфункции коры надпочечников у детей.
The article deals with the principles of the regulation of steroidogenesis in the adrenal glands in normal and pathological conditions. Modern data on the etiology, pathogenesis, clinical presentation, treatment of congenital adrenal hyperplasia are presented.
Врожденная дисфункция коры надпочечников (ВДКН, врожденная вирилизирующая гиперплазия коры надпочечников, адреногенитальный синдром) является наследственным заболеванием, в основе которого лежит ферментативный дефект на различных этапах стероидогенеза, приводящий к дефициту синтеза кортизола и/или альдостерона. В настоящее время получены сведения о генетических дефектах этого заболевания, разработаны методы пренатального и неонатального скрининга 21-гидроксилазного дефицита. Своевременная диагностика и правильное лечение способствуют нормальному формированию физического и полового развития.
Физиология надпочечников
Надпочечники состоят из двух анатомических слоев: коркового и мозгового. Корковая ткань имеет три зоны, которые вырабатывают различные стероидные гормоны: клубочковая, пучковая и сетчатая. Исходной структурой биосинтеза этих гормонов является холестерин. Он синтезируется в самих надпочениках из ацетата и частично поступает с микрочастицами липопротеидов низкой плотности. В митохондриях из холестерина образуется прегненолон. В разных зонах последний подвергается различным превращениям.
В клубочковой зоне из него образуется прогестерон, с последующим синтезом дезоксикортикостерона (ДОК) — соединения, обладающего умеренной минералокортикоидной активностью. Основным продуктом клубочковой зоны является альдостерон с максимальным минералокортикоидным эффектом. Альдостерон в почечных канальцах задерживает натрий и выводит калий.
В пучковой зоне прегненолон через ряд промежуточных продуктов превращается в 17a-гидроксипрогестерон, последний под воздействием фермента 21-гидроксилазы превращается в 11-дезоксикортизол, предшественник кортизола.
Среди продуктов пучковой и сетчатой зоны имеются С-19 стероиды, обладающие андрогенной активностью, — дегидроэпиандростерон (ДГЭА), андростендион, тестостерон. Андрогеновая активность надпочечниковых стероидов в основном обусловлена их способностью преобразовываться в тестостерон.
В процессе стероидогенеза принимают участие несколько ферментных систем. Для биосинтеза кортизола и альдостерона необходимы 21-гидроксилаза и 11-гидроксилаза, которые экспрессируются только в надпочечниках. Другие ферменты являются общими для надпочечников и гонад [1]. Контролирует глюкокортикоидную функцию надпочечников адренокортикотропный гормон гипофиза (АКТГ) по типу обратной связи. Синтез и секреция альдостерона зависят от ренин-ангиотензиновой системы, уровня калия в сыворотке крови и в меньшей степени от гипофиза.
Этиопатогенез
Ферментативные дефекты при ВДКН обусловлены мутациями генов. В настоящее время выявлены многочисленные точечные мутации генов, определяющих тот или иной дефицит ферментов, коррелирующий с клиникой глюко- и минералокортикоидной недостаточности и выраженностью вирилизации.
Надпочечники секретируют стероиды, единым субстратом которых является холестерин. Под влиянием 11α-гидроксилазы из него образуются все предшественники кортикостероидов. При дефекте этого фермента нарушается синтез всех гормонов коры надпочечников — глюкокортикоидов, минералокортикоидов, андрогенов и формируется липоидная гиперплазия надпочечников, очень редкая форма заболевания. Практически все больные умирают в раннем детском возрасте.
Кортизол, местом синтеза которого является кора надпочечников при участии ферментов 17-гидроксилазы, 21-гидроксилазы, 3β-гидроксистероид дегидрогеназы (3β-ГСД), образуется через промежуточные продукты обмена 17а-оксигидропрогестерон и 11-дезоксикортизол.
Минералокортикоиды находятся под контролем 3β-ГСД, 21-гидроксилазы, 11β-гидроксилазы и синтезируются в клубочковой зоне надпочечников.
Синтез андрогенов происходит в сетчатом слое коры надпочечников и у большинства больных с ВДКН не страдает.
В подавляющем числе случаев выявляется дефицит фермента 21-гидроксилазы, который встречается с частотой 1:14 000 новорожденных, а в Российской Федерации 1:9500. Диагностика этого заболевания важна с первой недели жизни ребенка. Другие формы ВДКН встречаются редко: дефект STAR, дефицит 11α-гидроксилазы, дефицит 17α-гидроксилазы, 3β-ГСД, дефицит 21-гидроксилазы, дефицит 11β-гидроксилазы, дефицит оксидоредуктазы [2].
Дефицит 11β-гидроксилазы вызывает нарушение синтеза кортизола и приводит к избыточной продукции 11-дезоксикортикостерона, который способствует задержке натрия и воды в организме. Артериальная гипертензия и вирилизация наружных половых органов характерная картина для этой формы ВДКН.
Фермент 3β-ГСД участвует в биосинтезе минералокортикоидов, глюкокортикоидов, андрогенов. При дефиците этого фермента рано развиваются симптомы обезвоживания, рвота. Наружные половые органы как у девочек, так и у мальчиков имеют черты гермафродитного строения из-за дефицита активных андрогенов.
Снижение активности 17-гидроксилазы приводит к нарушению синтеза кортизола и половых гормонов, что обуславливает недоразвитие наружных гениталий у мальчиков и гипогонадизм у девочек в пубертатном периоде.
21-гидроксилаза участвует в биосинтезе кортизола и минералокортикоидов. При умеренном дефиците этого фермента снижается продукция кортизола, что вызывает повышение секреции АКТГ. Минералокортикоидная недостаточность чаще сопровождается грубым дефицитом 21-гидроксилазы. Снижение выработки дезоксикортикостерона и альдостерона стимулирует рениновую активность плазмы и, соответственно, ангиотензина II.
При ВДКН дефект перечисленных ферментных систем, обеспечивающих синтез глюкокортикоидов в системе гипоталамус–гипофиз–надпочечники, по принципу обратной связи вызывает избыточное выделение аденогипофизом АКТГ, который приводит к значительному повышению предшественников кортизола или альдостерона с избыточной одновременной продукцией адреналовых андрогенов.
В базальных клетках аденогипофиза помимо АКТГ образуется a- и β-меланоцитостимулирующие гормоны, общим предшественником которых является проопиомеланокортин. Продукция последнего стимулируется кортиколиберином, гормоном гипоталамуса и угнетается кортизолом.
Клинические особенности
В практике врача встречаются три основные формы болезни: вирильная, сольтеряющая и реже гипертоническая.
Вирильная форма ВДКН развивается при умеренном дефиците фермента 21-гидроксилазы и связана с действием надпочечниковых андрогенов, без выраженных симптомов глюко- и минералокортикоидной недостаточности.
Активная вирилизация плода начинается с 20–25 недели гестации, когда запускается гипоталамо-гипофизарно-надпочечниковая ось. При рождении наружные половые органы девочек имеют гетеросексуальное строение: различная степень гипертрофии клитора; сращенные большие половые губы напоминают мошонку, что формирует единое мочеполовое отверстие у основания клитора — урогенитальный синус. У некоторых больных внутриутробная андрогенизация настолько выражена, что наружные половые органы чрезвычайно сходны с мужскими, и нередко девочкам при рождении присваивается мужской гражданский пол. Гипертрофированный клитор напоминает нормальный половой член, мочеполовое отверстие открывается чаще снизу ствола на разном уровне его протяженности, давая повод для постановки диагноза «гипоспадия» [3].
Формирование наружных половых органов у мальчиков происходит по изосексуальному типу — при рождении ребенка можно заметить небольшое увеличение полового члена. Следует отметить, что в период новорожденности поставить диагноз вирильной формы ВДКН у мальчиков весьма затруднительно, т. к. явных нарушений в развитии половых органов не определяется. Однако у некоторых больных мужского пола с рождения можно заметить увеличение полового члена, морщинистость мошонки, пигментацию срединного шва пениса, кожи мошонки, срединной линии живота, ареолы сосков.
В постантенатальном периоде продолжается избыточная секреция андрогенов, усиливаются симптомы вирилизации. Если диагноз ВДКН не поставили своевременно, не начато соответствующее лечение, то вследствие анаболического действия андрогенов в первые годы дети быстро растут, у них активно развивается скелетная мускулатура, появляется грубый голос, гирсутизм (оволосение по мужскому типу на лице, груди, животе, конечностях), т. е. признаки маскулинизации. У девочек увеличивается размер клитора, отмечается его напряжение. У мальчиков ускоряется рост полового члена, рано появляются эрекции.
У девочек в пре- и пубертатном периодах отсутствуют вторичные половые признаки и менструации. Повышенная секреция андрогенов надпочечниками по принципу обратной связи блокирует выделение гонадотропинов в аденогипофизе. У девочек по этой причине яичники уменьшены в размерах, с множественными кистами, матка недоразвита, а у мальчиков угнетается развитие тестикул — они остаются допубертатными. У взрослых, не леченных больных, нередко наблюдается олигоспермия. У лиц обоего пола значительно ускоряется дифференцировка скелета («костный» возраст опережает паспортный). К 10–12 годам происходит закрытие эпифизарных зон роста костей, что определяет конечную низкорослость больных. Пропорции тела у них нарушены: широкий плечевой пояс, узкий таз, хорошо развитая мускулатура. У девочек не развиваются молочные железы [4].
Степень выраженности влияния андрогенов при дефиците 21-гидроксилазы связана с индивидуальными особенностями метаболизма предшественников андрогенов и различием в активности периферических рецепторов андрогенов.
Сольтеряющая форма обусловлена более выраженным дефицитом фермента 21-гидроксилазы. Болезнь проявляется с первых недель после рождения и представляет серьезную угрозу жизни больному ребенку. Клинически эта форма характеризуется рвотой, расстройством стула, дегидратацией, снижением артериального давления (АД). У таких детей следует обратить внимание на потемнение кожи, реже — слизистых оболочек. Происходит быстрая потеря массы тела ребенка, что можно охарактеризовать как аддисонический криз. Клинические проявления болезни связаны со снижением биосинтеза альдостерона, что приводит к потере натрия через почки, кишечник, потовые железы. Эти симптомы болезни являются ведущими и часто приводят к диагнозу острого кишечного токсикоза и экзикоза как инфекционного, так и ферментативного характера (лактазная недостаточность).
Особенности в нарушении строения наружных половых органов у девочек быстро направляют мысли врача на возможность ВДКН. У мальчиков диагноз вызывает определенные затруднения. Однако именно эта форма болезни приводит впервые к правильному диагнозу у них при соответствующих электролитных нарушениях и результатах других лабораторных инструментальных методов обследования.
Гипертоническая форма ВДКН встречается в популяции в 10 раз реже, чем предыдущие формы, и обусловлена дефектом гена, контролирующего 11β-гидроксилазу. Дефицит этого фермента приводит к недостаточному образованию кортизола, что стимулирует выработку АКТГ. Повышается количество стероидов, предшествующих ферментативному блоку: 11-дезоксикортизола и 11-дезоксикортикостерона, надпочечниковых андрогенов. В клинической картине болезни, кроме симптомов вирилизации, повышение АД за счет 11-дезоксикортикостерона, обладающего минералокортикоидной активностью. Это способствует задержке натрия и жидкости в организме. Последние два фактора приводят к повышению АД, которое обнаруживается в связи с трудностью его измерения у детей раннего возраста в 3–4 года, вследствие длительно текущей гипертонии могут быть выражены изменения со стороны глаз, сердца и почек. Имеется корреляция между степенью вирилизации наружных половых органов и артериальной гипертензией. При этой форме ВДКН отсутствует гиперплазия юкстагломерулярного аппарата и уровень активности ренина в плазме не повышен [3].
При ВДКН у детей обоих полов истинный пубертат наступает позже. У девочек нормальный менструальный цикл может быть только при применении сбалансированной гормональной терапии. Но у детей, лечение которых начато поздно, после появления сесамовидной косточки (рентгенография кисти рук), возможно преждевременное половое развитие. Причина этого феномена объясняется активацией гипоталамуса после уменьшения выделения надпочечниковых андрогенов в результате глюкокортикоидной терапии. В этих случаях ростовой прогноз ухудшается.
У девочек с дефицитом 21-гидроксилазы в раннем возрасте преобладают маскулинный тип телосложения, а также мальчиковые черты поведения — предпочтение механических игрушек, более жесткий тип общения со сверстниками. Интеллектуальное развитие таких детей не страдает.
Новорожденный, имеющий бисексуальное строение наружных половых органов, должен быть обязательно осмотрен эндокринологом и урологом. Необходимо провести пальпацию в области расщепленной мошонки на наличие тестикул. При отсутствии их назначается ультразвуковое исследование (УЗИ) органов малого таза и надпочечников. У больных с женским биологическим полом видны гипоплазированная матка, надпочечники увеличены в размере, однородны, с четкими ровными контурами. При длительном течении заболевания надпочечники становятся аденоматозными с неровными краями.
Диагностика
С первых дней жизни ребенка вирильная и сольтеряющие формы болезни характеризуются высоким уровнем 17-оксипрогестерона в крови, который в 10–100 раз превышает нормальные показатели (15–20 нмоль/л). С учетом суточного ритма исследование 17-оксипрогестерона достаточно проводить один раз, в интервале от 7 до 9 часов утра, для чего необходимо взять каплю крови ребенка на фильтровальную бумагу на 2–5 день жизни. Неонатальный скрининг эффективен для диагностики классических форм дефицита 21-гидроксилазы. Известна возможность проведения этого теста и со слюной ребенка, а также в амниотической жидкости в первый триместр беременности с целью пренатальной диагностики ВДКН. В нашей стране неонатальный скрининг проводят с 2006 г. При положительном результате повторно проводят исследование. В сомнительных случаях с целью подтверждения заболевания проводят ретестирование с использованием тандемной масс-спектрометрии и молекулярно-генетического анализа [5, 6].
Важным диагностическим критерием служит определение тестостерона, но в более поздние сроки — с 4–5 месяцев жизни. Уровень его обычно повышается в 5–10 раз по сравнению с нормальными показателями (0,17–0,7 нмоль/мл).
Помогает в диагностике дефицита 21-гидроксилазы повышение уровня АКТГ, а у больных с сольтеряющей формой одновременно возрастает активность ренина плазмы. При гипертонической форме ВДКН повышен уровень 11-дезоксикортизола и 11-дезоксикортикостерона в крови, непосредственных предшественников ферментативного блока 11β-гидроксилазы. В диагностике неклассической формы дефицита 21-гидроксилазы и дифференциальной диагностике редких форм ВДКН является проба с синактеном с определением широкого спектра стероидов.
При рождении ребенка с интер- или гетеросексуальным строением наружных гениталий обязательным диагностическим методом исследования должно являться определение полового хроматина и кариотипа. Выявление кариотипа 46ХХ у такого ребенка с большей вероятностью может говорить о наличии 21-гидроксилазной недостаточности. Иногда указанные исследования необходимы и у мальчиков с двусторонним брюшным крипторхизмом и гипоспадией уретры, что также может вызвать сомнение в правильном установлении пола ребенка.
Характерным признаком сольтеряющей формы ВДКН при лабораторном исследовании является нарастание уровня натрия и хлора. Изменяется соотношение натрия к калию в сторону снижения. Гиперкалиемия может быть выявлена и на электрокардиографии. Всем новорожденным мужского пола с клиническими признаками обезвоживания, сочетающимися с гиперкалиемией и гипонатриемией, необходимо исследовать содержание 17-оксипрогестерона в крови.
Для диагностики ВДКН и уточнения половой принадлежности необходимо проводить УЗИ надпочечников, матки, яичников. В норме на УЗИ надпочечники имеют треугольную или округлую форму, при ВДКН определяется их гиперплазия, которую одновременно необходимо дифференцировать с андростеромой. При опухолях надпочечников проба с дексаметазоном должна быть отрицательной, высокая концентрация ДГЭА-С не изменяется на этом фоне. В настоящее время используется также компьютерная томография надпочечников и внутренних гениталий.
Лечение
Основной задачей лечения является заместительная терапия глюкокортикоидами при вирильной форме и глюко- и минералокортикоидами — при сольтеряющей форме ВДКН. Назначение этих гормонов подавляет избыточную секрецию АКТГ и снижает уровень стероидов, секреция которых повышена в результате ферментативного дефекта. При регулярном применении кортикостероидов уменьшается вирилизация гениталий, дети нормально растут, у девочек под влиянием собственных овариальных гормонов развиваются молочные железы, происходит становление менструального цикла. У мальчиков в обычные сроки начинается истинное половое развитие, появляется сперматогенез.
Критериями компенсации при вирильной форме болезни являются нормализация темпов роста и полового развития, скелетного созревания, отсутствие признаков прогрессирования вирилизации и кризов острой надпочечниковой недостаточности, снижение 17а-гидропрогестерона и тестостерона в крови. При возникновении у больных интеркуррентных заболеваний необходимо увеличивать дозы глюкокортикоидов в 1,5–2 раза.
Детям с сольтеряющей формой ВДКН необходимо назначить минералокортикоиды. Среди них широко в практике используется флудрокортизон, в таблетке которого содержится 0,1 мг препарата. Суточная доза составляет 0,05–0,3 мг и распределяется в 2–3 приема: утром, перед обедом, иногда перед сном. Лечение следует начинать с меньших доз — 1/4–1/2 таблетки. В дальнейшем под контролем общего состояния больного и уровня электролитов крови, а также данных электрокардиографии (ЭКГ) дозу корригируют. У детей первого года жизни потребность в минералокортикоидах выше и у некоторых детей может составлять 0,3 мг в сутки. С пищей рекомендуется дополнительно принимать поваренную соль (1–4 г). Об адекватности применяемой дозы можно судить по показателю рениновой активности, который снижается при избыточной дозе и повышается при недостаточности.
Критериями правильного лечения сольтеряющей формы ВДКН являются исчезновение дегидратации, тошноты, рвоты, нормализации АД, содержания натрия и калия в сыворотке крови. Следует обратить внимание на необходимость наиболее адекватной терапии этих больных. Нужно помнить, что перерыв в лечении неизбежно приводит к рецидиву заболевания, а большие дозы глюкокортикоидов — к быстрому нарастанию веса, гипертонии, появлению стрий на коже, матронизму, остеопорозу, снижению иммунитета, образованию язв в желудке и кишечнике, повышению уровня сахара в крови. В связи с этим необходим систематический контроль дозы препарата по данным 17ОНП, а также уровня активности ренина в плазме. Содержание 17ОНП в сыворотке может превышать нормальные показатели не более чем в 2 раза.
Тяжелым осложнением сольтеряющей формы ВДКН является криз острой надпочечниковой недостаточности, который проявляется бледностью кожных покровов, акроцианозом, похолоданием конечностей, профузным потом, гипотермией, тошнотой, рвотой, жидким стулом. У маленьких детей быстро нарастают симптомы эксикоза — западение большого родничка, заостренные черты лица, сухость кожи, снижение тургора ткани, снижение АД, тахикардия. В крови нарастает уровень калия и снижается содержание натрия, меняется соотношение натрия к калию, оно снижается до 20 и ниже (норма 30). Гиперкалиемия может вызвать блокаду сердца с последующей остановкой его. Все это требует срочной лечебной помощи больным. Для выведения из криза необходима не только заместительная гормональная терапия, но и борьба с дегидратацией. С этой целью используются капельное внутривенное введение физраствора и 5% раствора глюкозы из расчета 100–150 мл на кг массы тела в сутки и внутривенное введение гидрокортизона 10–30 мг на кг массы тела в сутки или преднизолона 10–15 мг на кг массы тела, распределенные на 4–6 приемов, а также ДОКСА не менее 2–3 мг в течение первых суток.
Следует заметить, что применение преднизолона, мало влияющего на задержку жидкости, вместо гидрокортизона ведет к более медленной компенсации обменных процессов во время аддисонических кризов. Более того, применение таких препаратов, как дексаметазон или метилпреднизолон, в данной ситуации нецелесообразно, т. к. они обладают только глюкокортикоидной активностью в отличие от гидрокортизона.
В последующие сутки продолжается инфузионная терапия с постепенным снижением глюкокортикоидов и минералокортикоидов. После улучшения состояния пероральное лечение гидрокортизоном по 12,5–25–50 мг каждые 6 часов. Вместо ДОКСА при стабильном улучшении состояния через 3–5 дней назначают лечение флудрокортизоном, который обладает выраженным минералокортикоидным свойством (в 5–10 раз превышает ДОКСА) и умеренным глюкокортикоидным эффектом. Лечение надо начинать с меньших доз — 1/4 или 1/2 таблетки один раз утром. В дальнейшем под контролем общего состояния больного и уровня электролитов крови, а также данных ЭКГ дозу флудрокортизона увеличивают до 1, а иногда до 2 таблеток в сутки, при этом можно уменьшить дозу гидрокортизона или преднизолона.
При назначении минералокортикоидов нужно следить за симптомами возможной передозировки препарата: появление отечности, повышение АД, парестезии, параличи, повышение уровня натрия в крови. В этих случаях достаточно сократить дозу препарата или временно отменить его, прервать дачу поваренной соли. Следует назначить хлористый калий в растворе или в порошке. При выраженной гипокалиемии показано в/в капельное введение 4% хлорида калия 10–15 мл в 250 мл 5% раствора глюкозы.
К отработанной схеме лечения переходят при отсутствии рвоты, нормализации стула. Как уже было сказано, гипертоническая форма ВДКН у детей встречается очень редко. При лечении этой формы наряду с глюкокортикоидами назначаются гипотензивные препараты. Применение только гипотензивных средств не эффективно.
Хирургическое лечение при ВДКН применяется у лиц с генетическим и гонадным женским полом для устранения вирильных нарушений наружных гениталий и осуществляется только в специализированных клиниках. Корригирующая пластическая операция на фоне адекватной гормонотерапии проводится через год после начала лечения: на первом этапе производят клитеротомию, на втором — ближе к пубертатному периоду — вскрытие урогенитального синуса (интроитопластику). Даже при резкой вирилизации наружных гениталий не встает вопрос об образовании искусственного влагалища, т. к. оно развивается до обычных размеров под влиянием систематического лечения глюкокортикоидными препаратами. Хирургическое лечение продиктовано не только косметической необходимостью. Гетеросексуальное строение наружных гениталий может приводить к патологическому формированию личности и даже к суициду. Корригирующая операция направлена на реализацию возможности нормальной половой жизни и выполнения детородной функции [5].
Выбор пола у больных ВДКН является очень важным вопросом, который может быть правильно решен при раннем распознавании болезни — в первую неделю жизни. Но, к сожалению, нередко при выраженной вирилизациии наружных половых органов девочки с рождения регистрируются как мальчики и получают соответствующее воспитание. При ВДКН у лиц с генетическим и гонадным женским полом единственно целесообразным решением является выбор женского пола не только в первые 2 года жизни, но в любом возрасте, в котором впервые был правильно определен биологический женский пол.
Однако перемена пола — очень сложный вопрос для больного, особенно в пре- и пубертатном периоде. При этом необходимо, учитывая возраст больного, знать его психосоциальные и психосексуальные установки. Подчас нужна длительная постепенная психологическая подготовка, а после перемены гражданского пола — продолжительная адаптация. Нередко семье больного приходится сменить место жительства для меньшей психологической травматизации ребенка и всей семьи. Пациенты, пожелавшие сохранить ошибочно присвоенный им мужской пол, обречены на бесплодие, на невозможность полноценной жизни из-за порока развития «полового члена», на необходимость применять андрогены на фоне глюкокортикоидной терапии. Кроме того, приходится прибегать к оперативному вмешательству — удалению внутренних половых органов (матки и ее придатков), что может привести к развитию посткастрационного синдрома. Отечественные авторы считают врачебной ошибкой сохранение мужского пола больным с генетическим и гонадным женским полом. В ряде случаев сохранение мужского пола является следствием недостаточной психологической подготовки больного, которая должна проводиться урологом, гинекологом, психотерапевтом, сексопатологом (в зависимости от возраста пациента).
В то же время при правильном подходе к смене гражданского пола и началу лечения глюкокортикоидами быстро осуществляется феминизация — развитие молочных желез, появление менструаций и становится реальной возможность осуществления репродуктивной функции в дальнейшем. Следует подчеркнуть, что смена гражданского пола должна осуществляться с учетом всех юридических правил.
При своевременно начатом и адекватно проводимом лечении, особенно вирильной формы ВДКН, прогноз в отношении жизни и трудовой деятельности может быть вполне благоприятным.
Особого внимания требует сольтеряющая форма болезни, дающая тяжелые обострения у ребенка при присоединении интеркуррентных заболеваний, стрессовых состояниях или нерегулярном лечении.
Больные ВДКН должны находиться на диспансерном учете у эндокринолога, т. к. они нуждаются в пожизненном применении гормональных препаратов. В зависимости от возраста и адекватности проводимой терапии дети осматриваются эндокринологом не реже 2 раз в год (по показаниям — чаще); минимум дважды в течение года у них должны контролироваться показатели 17ОНП.
Литература
В. В. Смирнов, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва