Ангиолимфатическая инвазия что это
Инвазивный рак
Независимо от вида и степени онкологии, следует отметить, что это крайне тяжелое заболевание. Причем его течение и развитие крайне сложно предугадать. Оно имеет определенные особенности.
«Инвазивный рак» – таким термином специалисты называют вид онкологии, при котором ткани, подвергшиеся мутации, распространяются за границы пораженной области на здоровые части тела. Начальная стадия инвазивного рака проявляется как развивающаяся опухоль. Этот процесс подразумевает проникновение измененных онкологией клеток в ткани на глубину до 6 мм за пределами пораженного участка.
Практика показывает, что больше всего шансов на эффективное лечение болезни наблюдается в момент стадии микроинвазии. Раковые опухоли имеют одинаковую природу происхождения с инвазивной карциномой.
Какие виды инвазивного рака существуют
Сегодня врачи-онкологи выделяют три разновидности инвазивного рака.
Первая. Карцинома протоковая. Данная патология возникает у женщин. Измененные клетки атакуют проток, по которому во время лактации течет молоко. Такой вид заболевания является наиболее распространенным и считается чрезвычайно опасным. Аномальные клетки в случае возникновения такой карциномы быстро проникают в лимфоток или системные кровотоки. Такая онкология проявляется в изменении формы женских сосков, приводя их деформации. Чаще всего с подобной проблемой сталкиваются женщины от 55 лет. Есть три стадии протокового карцинома:
Вторая. Рак протоковый преинвазивный. В этой стадии патология еще не может распространяться на ткани других органов, однако есть высокий шанс того что рак перейдет в инвазивную форму.
Третья. Рак дальковый инвазивный. Такой вид онкологии развивается из частей клеточных желез. Этот вид заболевания встречается в 10-16% случаев. При таком раке возникает одна или несколько опухолей. Еще стоит отметить, что данный тип рака крайне сложно диагностируется, так как при его развитии нет внешних факторов указывающих на заболевание.
Неспецифированные формы инвазивной онкологии
Данная форма заболевания отличается тем, что ее сложно отнести к конкретному виду: пртоковой карциноме или дольковому раку. Сегодня специалисты выделяют следующие виды неспецифированного рака:
Общим свойством всех выше перечисленных патологий является их гормонозависомость. Рак имеет эстрогены и рецепторы, поэтому его можно эффективно лечить с помощью специальной гормональной терапии. Однако если болезнь изначально образовалась в предменопаузе, то это значит, что она не имеет рецепторов и нужно применять другие средства борьбы.
Специалисты считают, что при развитии инвазивного рака, медуллярный вид опухолей лучше подается терапии и лечению, чем дольковая карцинома, протоковый рак или онкология Педжета.
Симптомы заболевания
В зависимости от того, на какой стадии находится инвазивный рак молочной железы, или инвазивный рак неспецифического типа, их симптомы могут проявляться по-разному. До того момента пока рак не выходит за границы своей изначальной структуры многие женщины в принципе не обращают на него внимание. Некоторые могут жаловаться на дискомфорт в момент касания молочных желез. Признаки морфологического типа на ранних стадиях инвазивного рака диагностировать крайне сложно. Только после того как опухоль начнет расти, появятся явные симптомы в виде:
Когда обращаться к специалисту
Инвазивный рак, как понятно из всего вышесказанного, очень сложно определить на первых стадиях. Однако женщины должны знать при появлении первых симптомов им следует идти к специалисту.
Сегодня диагностировать инвазивный рак молочной железы или инвазивный рак неспецифического типа могут опытные специалисты онкоцентра София, который расположен в центре Москвы.
Стадии заболевания
Врачи выделяют несколько стадий инвазивного рака.
Инвазивный рак шейки матки как развивается болезнь
Рак матки по статистике находится на втором месте по распространенности после рака молочных желез. Данное заболевание может иметь как неинвазивную так инвазивную форму. При этом переход от одного этапа болезни к другому может происходить очень долго.
В основном инвазивный рак шейки матки, как и инвазивный плоскоклеточный рак, встречается у женщин старше 40 лет. Фактором развития заболевания могут быть разные обстоятельства, в том числе он может развитья на фоне других болезней, например:
Какая бы ни была причина возникновения инвазивного плоскоклеточного рака или другого типа онкологии в онкоцентре София всегда готовы помочь людям с их проблемами. Здесь проводят эффективное лечение инвазивного рака.
Симптомы инвазивного рака матки
Среди симптомов данного заболевания доктора отмечают следующие факторы:
Все эти признаки повод пойти к врачу. В онкоцентре София квалифицированные специалисты проведут необходимые обследования, применяя самое современное диагностическое оборудование. В случае выявления патологии здесь предложат лучшее лечение инвазивного рака. Также специалисты смогут сделать прогноз по инвазивному раку для конкретного пациента. Найти центр можно в центральном округе Москвы.
Диагностирование рака
Сегодня диагностирование онкологии находится на очень высоком уровне. Благодаря современным технологиям врачи могут выявлять болезнь на ранних стадиях и проводить терапию. Среди средств, которые применяют специалисты, следует отметить:
А также многие другие аппараты.
Онкоцентр София располагается в ЦАО Москвы по адресу: 2-й Тверской-Ямской переулок, дом 10, метро «Маяковская». Записаться на прием можно через форму обратной связи или по телефону +7 (495) 995-00-34.
Карцинома
Один из самых распространенный типов раковых опухолей у людей – карцинома. Этот тип неоплазии, злокачественного роста, который зарождается в тканях, которые покрывают как внешние поверхности тела, так и внутренние полости. Этот вид онкологии относится к опухолям эпителиального происхождения.
Акции
Запись на консультацию со скидкой 10%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Общие данные

Кроме того, будут характеризоваться как карцинома и те злокачественные опухоли, которые состоят из клеток, подвергшихся трансформации, которые имеют специфические характеристики на молекулярном, гистологическом и клеточном уровне, типичные для эпителиальной ткани.
По данным ВОЗ на долю карцином приходится ежегодно до 9,5 млн смертей. Лечение этих видов рака (карциномы) достаточно трудная задача, показатели выживаемости очень разнятся. Участки органов, часто поражаемые карциномами, включают:
Причины возникновения карцином
Пока точные причины, по которой развиваются разные типы рака, включая карциному, не определены. Но ученые выделили ряд факторов, предрасполагающих к развитию патологии:
Типы карциномы, классификация
Хотя карциномы могут возникать во многих частях тела, наиболее распространены следующие типы карциномы:
Основа классификации карцином – тип клеток и их локализация, а также стадии карциномы.
Карциномы могут распространяться на другие части тела или ограничиваться основным местом. Заболевание имеет различные формы, в том числе:
Важно знать также признаки опухоли в разных стадиях развития.

Стадия 2 – опухоль не более 5 см в диаметре, в лимфоузлах определяются единичные метастазы.
Стадия 3 – опухоль превышает 50 мм диаметром, есть массивные метастазы в области лимфоузлов.
Стадия 4 – определяются отдаленные метастазы по всему организму.
Карцинома: симптомы
Врачи дают описание того, как выглядит тот или иной тип карциномы.
Если выявлена базальноклеточная карцинома, вероятно, она возникла из-за слишком длительного пребывания на солнце. Возможно, было несколько серьезных солнечных ожогов или в течение жизни человек много времени проводил на солнце.
Когда плоскоклеточный рак развивается в коже, он часто обнаруживается на участках, подверженных воздействию солнца, таких как:
Плоскоклеточная карцинома, которая развивается на коже, имеет тенденцию к росту и распространению больше, чем рак базальных клеток. В редких случаях он может распространяться на лимфатические узлы.
На фоне карциномы возможен синдром интоксикации с лихорадкой, потерей аппетита и веса, слабостью, локальные изменения в области пораженной кожи, изменение цвета, уплотнение. Если поражен внутренний орган, страдают его функции.
Диагностика
Постановкой диагноза занимаются онкологи, они помимо оценки жалоб и осмотра, назначают целый ряд обследований. К ним относят:
Методы лечения

Карцинома: прогноз

Рекомендации
Для рака кожи основные рекомендации – это снизить облучение кожи УФ-лучами и оградить себя от влияния потенциальных канцерогенов. В целом, ведение здорового образа жизни с рациональным питанием, дозированными нагрузками помогает снизить риск онкологии.
Ангиолимфатическая инвазия что это
Можно сказать, что раковые клетки в определенной степени не реагируют на механизмы, контролирующие рост и развитие нормальной ткани. При пролиферации нормальной ткани непосредственный контакт клетки со своими соседями обычно служит сигналом к прекращению размножения. Это контактное торможение отсутствует в опухолевых тканях.
При подкожном введении раковых клеток иммунодефицитным мышам происходит рост и развитие опухоли, что никогда не случается при введении здоровых клеток. Раковые клетки отличаются от здоровых по составу мембранных гликопротеинов, по микропотенциалам на клеточной мембране, а также характеризуются повышенным содержанием сиаловой кислоты. Локомоторный клеточный аппарат (микротрубочки и микрофиламенты) раковых клеток деградирует, клетка теряет присущие ей формы, отмечается миграция цитоплазмы раковой клетки в зону контакта со здоровыми клетками.
Одновременно раковые клетки становятся локально инвазивными, хотя биохимические основы этого свойства до сих пор четко не выявлены. Опухолевые клетки часто демонстрируют пониженную адгезивность в сравнении с нормальными клетками. Важным моментом механизма инвазии является секреция определенных ферментов. Некоторые ферменты играют ключевую роль в протеолизе внутриклеточного матрикса, который всегда сопровождает инвазию раковых клеток. К таким ферментам относится семейство матричных металлопротеиназ (ММП), которое включает в себя колллагеназы, желатиназы и стромолизины.
Эти ферменты экскретируются в неактивной форме. Последующий разрыв сульфгидрильной группы и присоединение атома металла (чаще всего цинка) приводят к изменению конформации фермента и переводят его в активное состояние. Тканевые ингибиторы металлопротеиназ (ТИМП) прекращают действие этих ферментов. Некоторые типы тканей изначально обладают повышенной устойчивостью к инвазии. Это, например, компактная костная ткань, ткани крупных сосудов и хрящевая ткань. Предположительно способность к инвазии у опухолевых клеток появляется в результате трансформации нормальных процессов реконструкции и восстановления здоровых тканей. Тем не менее к настоящему моменту неизвестно, какие конкретно изменения генетической структуры раковых клеток ответственны за инвазивный рост.
По мере роста опухоли она выделяет в кровь ангиогенные факторы, которые стимулируют прорастание опухоли кровеносными сосудами и формирование сети капилляров. Сосудистая система кровоснабжения опухоли может стать мишенью для различных видов противораковой терапии. Опухоль стимулирует пролиферацию эндотелиальных клеток, выделяя ангиогенные цитокины, такие как эндотелиальный фактор роста сосудов (ЭФРС), ТФР и факторы роста фибробластов. Эндотелиальные же клетки в свою очередь могут стимулировать рост клеток опухоли. В одном грамме опухолевой ткани может находиться до 10-20 млн эндотелиальных клеток, которые не являются неопластическими.
Антигены нормальных эндотелиальных клеток, включая и профакторы свертываемости крови, могут быть разрегулированы в активно пролиферирующей под действием опухоли эндотелиальной ткани. В дополнение к действию цитокинов, гипоксия, развивающаяся в сети опухолевого кровоснабжения, может стимулировать выбросы ЭФРС и других факторов. В ходе ангиогенеза эндотелиальные клетки внедряются в строму опухоли, активно делятся там с образованием зачатков новых капилляров, которые затем развиваются в сосудистую систему опухоли. Как и в случае инвазии опухолевых клеток, этот процесс идет с участием продуцируемых эндотелием ММП и их естественных ингибиторов.
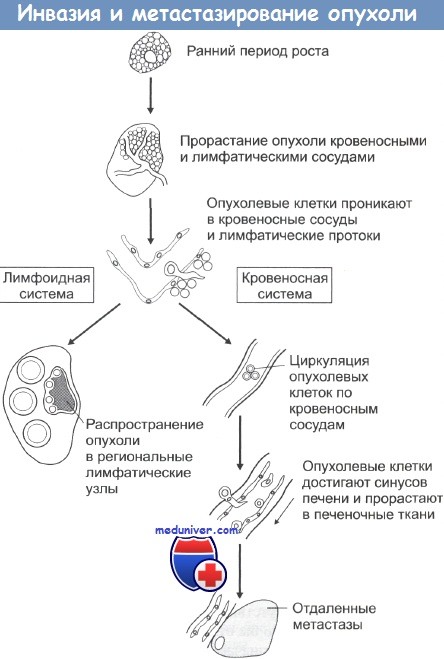
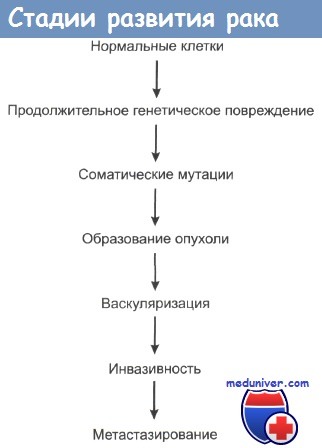
При локальной инвазии рака опухолевые клетки могут попадать в сосудистую систему и давать начало метастазам. Последовательность событий при метастазировании показана на рисунке. Распространение раковых клеток по лимфатической системе, что особенно характерно при карциномах, происходит при попадании опухолевых клеток в лимфатические протоки с последующим оседанием их в местах разветвления протоков и в ближайших лимфатических узлах. Вслед за этим обычно происходит инфильтрация опухолевыми клетками и отдаленных лимфоузлов. Распространение через кровяное русло проходит при проникновении раковых клеток в кровеносные сосуды рядом с местом первичной локализации опухоли либо через грудные протоки. Подхваченные током крови раковые клетки затем захватываются ближайшими капиллярными сетями, чаще всего сетями печени и легких, и оседают в них. При оценке направлений метастазирования очень важно учитывать первичную локализацию опухоли.
Например, опухоли пищеварительного тракта обычно метастазируют через воротную вену в печень. Опухоли также могут метастазировать непосредственно сквозь прилегающие ткани. Так возникающие в брюшной полости новообразования могут очень быстро рассеяться по всему внутрибрюшинному пространству, а клетки рака легкого могут мигрировать через плевру. Некоторые опухоли метастазируют в определенные органы и ткани, другие — бессистемно. Саркомы, например, почти всегда метастазируют в легкие, рак молочной железы поражает также ткани осевого скелета. Тем не менее биологических механизмов, объясняющих такую избирательность, пока не найдено.
Региональные лимфоузлы могут осуществлять барьерную функцию, предотвращая распространение метастазов за пределы области первичной локализации опухоли. До сих пор четко не выяснено, каким образом и за счет каких специфических иммунных механизмов лимфатические узлы создают барьер на пути распространения опухоли.
Проникая в кровеносное русло в районе первичной опухоли, раковые клетки затем могут достигать других органов и тканей. Для того чтобы дать начало новым очагам опухоли, эти клетки на новом месте должны, во-первых, проникнуть в ткани через эндотелий капилляров, а во-вторых, выжить при атаках местных иммунных систем защиты, таких как фагоцитирующие клетки и так называемые естественные киллеры (ЕК).
Способность к инвазированию и расселению в отдаленных органах и тканях у различных видов опухолей сильно варьирует. Эта способность, по-видимому, определяется степенью экспрессии того участка генома, который и обусловливает злокачественный рост клеток. Действительно, со временем почти все раковые опухоли накапливают все больше и больше генетических изменений в своих клетках и приобретают способности к инвазии и метастазированию. Но даже при клиническом обнаружении опухоли метастазы и инвазия могут проявиться лишь спустя несколько лет. Типичным примером является карцинома низкой степени злокачественности. Следует отметить, что даже однотипные виды рака с одинаковой степенью дифференцированности опухолевых клеток по-разному метастазируют у разных больных.
Все это говорит о необходимости поиска молекулярных маркеров, которые смогли бы предсказывать исход течения онкологического заболевания более точно, чем диагностика по гистологическому типу опухоли (хотя последний метод в настоящее время является наиболее точным из всех возможных). Кроме того, даже конкретная опухоль может быть в значительной степени гетерогенной и состоять из клеток, различных по своему метастатическому потенциалу, что было показано на клонированных субпопуляциях, выделенных из одной опухоли. Биологические причины такой вариабельности в настоящее время неизвестны.
Совершенно ясно, что для успешного лечения онкологических пациентов необходимо проводить масштабные исследования в области нахождения механизмов тканевой инвазии, метастатического роста и поиска биологических причин гетерогенности опухолей. Отсутствие гомогенности в опухолях, сходство опухолевых клеток со здоровыми клетками породившей ее ткани, и отсутствие четкого единичного критерия, по которому можно было бы отличить раковую клетку от здоровой, — все это вместе означает, что наши рассуждения о противоопухолевом иммунитете или о механизмах действия лекарственных цитостатических препаратов должны приниматься с изрядной долей скептицизма, особенно если они базируются на экспериментах с гомогенными опухолевыми культурами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Влияние экстратиреоидной инвазии на метастазирование при папиллярном раке щитовидной железы
Полный текст:
Аннотация
Обоснование. Течение и исход заболевания при папиллярном раке щитовидной железы (ПРЩЖ) во многом зависят от факторов прогноза. Одним из наиболее значимых факторов является наличие экcтратиреоидного распространения опухоли, которое может быть локальным и широким. Рост опухоли за пределы капсулы щитовидной железы (ЩЖ), по мнению ряда авторов, ассоциирован с повышенным риском регионарного и отдаленного метастазирования, приводя к увеличению частоты рецидивов и уменьшению выживаемости больных. По другим литературным данным, наличие микроскопической экстратиреоидной инвазии (ЭТИ) не влияет на прогноз заболевания. Таким образом, требуется проведение дополнительных исследований и уточнение значения ЭТИ при ПРЩЖ.
Цель: оценить роль экстратиреоидной инвазии в развитии процесса метастазирования у пациентов с папиллярным раком щитовидной железы.
Результаты. Прорастание капсулы ЩЖ выявлено у 111 (47,6%) больных: макроскопическая инвазия – у 19 (8,2%), микроскопическая – у 92 (39,5%). У 122 (52,4%) пациентов признаков ЭТИ не выявлено. Частота регионарных метастазов без и с ЭТИ составила 35,8 и 62,2% (что достоверно чаще ( р = 0,000, χ 2 = 21,342)) соответственно. При микроскопической и макроскопической инвазии частота лимфогенных метастазов составила 56,5 и 94,7%, а отдаленных – 1,1 и 21% соответственно. Наличие ЭТИ достоверно чаще встречалось при неинкапсулированных опухолях (р = 0,000, χ 2 = 15,122) и при увеличении размера первичной карциномы от 1 до 2 см и более ( р = 0,026, χ 2 = 7,293). У пациентов с клинической стадией N0 экстратиреоидное распространение зафиксировано в 41%, при N1 – в 72,9% случаев, что значимо чаще ( р = 0,000, χ 2 = 14,235).
Заключение. Экстратиреоидное распространение является предиктором развития метастазов. Наличие локальной ЭТИ диктует необходимость применения более агрессивных лечебных подходов у пациентов с ранними стадиями ПРЩЖ, включающих применение ТЭ в сочетании с ЦШЛД с последующей радиойодтерапией. Широкая ЭТИ существенно повышает риск как регионарных, так и отдаленных метастазов.
Ключевые слова
Для цитирования:
Солодкий В.А., Фомин Д.К., Галушко Д.А., Асмарян А.Г. Влияние экстратиреоидной инвазии на метастазирование при папиллярном раке щитовидной железы. Эндокринная хирургия. 2019;13(4):183-191. https://doi.org/10.14341/serg12236
For citation:
Solodkiy V.A., Fomin D.K., Galushko D.A., Asmaryan H.G. The influence of extrathyroidal extension in development of metastasis in papillary thyroid cancer. Endocrine Surgery. 2019;13(4):183-191. (In Russ.) https://doi.org/10.14341/serg12236
Обоснование
Папиллярный рак щитовидной железы (ПРЩЖ) – самый часто встречающийся морфологический тип злокачественных опухолей данного органа (около 90 и 75–92% по разным источникам) [1–3]. Это вариант опухоли с относительно хорошим прогнозом и низким уровнем смертности. Несмотря на это, ПРЩЖ чаще всего распространяется лимфогенным путем, что и обусловливает высокий процент локорегионарных рецидивов [4]. Множество клинико-морфологических и молекулярно-биологических факторов влияют на прогноз ПРЩЖ, некоторые из них являются факторами риска рецидива опухоли высокой, средней или низкой степени [5]. Одним из таких факторов является экстратиреоидная инвазия (ЭТИ). ЭТИ – это выход опухоли за пределы капсулы щитовидной железы (ЩЖ). Такое распространение может быть как минимальным – с поражением окружающей жировой клетчатки и передних мышц шеи, так и более широким – поражающим трахею, структуры гортани, возвратный гортанный нерв, глотку, пищевод и магистральные сосуды [6]. Классификация ЭТИ в основном направлена на определение степени инвазии. В литературе и в рекомендациях разных обществ встречаются такие типы, как микроскопическая (не определяемая визуально) и макроскопическая (определяемая визуально, видимая глазом); минимальная или локальная (инвазия жировой клетчатки и передних мышц) и обширная или широкая (инвазия возвратного нерва, трахеи, гортани, глотки, пищевода, магистральных сосудов, подкожной клетчатки и кожи) [7–10]. Впервые на неблагоприятный прогноз у пациентов c ПРЩЖ с локальной и широкой ЭТИ обратили внимание L.B. Woolner и соавт. в 1961 г. [11]. А в 1986 г. W.M. McConahey и соавт. сообщили, что у пациентов с ПРЩЖ, у которых была обнаружена макроскопическая ЭТИ, во время операции был повышен риск местного и регионарного рецидива и отдаленных метастазов [12]. В 1988 г. B. Cady и R. Rossi выделили группу риска ПРЩЖ и предложили систему АМЕS, включающую большую инвазию капсулы ЩЖ [13]. В последних рекомендациях Американской тиреоидологической ассоциации ЭТИ занимает среднюю позицию в структуре факторов риска рецидива [5]. Но нужно отметить, что в той же классификации ЭТИ с выявленной мутацией BRAF 600E является фактором риска рецидива высокой степени (10–40%) [5]. Некоторые авторы отмечают роль ЭТИ как предиктора лимфогенного метастазирования, однако пока не существует единого мнения о ее влиянии на безрецидивную и общую выживаемость [14–16]. Согласно последней (8-й) редакции TNM-классификации рака щитовидной железы, наличие минимальной ЭТИ не влияет на определение стадии заболевания, однако роль ЭТИ как прогностического фактора, предиктора регионарного распространения опухоли и как фактора, определяющего тактику лечения, остается дискутабельной, и только дальнейшие исследования могут прояснить данный вопрос.
Оценить влияние экстратиреоидной инвазии в развитии регионарных и отдаленных метастазов у пациентов с папиллярным раком щитовидной железы.
Методы
Дизайн исследования
Проведено одномоментное одноцентровое неконтролируемое исследование, планировалось провести детальный анализ группы пациентов с ДРЩЖ с клинической стадией сT1-4N0-1bM0-1, прошедших хирургическое лечение в ФГБУ “Российский научный центр рентгенорадиологии” Минздрава России.
Критерии соответствия
В исследование включены все пациенты независимо от пола и возраста, у которых по данным обследования (УЗИ щитовидной железы, шейных лимфатических узлов и органов брюшной полости, цитологическое исследование, КТ органов грудной клетки, остеосцинтиграфия) впервые выявлен папиллярный рак. В исследование не входили больные, которым по тяжести сопутствующих заболеваний проведение хирургического лечения противопоказано, и пациенты с другими морфологическими формами рака щитовидной железы (фолликулярным, медуллярным, низкодифференцированным, анапластическим).
Условия проведения
Исследование является моноцентровым. Оно проводилось в ФГБУ “Российский научный центр рентгенорадиологии” Минздрава России.
Продолжительность исследования
Продолжительность исследования – 7 лет, начало исследования в 2012 г.
Описание медицинского вмешательства
Больным ПРЩЖ c клиническими стадиями T1-3N0M0 проводилось хирургическое лечение в объеме стандартной тиреоидэктомии с профилактической двусторонней центральной шейной лимфодиссекцией (ЦШЛД). Границами лимфодиссекции являлись: сверху – подъязычная кость, латерально – медиальные края общих сонных артерий и брахиоцефального ствола справа, снизу – яремная вырезка, сзади – превертебральная фасция [18].
Основной исход исследования
В качестве основного исхода исследования выступала частота изменения клинического диагноза по данным послеоперационного морфологического исследования.
Анализ в подгруппах
В ходе статистической обработки результатов исследования для выявления значимости отдельных факторов в прогнозировании риска метастатического поражения лимфатических узлов участники были разделены на подгруппы по нескольким признакам: возраст (группа ≤45 лет и группа >45 лет), пол (мужской, женский), размер опухоли (группа ≤1 см и группа >1 см), мультифокальность (есть или нет), наличие фоновых заболеваний (есть или нет).
Методы регистрации исходов
Для регистрации основного исхода исследования использовалось патоморфологическое исследование послеоперационного материала. Выявление скрытых метастазов в лимфоузлах VI группы и выход опухоли за пределы капсулы щитовидной железы, приводящие к изменению клинической стадии заболевания.
Этическая экспертиза
Этическая экспертиза проводилась, протокол был одобрен на независимом этическом комитете ФГБУ “Российский научный центр рентгенорадиологии” Минздрава России (заседание №2 от 26.02.2012).
Статистический анализ
Принципы расчета размера выборки: размер выборки предварительно не рассчитывался. Методы статистического анализа данных: обработка информации осуществлялась в базе данных Microsoft Access, при помощи таблиц Microsoft Excel и программы Biostat (AnalystSoft Inc., Республика Беларусь). Для анализа количественных признаков использовался однофакторный дисперсионный анализ, а качественных – критерий χ-квадрат. Многофакторный анализ проведен в программе SPSS 20 (IBM Company, США). Переменные со значением p меньше чем 0,05 в одномерном анализе были включены в многофакторный логистический регрессионный анализ для определения отношения шансов.
Результаты
Объекты (участники) исследования
В РНЦРР с 2012 г. проведено хирургическое и комбинированное лечение 243 больным по поводу впервые выявленного ПРЩЖ. ЭТИ имела место в 111 случаях, отсутствие экстратиреоидного распространения – у 122 больных. У 10 пациентов было выявлено врастание опухоли в капсулу ЩЖ без явных признаков выхода в окружающие ткани, в связи с чем из дальнейшего анализа они были исключены. Таким образом, статистической обработке подвергнуты результаты обследования и лечения 233 пациентов. Во всех случаях ПРЩЖ был подтвержден при плановом гистологическом исследовании. Стадирование проводилось согласно классификации TNM (UCCI) 2017 г., 8-я редакция. Клиническая характеристика больных представлена в табл. 1.
Таблица 1. Клиническая характеристика пациентов с ПРЩЖ
Клинические характеристики
Количество больных, n (%)
Возраст:
Возраст:
Количество фокусов:
поражение обеих долей
Размер опухоли:
Наличие капсулы узла:
Вариант папиллярного рака:
Метастазы в лимфатические узлы:
Метастазы отдаленные:
Как видно из представленных данных, наличие экстратиреоидного распространения достоверно чаще встречалось при неинкапсулированных опухолях (р = 0,000, χ 2 = 15,122), при увеличении размера первичной карциномы (р = 0,026, χ 2 = 7,293) и было четко ассоциировано с наличием регионарных метастазов (р = 0,000, χ 2 = 21,342). Размер первичной опухоли у пациентов с ЭТИ был значимо больше, чем в группе без экстратиреоидного распространения (1,6 ± 1,1 см против 1,2 ± 0,6 см, р = 0,000). Все пациенты с отдаленными метастазами имели ЭТИ и регионарные метастазы. Прорастание капсулы ЩЖ не зависело от пола, возраста пациентов, количества фокусов опухоли и не отличалось при типичном или фолликулярном варианте папиллярного рака. Однако у мужчин ЭТИ встречалась существенно чаще, чем у женщин, и отсутствие различий связано, вероятно, с малочисленностью мужской группы. Среди пациентов без ЭТИ лимфогенные метастазы выявлены в 35,8%, при наличии ЭТИ – в 62,2% случаев. Следует отметить, что в группе микроскопического экстратиреоидного распространения (n = 92) поражение регионарных лимфатических узлов имело место у 52 (56,5%), органные метастазы – у 1 (1,1%) больного. Среди 19 пациентов с макроскопической ЭТИ лимфогенные метастазы выявлены в 18 (94,7%) и отдаленные – в 4 (21%) случаях. Таким образом, прослеживается довольно четкая тенденция в виде увеличения частоты регионарного и отдаленного метастазирования в зависимости от степени вовлечения анатомической капсулы ЩЖ. Фоновые заболевания, в частности наиболее часто присутствующий хронический аутоиммунный тиреоидит, встречались одинаково часто в группах с и без ЭТИ.
Как было показано выше, среди 233 пациентов клиническая стадия N0 имелась в 185 и N1 – в 48 случаях. После профилактической ЦШЛД при гистологическом исследовании метастазы в VI группе лимфатических узлов выявлены у 61 (33%) больного, ЭТИ в этой группе зафиксирована в 76 (41%) случаях. При наличии прорастания капсулы ЩЖ скрытые метастазы в центральных лимфатических узлах выявлены у 35 (46,1%) больных, при отсутствии экстратиреоидного распространения – у 26 (23,9%), что достоверно чаще (р = 0,003, χ 2 = 9,006). При многофакторном анализе прорастание капсулы ЩЖ явилось наиболее значимым фактором, отвечающим за развитие скрытых метастазов в центральной зоне (р = 0,001, ОШ 3,422, 95% ДИ 1,665–7,031). В группе пациентов с клинически определяемыми метастазами (n = 48) экстратиреоидное распространение опухоли выявлено в 35 (72,9%) случаях, что достоверно чаще, чем в группе с клинической стадией N0 (р = 0,000, χ 2 = 14,235).
Дополнительные результаты исследования
Интересен факт, что среди 10 пациентов, не вошедших в исследование, с врастанием опухоли в анатомическую капсулу ЩЖ, но без выхода за ее пределы, регионарные метастазы выявлялись существенно чаще, чем в группе без ЭТИ (60% против 35,8%). Однако малочисленность данной группы пока не позволяет судить о значении данного факта. Следует отметить, что интерпретация интраоперационной макроскопической картины достаточно субъективна, так, из 26 пациентов с визуальным прорастанием капсулы ЩЖ у 7 (26,9%) наличие ЭТИ при гистологическом исследовании не подтвердилось. При анализе первичных гистологических заключений группы из 106 пациентов, оперированных в РНЦРР повторно, по поводу регионарного рецидива, частота ЭТИ составила 64,2%, что дополнительно свидетельствует о значительном влиянии экстратиреоидного распространения в развитии метастазов при ПРЩЖ.
Нежелательные явления
Нежелательные явления не наблюдались.
Обсуждение
Резюме основного результата исследования
Таким образом, неинкапсулированный вариант карциномы, размер опухоли 1 см и более достоверно повышают частоту ЭТИ и ассоциируются с высоким риском в первую очередь регионарного метастазирования. Учитывая высокую вероятность лимфогенных метастазов, при наличии или подозрении на ЭТИ оправданы более агрессивные подходы к лечению, а именно выполнение ТЭ и ЦШЛД и проведение радиойодтерапии.
Обсуждение основного результата исследования
Вопросы хирургического лечения ранних стадий ПРЩЖ остаются дискутабельными. На протяжении многих лет, согласно рекомендациям многочисленных организаций (NCCN, Американская тиреоидологическая ассоциация (АТА), Европейский консенсус 2006 г.), ТЭ являлась основным объемом хирургического вмешательства при ПРЩЖ, особенно при размере карциномы более 1 см. В системе ТNM (UCCI) 2003, 2010 гг. (6-я и 7-я редакции) любая опухоль с минимальным выходом за пределы капсулы ЩЖ трактовалась как Т3 и у пациентов старше 45 лет соответствовала III стадии заболевания. Наличие ЭТИ в рекомендациях АТА 2009 г. требовало выполнения ТЭ и ЦШЛД. В 8-м издании системы ТNM (UCCI) 2017 г. значение ЭТИ существенно пересмотрено, наличие локального экстратиреоидного распространения не влияет на категорию Т и она кодируется исходя из размера опухоли. Только широкая инвазия передних мышц шеи обозначается как Т3, однако критерии глубины их поражения отсутствуют. Причиной изменений классификации явились высокие цифры выживаемости при наличии локальной ЭТИ, которые практически не отличались от Т1-2. Впоследствии рекомендации были пересмотрены, и в последних из них (NCCN с 2017 г., АТА 2015 г.) при опухолях, ограниченных ЩЖ, отсутствии регионарных и отдаленных метастазов, а также других факторов неблагоприятного прогноза допускается выполнение гемитиреоидэктомии. К сожалению, не все факторы прогноза можно учесть до операции. Часть из них, такие как неблагоприятный вариант карциномы, наличие ЭТИ, ангиолимфатической инвазии, скрытых метастазов в лимфатических узлах, выявляются только при плановом гистологическом исследовании, что может служить причиной тактических ошибок при выборе первичного объема хирургического лечения и последующих рецидивов. В большинстве случаев наличие локальной ЭТИ является находкой морфологов. Так, согласно нашим данным, у больных с размером опухоли ≤1 см, что соответствует микрокарциноме, прорастание капсулы ЩЖ выявляется в 38,5% случаев, доля регионарного метастазирования составляет 36,5%, причем частота скрытых метастазов, не обнаруженных на этапе предоперационной диагностики при УЗИ и КТ, достигает 25%. При увеличении степени экстратиреоидного распространения от микроскопической к макроскопической частота регионарных метастазов растет, а при широкой инвазии выявляются отдаленные метастазы.
Ограничения исследования
Из-за небольшой выборки группы мужчин и агрессивных форм папиллярного рака щитовидной железы не представляется возможным статистически достоверно оценить значимость данных факторов.
Заключение
Таким образом, учитывая высокую вероятность лимфогенных метастазов при наличии ЭТИ (даже при отсутствии клинико-инструментальных данных о поражении лимфатических узлов) оправдан более агрессивный подход к лечению, а именно выполнение тиреоидэктомии и профилактической центральной лимфодиссекции. В клинической практике следует максимально скрупулезно оценивать взаимоотношение опухоли и анатомической капсулы ЩЖ и, при выявлении или подозрении на экстратиреоидное распространение опухоли, проводить соответствующее радикальное лечение.
Дополнительная информация
Источник финансирования. Исследование выполнено при финансовом обеспечении ФГБУ “Российский научный центр рентгенорадиологии” Минздрава России.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.