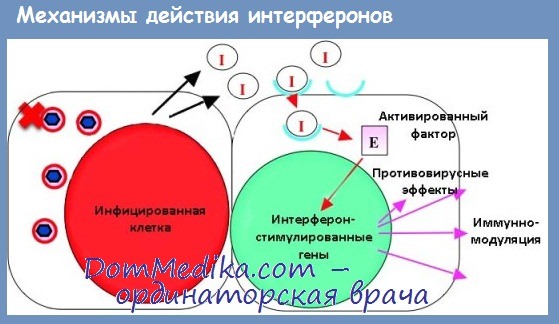
Антипрофилеративный что это значит
Антипрофилеративный что это значит
Некоторые функции лежат в основе антипролиферативного действия интерферонов. Большинство из составляющих противоинфекционной активности интерферонов играет ту или иную роль и в их противоопухолевом эффекте.
Упоминавшееся увеличение синтеза Мх-протеинов, являющихся ингибиторами транскрипции иРНК, ферментов системы 2′-5′-олигоаденилатсинтетазы, ингибирующих трансляцию, необходимую для синтеза клеточных белков, истощение внутриклеточных запасов триптофана, ведущее к нарушению белкового синтеза в клетке, имеют большое значение в антипролиферативном, в том числе противоопухолевом, действии интерферонов.
Значение изменения уровня 2’— 5′-синтетазы в антипролиферативном действии ИФН-а подтверждено клиническими наблюдениями: показана корреляция степени повышения уровня фермента с эффективностью терапии у больных с карциноидом кишечника и лимфомами.
Не менее значимым в антипролиферативном действии интерферонов является и другой механизм. Сигнал, передающийся ядру клетки в результате связывания интерферона с интерфероновым рецептором, уменьшает экспрессию протоонкогенов, в частности с-тус и c-fos, участвующих в регуляции клеточного роста.
Подавление активности этих протоонкогенов ведет к блокаде клеточного цикла, накоплению клеток в фазе G0, в результате чего пролиферация резко замедляется или даже прекращается, так как большинство клеток подвергаются апоптозу. Этот процесс обратим, и спустя некоторое время после удаления интерферона клеточная пролиферация может восстановиться в прежнем темпе, при этом экспрессия онкогенов, подавленная в присутствии интерферона, после его удаления из организма также может восстановиться на прежнем уровне.
Точно так же действие интерферонов в большинстве случаев не вызывает необратимых процессов в клетках, генотип которых изменен под влиянием интеграции генома вируса в ДНК клетки. Длительное применение интерферона в этих случаях может восстановить нормальный фенотип клеток, но прекращение действия интерферона вновь приводит к развитию опухоли.
Важным в антипролиферативном, в частности противоопухолевом, действии интерферонов является ингибирование ангиогенеза — роста и новообразования сосудов, играющее важную роль в росте и метастазировании опухоли. Многочисленные исследования, посвященные изучению механизма лечебного действия ИФН-а при гемангиоматозе, показали, что интерфероны ингибируют пролиферацию эндотелиальных клеток и клеток гладких мышц, подавляют фактор роста фибробластов и ангиогенина (фактор роста и новообразования сосудов), уменьшают продукцию коллагена.
Показано, что ИЛ-12, обладающий выраженным антиангиогенным эффектом, усиливает образование ИФН-у и его эффекторного белка р10.
На клеточных культурах здоровых доноров и больных острым лейкозом продемонстрировано, что ИФН-а значительно подавляет активность теломеразы — фермента, регулирующего длину теломер, необходимую для клеточного деления. Имеются неоднократно подтвержденные данные о том, что ИФН-у увеличивает экспрессию FAS-антигена и каспазы 3 и тем самым индуцирует апоптоз в костно-мозговых (CD34+) предшественниках.
Получены данные о том, что аналогичным образом действует и ИФН-а, причем эффект апоптотического действия его усиливается вызываемой им фрагментацией антиапоптотической молекулы Вах. ИФН-а усиливает также выброс в кровь фактора некроза опухоли, действие которого направлено на деградацию опухолевых клеток.
Таким образом, из имеющихся к настоящему времени данных очевидно, что интерфероны оказывают антипролиферативное, в том числе противоопухолевое, действие, реализуемое несколькими, нередко взаимосвязанными путями. В противоопухолевом действии интерферонов имеют значение как изложенные способы непосредственного воздействия на опухоль, так и непрямые противоопухолевые механизмы, связанные с увеличением активности макрофагов, активацией Т-клеток, натуральных киллеров и увеличением продукции антител.
АНТИПРОЛИФЕРАТИВНЫЕ СРЕДСТВА
АНТИПРОЛИФЕРАТИВНЫЕ СРЕДСТВА
Цитостатики и иммунодепресанты (представлены в таблице в разделе «Лимфопролиферативные болезни») своим основным показанием к применению имеют пролиферативные, в том числе опухолевые, заболевания кожи (лимфомы и другие гемобластозы, псориаз), а также дерматозы, связанные с патологией иммунной системы (ангииты, красная волчанка и др.).
Читайте также
ЛЕКЦИЯ № 11. Лекарственные средства, действующие на периферические нейромедиаторные системы. Средства, действующие на периферические холинергические процессы
ЛЕКЦИЯ № 11. Лекарственные средства, действующие на периферические нейромедиаторные системы. Средства, действующие на периферические холинергические процессы 1. Лекарственные средства, действующие преимущественно на периферические нейромедиаторные системы В
ЛЕКЦИЯ № 15. Средства, действующие в области чувствительных нервных окончаний. Средства, понижающие чувствительность нервных окончаний
ЛЕКЦИЯ № 15. Средства, действующие в области чувствительных нервных окончаний. Средства, понижающие чувствительность нервных окончаний 1. Местноанестезирующие средства Препараты этой группы избирательно блокируют процесс передачи возбуждения в эфферентных нервах и
4. Обволакивающие средства и адсорбирующие средства
4. Обволакивающие средства и адсорбирующие средства Обволакивающие средства.Обволакивающие средства образуют в воде коллоидные растворы – слизи, покрывающие слизистые оболочки и защищающие их от действия раздражающих веществ.Используют их для лечения воспалительных
2. Средства, содержащие эфирные масла. Горечи. Средства, содержащие аммиак
2. Средства, содержащие эфирные масла. Горечи. Средства, содержащие аммиак Средства, содержащие эфирные масла.Лист эвкалипта (Folium Eucalypti).Применение: отвар и настой эвкалипта как антисептическое средство для полосканий и ингаляций при лор-заболеваниях, а также для лечения
47. Обволакивающие средства и адсорбирующие средства
47. Обволакивающие средства и адсорбирующие средства Обволакивающие средства.Обволакивающие средства образуют в воде коллоидные растворы – слизи, покрывающие слизистые оболочки и защищающие их от действия раздражающих веществ.Используют их для лечения
48. Средства, содержащие эфирные масла. Горечи. Средства, содержащие аммиак
48. Средства, содержащие эфирные масла. Горечи. Средства, содержащие аммиак Средства, содержащие эфирные масла.Лист эвкалипта (Folium Eucalypti).Применение: отвар и настой эвкалипта как антисептическое средство для полосканий и ингаляций при лор-заболеваниях, а также для лечения
X. Средства домашняго обихода X. Средства домашняго обихода ( подспорныя ).
X. Средства домашняго обихода X. Средства домашняго обихода ( подспорныя ). Блюдечко. Въ немъ приготовляютъ л?карства.Бутылки. Въ нихъ приготовляютъ и сохраняютъ н?которые „составы“ и др. л?карства.Вода обыкновенная употребляется для приготовленія отваровъ, наваровъ,
ЖАРОПОНИЖАЮЩИЕ СРЕДСТВА
ЖАРОПОНИЖАЮЩИЕ СРЕДСТВА У здорового ребенка в норме температура тела в течение суток может колебаться от 36 до 37°С. Максимальная температура тела наблюдается между 17 и 20 часами, минимальная – от 4 до 7 часов.Повышенная температура тела (до определенного предела) является
ПРОТИВОВИРУСНЫЕ СРЕДСТВА
ПРОТИВОВИРУСНЫЕ СРЕДСТВА Специфическим противовирусным средством является ремантадин – препарат обладает противовирусным действием в отношении вирусов гриппа А, В. Он защищает клетки организма от проникновения в них вируса гриппа. На вирус, уже проникший в клетки,
СРЕДСТВА ОТ НАСМОРКА
СРЕДСТВА ОТ НАСМОРКА В начале заболевания при наличии насморка с обильными выделениями из носа («течет» из носа) целесообразно закапывать в нос сосудосуживающие капли: отривин, назолин, галазолин, нафтизин – по 2 – 3 капли в каждую ноздрю 3 – 4 раза в день детям старшего
СРЕДСТВА ОТ КАШЛЯ
СРЕДСТВА ОТ КАШЛЯ При кашле для разжижения и лучшего отхождения мокроты применяются следующие отхаркивающие средства.• Грудной эликсир. Препараты принимают внутрь; детям до 1 года назначают по 1 – 2 капли 2 – 3 раза в день, детям старше года – количество капель на прием,
Общеукрепляющие средства. Средства, регулирующие обмен веществ
Общеукрепляющие средства. Средства, регулирующие обмен веществ — Взять по щепотке цветков терна и соцветий одуванчика, залить 1 стаканом кипятка, дать настояться, процедить, добавить 1 ст. ложку яблочного уксуса. Выпить теплым перед сном.— Для общеукрепляющей ванны
Средства для рук
Средства для рук • Для потрескавшейся кожиОтварить 5 картофелин, растереть в кашицу, добавить 5 ст. л. молока. Кашицу теплой нанести на кожу и держать 10 минут, сделать энергичный массаж. Вымыть руки холодной водой и нанести крем. Можно в эту кашицу просто погрузить руки до
Антипролиферативные средства – Список лекарств и медицинских препаратов
Описание фармакологического действия
Антипролиферативное действие направлено на подавление избыточной пролиферации различных клеток. Механизм действия различен и зависит от конкретного препарата и типа клеток, на которые это действие направлено. В частности, механизм данного действия может быть связан с оказанием модулирующего влияния на синтез некоторых онкогенов, приводящее к нормализации неопластической трансформации клеток и ингибированию опухолевого роста. Или механизм действия может быть основан на угнетении пролиферации фибробластов, стимулированной основным фактором роста фибробластов. Препараты, обладающие антипролиферативным действием, применяются в лечении и профилактике различных онкологических заболеваний, при аденоме простаты, различных хронических заболеваниях кожи (например, псориаз).
Поиск препарата
Препараты c фармакологическим действием «Антипролиферативное»
Внимание! Информация, представленная в данном справочнике лекарств, предназначена для медицинских специалистов и не должна являться основанием для самолечения. Описания препаратов приведены для ознакомления и не предназначены для назначения лечения без участия врача. Есть противопоказания. Пациентам необходима консультация специалиста!
Если Вас интересуют еще какие-нибудь Антипролиферативные средства и препараты, их описания и инструкции по применению, синонимы и аналоги, информация о составе и форме выпуска, показания к применению и побочные эффекты, способы применения, дозировки и противопоказания, примечания о лечении лекарством детей, новорожденных и беременных, цена и отзывы о медикаментах или же у Вас есть какие-либо другие вопросы и предложения – напишите нам, мы обязательно постараемся Вам помочь.
Вход в личный кабинет
Интерфероны: иммунорегуляторная роль, противовирусное и антипролиферативное действие
| |
А.Н. Моисеев, канд. вет. наук, ООО «БИОТЕХ-ФАРМ», г. Санкт-Петербург
П.И. Барышников, д-р вет. наук, профессор, Алтайский АГАУ, г. Барнаул
В семейство цитокинов входят интерфероны (далее — IFN), интерлейкины, хемокины, ростовые и колониестимулирующие факторы, представляющие собой сигнальные полипептидные молекулы иммунной системы. Обладая широким спектром биологической активности, они определяют не только адекватный уровень иммунного ответа, но и регулируют взаимодействия главных интегративных систем организма — нервной, иммунной и эндокринной.
Структура и механизм действия большинства цитокинов охарактеризованы достаточно полно. Благодаря использованию методов генной инженерии и современной биотехнологии многие цитокины в настоящее время производятся в виде рекомбинантных препаратов, идентичных эндогенным молекулам, в количестве достаточном для их клинического применения.
Многие микроорганизмы — бактерии, дрожжи, вирусы — используются в качестве реципиентов чужеродного генетического материала с целью получения рекомбинантных штаммов — продуцентов биотехнологической продукции. Так получены рекомбинантные штаммы Е. coli, продуцирующие интерфероны, инсулин, гормоны роста, разнообразные антигены; штаммы В. subtilis, вырабатывающие интерферон; дрожжи, продуцирующие интерлейкины и др.
Использование рекомбинантных цитокинов, обеспечивающих адекватную и целенаправленную медикаментозную коррекцию иммунных дисфункций, повышает эффективность иммунотерапии и лечения в целом. Вводимые в организм цитокины восполняют дефицит эндогенных регуляторных молекул и полностью воспроизводят их эффекты. Это особенно важно в условиях тяжелой или хронической патологии, когда применение традиционных иммуномодуляторов или индукторов синтеза цитокинов бесполезно из-за истощения компенсаторных возможностей иммунной системы. В настоящее время терапия рекомбинантными цитокинами является одним из наиболее перспективных и постоянно расширяющихся направлений иммунофармакологии.
Так, противовирусное и антипролиферативное действие оказывают интерфероны первого типа (далее — IFN-α, IFN-β). Особое место в свете современных представлений о молекулярных механизмах иммунных реакций принадлежит интерферону гамма (далее — IFN-γ) — регуляторному цитокину иммунного ответа.
На основе рекомбинантных интерферонов различными компаниями разработаны лекарственные препараты для животных и человека, которые применяются для лечения и профилактики инфекционных заболеваний, в первую очередь вирусной этиологии.
Рекомбинантные IFN в организме животных и человека при терапии и профилактике заболеваний различной этиологии обеспечивают адекватную и целенаправленную медикаментозную коррекцию иммунных дисфункций, восполняя дефицит эндогенных регуляторных молекул и полностью воспроизводят их эффекты. Высокая иммунокорригирующая эффективность, прогнозируемость и селективность их действия обусловлены наличием на клетках специфических рецепторов и существованием природных механизмов их элиминации. Лекарственные препараты на основе рекомбинантных IFN являются мощными средствами патогенетической иммуноориентированной терапии и обладают как прямым замещающим действием, так и оказывают различные индуктивные эффекты. В настоящее время они находят широкое применение в лечении инфекционных, онкологических и некоторых других заболеваний животных.
Классификация интерферонов
Интерфероны (IFN, ИФН) — общее название, под которым в настоящее время объединяют ряд биологически активных белков или гликопротеидов со сходными свойствами, синтезируемых клетками организма в процессе защитной реакции в ответ на вторжение чужеродных агентов — вирусную инфекцию или антигенное воздействие. Благодаря интерферонам клетки становятся невосприимчивыми по отношению к вирусу.
Интерфероны — мультигенное семейство индуцибельных цитокинов, обладающих разнообразными функциями, включая противовирусную, антипролиферативную, противоопухолевую и иммуномодулирующую.
В настоящее время известно более 20 IFN, различающихся по структуре, биологическим свойствам и преобладающему механизму действия. IFN подразделяют на три типа:
• Тип II, известный как иммунный, включает IFN-γ (синтезируется активированными Т-лимфоцитами и NK-клетками). Главное действие интерферонов второго типа (IFN-γ) — участие в реакциях иммунитета. Он начинает вырабатываться на последующих этапах инфекционного процесса уже сенсибилизированными Т-лимфоцитами и активно участвует в каскаде специфического иммунного ответа. Индуцировать выработку IFN-γ способны интерфероногенные вещества, антигены, Т-митогены и некоторые цитокины. Клетками-мишенями для действия IFN-γ являются макрофаги, нейтрофилы, естественные киллерные клетки, цитотоксические Т-лимфоциты, имеющие на своей поверхности рецепторы к IFN-γ Продукция IFN-γ находится под контролем цитокинов. IL-12 и IL-18 усиливают его экспрессию, а IL-2 способствует реализации функции CD4+ лимфоцитов, активируя выработку IFN-γ. Фоновое количество IFN-γ всегда есть в организме, даже если нет инфекции: например, анализ на интерфероновый статус показывает у здоровых людей и животных всегда определяемое количество IFN в крови, при стимуляции или инфекции оно многократно возрастает. Однако при герпесвирусной инфекции и на последних стадиях опухолевого процесса количество IFN-γ стремится к нулю, так как вирус герпеса и раковые клетки продуцируют белки, блокирующие синтез IFN-γ. Поэтому при герпесвирусной инфекции и раке индукторы интерферонов бессмысленны, их нужно вводить в организм извне.
• Тип III был обнаружен позже типа I и типа II; информация о нем свидетельствует о важности IFN типа III в некоторых видах вирусных инфекций.
Вирусные интерфероны (IFN-α/β) индуцируются в процессе вирусной инфекции, а синтез интерферонов II типа (IFN-γ) индуцируется митогенными или антигенными стимулами. Большинство типов вирусоинфицированных клеток способно синтезировать IFN-α/β в клеточной культуре. В противоположность этому IFN-γ синтезируется только некоторыми клетками иммунной системы, включая естественные киллерные (NK) клетки, CD4 Т-клетки и CDS цитотоксические супрессорные клетки.
Противовирусный эффект интерферонов
Интерфероны не действуют непосредственно на вирус. Под их влиянием клетка становится резистентной к инфекции. Интерфероны являются первой линией защиты от вирусной инфекции, поскольку начинают вырабатываться сразу же после контакта с вирусом. При этом выраженность ответа прямо пропорциональна заражающей дозе.
Некоторые вирусы способны блокировать противовирусное действие IFN. Так, например, аденовирусы продуцируют специфическую РНК, которая предотвращает активацию протеинкиназы.
Cвязывание IFN с рецептором индуцирует в клетке три одновременно протекающих процесса, которые заканчиваются:
• активацией латентной эндорибонуклеазы, приводящей к разрушению вирусной РНК;
• подавлением синтеза вирусной матричной РНК;
• подавлением синтеза белков вирусной оболочки.
Эти механизмы интегрально реализуют противовирусный эффект, приводя к подавлению репликации вируса.
Иммуномодулирующее действие интерферонов
IFN обладают не только противовирусным, но и иммуномодулирующим действием за счет влияния на экспрессию рецепторов главного комплекса гистосовместимости (МНС). IFN увеличивают экспрессию молекул 1-го класса МНС на всех видах клеток, тем самым улучшая распознавание инфицированных клеток цитотоксическими Т-лимфоцитами (CTL). Кроме того, IFN-γ усиливает экспрессию молекул 2-го класса МНС на антигенпрезентирующих клетках, в результате чего улучшается презентация вирусных антигенов CD4+ лимфоцитам и активируются натуральные киллеры (NK-клетки). IFN также стимулируют фагоцитоз.
Регуляция иммунного ответа цитокинами, в том числе интерферонами, происходит по эстафетному принципу, воздействие цитокина на клетку вызывает образование ею других цитокинов (цитокиновый каскад).
Антипролиферативный эффект интерферонов
Антипролиферативный эффект IFN объясняется следующими механизмами:
• активацией цитотоксических клеток;
• усилением экспрессии опухольассоциированных антигенов;
• модуляцией продукции антител;
• ингибицией действия опухолевых ростовых факторов;
• ингибицией синтеза РНК и белков опухолевой клетки;
• замедлением клеточного цикла с переходом в фазу покоя;
• стимуляцией опухолевых клеток к созреванию;
• восстановлением сдерживающего контроля за пролиферацией;
• торможением образования новых сосудов в опухоли;
• биомодуляцией активности цитостатиков: изменением метаболизма и снижением клиренса;
• преодолением лекарственной резистентности за счет ингибиции генов множественной лекарственной резистентности.
Антибактериальный эффект интерферонов
В последние годы показано, что IFN обладают также антибактериальным эффектом, в основе которого лежит способность IFN индуцировать активность некоторых ферментов в пораженной клетке.
Кроме того, антибактериальная роль IFN-γ заключается в активации макрофагов, которые продуцируют провоспалительные цитокины, а также активные формы кислорода и азота, простагландины. Эти факторы способствуют развитию воспалительного процесса, ведущего к гибели бактерий.
Таким образом, все интерфероны представляют собой группу полифункциональных белковых факторов с выраженным противовирусным и противоопухолевым эффектом разной степени. IFN-α обладает самой сильной противовирусной активностью среди всех интерферонов, а IFN-γ имеет более выраженную антипролиферативную активность. Все интерфероны обладают иммунорегуляторным действием разной степени выраженности (максимальной обладает IFN-γ) — повышают активность макрофагов, Т-лимфоцитов и NK-клеток.
Антипролиферативное средство
Владельцы патента RU 2637647:
Изобретение относится к фармацевтической промышленности, в частности к средству природного происхождения, обладающему антипролиферативной активностью. Средство, обладающее антипролиферативной активностью, представляющее собой белковый экстракт Toxocara canis, полученный путем экстрагирования гомогентата гельминтов Т. Canis фосфатно-солевым буферным раствором с рН 7,2 в соотношении 1:10 в течение 36-48 ч при температуре 4°С, центрифугирования. Вышеописанное средство обладает выраженной антипролиферативной активностью. 1 з.п. ф-лы, 1 табл.,2 пр.
Изобретение относится к области медицины и ветеринарии, в частности к новому средству природного происхождения, оказывающему антипролиферативное действие.
Современная медицина располагает достаточно обширным арсеналом лекарственных препаратов для химиотерапии опухолей. В основном химиотерапевтические средства представлены группами алкилирующих антинеопластических препаратов, антиметаболитов, противоопухолевых антибиотиков, противоопухолевых гормональных препаратов, иммуномодуляторов и некоторых других с иным механизмом действия. Большинство указанных противоопухолевых препаратов очень токсичны, и поэтому схемы и продолжительность химиотерапии выбирают с учетом проявления побочных эффектов, что отражается на эффективности лечения в целом.
Известны природные противоопухолевые препараты растительного происхождения (алкалоиды барвинка розового (винбластин, винкристин); алкалоиды тисового дерева (таксаны) (паклитаксел, доцетаксел); подофиллотоксины, выделяемые из подофилла щитовидного (этопозид, тенипозид) и алкалоиды безвременника великолепного (демекольцин (колхамин), колхицин)) и бактериального происхождения (рубромицин и др.), которые имеют ограниченное применение также из-за высокой токсичности и узкого терапевтического спектра действия (лечение некоторых разновидностей опухолей, преимущественно с экзофитным ростом).
Следовательно, существует необходимость в новых, высокоэффективных противоопухолевых препаратах природного происхождения, которые имели бы широкий спектр действия и были бы менее токсичными.
К гельминтам относят представителей ленточных червей, или цестод, сосальщиков, или трематод (обе эти группы относятся к плоским червям) и круглых червей, или нематод.
К числу последних относятся токсокары (в частности, Toxocara canis). Т. canis представляет нематоду, паразитирующую в кишечнике плотоядных, например собак; вызывающую инвазию, известную как токсокароз.
Во время паразитирования гельминты продуцируют и высвобождают различные продукты метаболизма. Секреторно-экскреторные продукты жизнедеятельности гельминтов являются для организма хозяина неестественными веществами в его физиологически процессах.
Известно, что возбудители инвазий могут оказывать модулирующее влияние на течение многих заболеваний самой различной этиологии, в том числе, злокачественных (например, Vasilev S. et al. (2015). В частности, имеются сообщения о том, что заражение мышей нематодой Trichinella spiralis (воспроизведение трихинеллеза) приводит к подавлению роста злокачественных клеток и повышению выживаемости животных после прививки клеток меланомы В-16 в условиях in vivo (Molinari J.A., Ebersole J.L., 1977; Pocock D., Meerovitch E., 1982; Kang Y.L. et al., 2013). Также имеются данные по испытанию продуктов метаболизма Т. spiralis с ингибирующим эффектом в отношении роста и выживаемости опухолевых клеток в условиях in vitro (Vasilev S. et al., 2015; Wang X.L. et al., 2009; Wang X.L. et al., 2013).
Исследования по оценке противоопухолевой активности Т. canis или продуктов метаболизма этих гельминтов ранее не проводились.
Целью изобретения является получение белковых экстрактов из тканей Т. canis, оценка их антипролиферативного действия на моделях опухолевых клеток различных линий и обеспечение их возможного применения в дальнейшем в качестве эффективного противоопухолевого средства.
Сущность изобретения заключается в том, что средство, обладающее антипролиферативной активностью, представляет белковый экстракт гельминтов, в частности экстракт Toxocara canis. Необходимо отметить, что условия получения экстракта из гомогената гельминтов, в том числе, Т. canis, зависят от используемого биологического материала, и существенными признаками получения белковых экстрактов является экстракция фосфатно-солевым буфером с рН=7,2.
Экстракт оказывает выраженное антипролиферативное и цитостатическое действие на моделях опухолевых клеток человека in vitro. Как уже указывалось выше, экстракт токсокар ранее не испытывался на моделях опухолевых клеток человека in vitro.
За счет природного происхождения предлагаемое антипролиферативное средство может быть менее токсичным при наличии высокой противоопухолевой эффективности широкого спектра действия.
Примеры конкретного исполнения
Пример 1. Приготовление белкового экстракта Т. canis.
В качестве средства, предположительно обладающего антипролиферативной активностью, использовали белковый экстракт из половозрелых Т. canis, предварительно очищенный от низкомолекулярных соединений.
Пример 2. Оценка влияния белкового экстракта Т. canis на культуры опухолевых клеток молочной железы человека (MCF-7) и ободочной кишки человека (Сасо-2) в зависимости от концентрации экстракта.
Целью настоящего опыта была оценка влияния белкового экстракта Т. canis на пролиферацию опухолевых клеток человека двух линий.
Материалы и методы
Перед работой пробирку с белковым экстрактом размораживали при комнатной температуре. В эксперименте in vitro белковый экстракт испытывали в следующих концентрациях по белку: 12,5, 25, 50, 100, 250, 500, 1 и 2 мг/мл. Для приготовления разведений использовали ростовую среду DMEM GlutaMAX (DGIBCO) с 2% FBS и антибиотиком.
Перед проведением опыта готовили рабочий раствор с концентрацией 2 мг/мл, после его стерилизации через миллипоровый фильт-насадку (0,22 μ) были приготовлены разведения экстракта Т. canis: 1, 500, 250, 100, 50, 25 и 12,5 мкг/мл с использованием ростовой среды DMEM GlutaMAX (DGIBCO) с 2% FBS и антибиотиком.
Для проведения эксперимента клетки MCF-7 и Сасо-2 инкубировали по стандартной методике до получения субконфлуэнтного монослоя. В стадии активного роста клеточный монослой диспергировали раствором трипсин/версена, полученные клетки ресуспендировали в ростовой среде DMEM GlutaMAX (Gibco) с 10% FBS и антибиотиком стандартной концентрации. Свежеприготовленную суспензию клеток высевали в 24-луночные планшеты (SARSTEDT, Германия) по 35×10 3 клеток в лунку для клеток MCF-7 и по 30×10 3 клеток в лунку для клеток Сасо-2. После чего планшеты ставили в СО2-инкубатор на 3 ч до полного распластывания клеток. Затем из лунок удаляли среду с не прикрепившимися клетками и в опытные лунки вносили ростовую среду с исследуемыми концентрациями вещества (в 4 повторах на каждую исследуемую концентрацию). В качестве контроля оставили четыре лунки с клетками, которые культивировали в полной ростовой среде с 2% FBS без исследуемого вещества. Конечный объем ростовой среды в контрольных и опытных группах по 500 мкл на лунку.
В ходе эксперимента проводили ежедневное светооптическое наблюдение за клетками с использованием инвертированного микроскопа Olympus CK 40 (Japan), оценивая наличие или отсутствие изменений морфологии клеток в опытных лунках по сравнению с контролем. Пролиферативный ответ опухолевых клеток на действие исследуемого экстракта Т. canis оценивали по плотности и жизнеспособности сформированного монослоя после 96-часовой инкубации клеток в присутствии исследуемого экстракта.
Жизнеспособность клеток определяли, используя стандартную процедуру подсчета клеток в камере Горяева с предварительным окрашиванием клеточной суспензии раствором трипанового синего. Для этого монослой диспергировали раствором трипсин/версена, клетки ресуспендировали в ростовой среде и готовую клеточную суспензию красили 0,4% раствором Trypan Blue (SIGMA). После этого клетки считали в камере Горяева. Для этого в каждой лунке подсчитывали общее (тотальное) количество клеток и количество окрашенных (нежизнеспособных) клеток.
% жизнеспособных клеток (Nж) рассчитывали по формуле
Влияние исследуемого экстракта Т. canis на пролиферативную активность опухолевых клеток MCF-7 и Сасо-2 оценивали через 96 ч, сравнивая общее количество клеток в опытных лунках относительно контроля.
В ходе эксперимента по оценке влияния исследуемого экстракта Т. canis в указанных концентрациях на эпителиальные культуры опухолевых клеток молочной железы человека (MCF-7) и ободочной кишки человека (Сасо-2) проводили ежедневный визуальный контроль за характером роста и морфологией растущих колоний клеток. Через 24 и 48 ч во всех опытных лунках с клетками MCF-7 и Сасо-2 плотность колоний сопоставима с контролем. Морфологических изменений не обнаружено. Детрит полностью отсутствовал.
Через 72 ч в клетках MCF-7 и Сасо-2 при концентрации 2 мг/мл наблюдали заметное отставание в росте. Отмечено, что в опытных лунках при 2 мг/мл размер колоний был меньше, чем в контрольной группе; также в поле зрения заметно снизилось количество митотически делящихся клеток, при этом морфологических изменений не отмечено. В лунках с клетками MCF-7 и Сасо-2 при 1 и 500 мкг/мл наблюдали незначительное отставание в росте по сравнению с контролем. В опытных лунках с концентрацией 12,5, 25, 50 и 250 мкг/мл отличий в сравнении с контрольной группой К не обнаружено.
Через 96 ч культивирования в клетках MCF-7 и Сасо-2 при концентрациях 2, 1 и 500 мкг/мл в поле зрения наблюдали значительно меньше пролиферирующих колоний, с меньшим количеством клеток, в сравнении с колониями клеток контрольной группы. Морфологические изменения отмечены в клетках MCF-7 только при максимальной концентрации 2 мг/мл. В этой опытной группе видны отдельные колонии, в которых наблюдали клетки без четких и ярко выраженных контуров с потерей характерного рисунка. Количество митотически делящихся клеток в поле зрения снижено. При этом детрит в среде отсутствовал.
После завершения эксперимента, через 96 ч, клетки трипсинизировали, полученную клеточную суспензию красили 0,4% раствором трипановым синим и количество клеток подсчитали в камере Горяева. Результаты подсчета клеток представлены в таблице 1.
При сравнении полученных результатов (таблица 1) по влиянию экстракта Т. canis на культуру опухолевых клеток молочной железы человека и ободочной кишки человека можно предположить, что клетки MCF-7 более чувствительны к негативному действию исследуемого вещества. Так, из данных таблицы 1 следует, что количество жизнеспособных клеток MCF-7 постепенно снижалось с 95,2% при минимальной дозе от 12,5 до 79,5% при максимальном значении 2 мг/мл, по сравнению с контрольным значением 96,8%. Незначительное ингибирующее действие исследуемого экстракта на пролиферативную активность клеток MCF-7 проявлялась при уже в концентрации 50 мкг/мл, где общее количество клеток составляло 151,9×10 3 кл/лунке, в сравнении с контрольным значением 181,3×10 3 кл/лунке. С увеличением концентрации от 100 мкг/мл и выше ингибирующее действие экстракта усиливалось пропорционально концентрации и достигало максимальных значений при 2 мг/мл, где тотальное количество клеток снизилось в три раза по сравнению с контролем и составляло 60,0×10 3 кл/лунку.
На основании результатов, полученных в данной работе, можно заключить следующее.
1. Исследуемый экстракт Т. canis обладает выраженным антипролиферативным действием на клетки MCF-7 в концентрациях 100, 250, 500, 1 и 2 мг/мл, которое проявляется к 96 ч инкубации.
2. Влияние экстракта на клетки MCF-7 носит дозозависимый характер.
3. Ингибирующее действие экстракта Т. canis на пролиферативную активность культуры клеток Сасо-2 проявляется в меньшей степени и в более высоких концентрациях 500, 1 и 2 мг/мл.
4. Культура клеток MCF-7 обладает более высокой чувствительностью к антипролиферативному действию экстракта Т. canis по сравнению с клетками Сасо-2 в модели in vitro через 96 ч культивирования.
1. Средство, обладающее антипролиферативной активностью, представляющее собой белковый экстракт Toxocara canis, полученный путем экстрагирования гомогентата гельминтов Т. Canis фосфатно-солевым буферным раствором с рН 7,2 в соотношении 1:10 в течение 36-48 ч при температуре 4°С, и центрифугирования.
2.Средство по п.1, отличающееся тем, что оно обладает антипролиферативной активностью на моделях опухолевых клеток человека in vitro.