Атипичные клетки что это такое в гинекологии расшифровка
Атипичные клетки – это рак или нет?
Атипичные клетки – это такие клетки, которые под воздействием различных неблагоприятных факторов из обычной нормальной клетки человеческого организма преобразовались в нехарактерную структуру, изменили свой размер и форму. Организм в свою очередь теряет контроль над такими клетками, поэтому существует риск перерождения атипических клеток, что может привести к образованию рака.
Что может повлиять на образование атипичных клеток:
Это некоторые факторы, которые могут привести к образованию атипичных клеток. К сожалению, точной причины их возникновения сказать никто не может. Даже какой-то незначительный сбой в организме может привести к возникновению не одной и даже не двух таких клеток, а тысяч.
Как происходит перерождение атипичных клеток в рак
Давно известно, что образование клеток с измененной ДНК появляются постоянно. Но появление атипичных клеток не всегда приводят к раку. В нашем организме есть защитный механизм, процесс старение и уничтожение клеток, так называемый апоптоз. Он отвечает за то, чтобы аномальные клетки исчезали из организма. Но любая система может дать сбой, и в результате атипичные клетки затаятся в организме. При таком раскладе есть вероятность их перерождения в раковые клетки.
Что делать, если обнаружили атипичные клетки во время биопсии? Рак это или нет?
В такой ситуации лучше перестраховаться, чем что-то пропустить. Ведь ранняя диагностика рака может спасти вам жизнь.
Иногда врач назначает какое-то конкретное лечение, чтобы постараться остановить образование атипичных клеток. Либо может понадобиться еще один образец ткани – дополнительная биопсия, чтобы быть уверенным в отсутствии рака или какого-то другого заболевания.
Цитология шейки матки
Хоперская Ольга Викторовна
Акушер-гинеколог кандидат медицинских наук
Подписаться на email-рассылку
Спасибо за подписку!
Запись на онлайн-консультацию
Ваша заявка будет обработана в течение часа. С Вами свяжется специалист колцентра клиники и согласует время онлайн консультации
Что такое цитология шейки матки? Как осуществляется взятие мазка на цитологическое исследование? Как правильно расшифровать результаты анализа? Что такое nilm,ASC-US, LSIL, HSIL, CIS, AGC, AIS в результатах цитологии? На эти и другие вопросы отвечает кандидат медицинских наук акушер-гинеколог Хоперская Ольга Викторовна.
Цитологическое исследование (цитология) является основным методом скрининговой оценки состояния эпителия шейки матки. Основная задача цитологического скрининга заключается в поиске измененных эпителиальных клеток (атипичных, имеющих отличное от нормальных эпителиальных клеток строение).
Термин «атипичные клетки» подразумевает как клетки с признаками дисплазии – легкой, умеренной или тяжелой (предраковые клетки), так и собственно раковые клетки. Разница между ними – в степени выраженности изменений в строении клеток.
Цитологический скрининг необходимо выполнять всем женщинам (исключая девственниц и пациенток, перенесших экстирпацию (удаление) матки), начиная с 21 года, заканчивая в 69 лет (при отсутствии в исследованиях изменений), регулярность сдачи анализа – 1 раз в год, согласно приказу 572н (1 ноября 2012), однако допустимо сдавать анализ 1 раз в три года (приказ МЗРФ №36 ан, от 3 февраля 2015).
В настоящее время существует две альтернативных методики фиксации и исследования биологического материала, ключевым отличием которых для пациентов является их эффективность.
ПАП-тест и жидкостная цитология
Забор материала осуществляется однотипно (стандартизированный забор): комбинированной щеткой или двумя цитологическими щеточками (рисунок 1), так как эпителий должен быть взят как с наружной вагинальной поверхности шейки матки (эктоцервикса), так и с внутренней – из цервикального канала (эндоцервикса). Необходимость забора клеточного материала из цервикального канала обусловлена тем, что зона стыка эпителиев (цилиндрического и многослойного плоского неороговевающего –места, где чаще всего начинаются «нехорошие» процессы (90-96%случаев)) с возрастом смещается ближе к центру и внутрь цервикального канала.
Рисунок 1 – Цитологические щетки (слева – комбинированная, справа – 2 цитологические щетки)
Рекомендуют осуществлять забор цитологического материала до бимануального (двуручного) вагинального обследования, кольпоскопии и ультразвукового исследования. Не следует сдавать мазки при наличии вагинита (воспалительного процесса во влагалище), в период его лечения, во время менструации. Также за двое суток необходимо половое воздержание.
Техника забора биоматериала:
Отличия ПАП-теста и жидкостной цитологии
В 99% случаев результат, полученный при использовании жидкостной цитологии, совпадает с результатами гистологического исследования.
Единственный недостаток метода – он не включен в систему обязательного медицинского страхования, т. е. анализ платный.
Результаты цитологии шейки матки
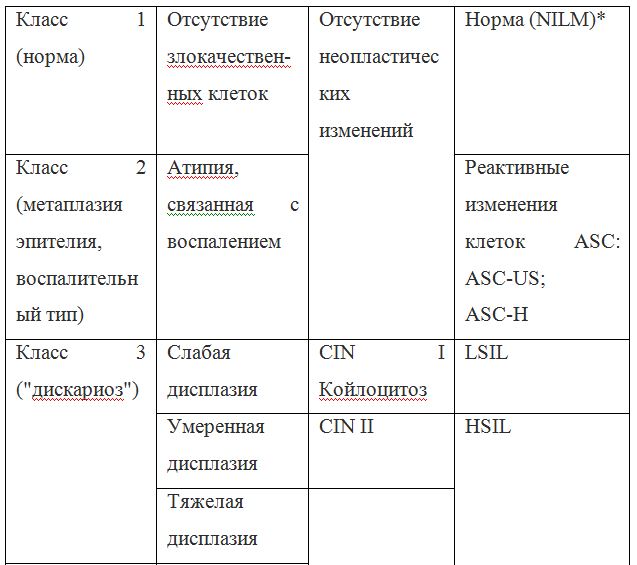
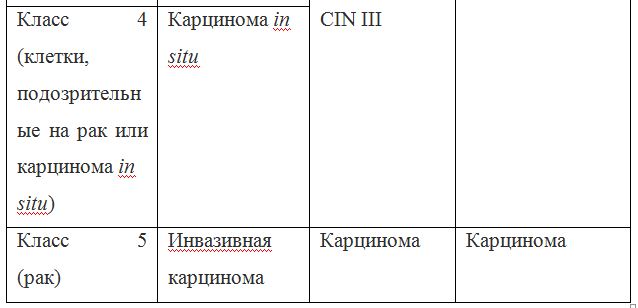
Согласно действующим клиническим рекомендациям от 2017 года, расшифровка результатов анализа должна проводиться по системе Бетесда, хотя можно встретить цитологическое заключение по системам Папаниколау, ВОЗ и CIN (гистологическая классификация). Сравнение систем приведено в таблице 1.
Клиническое значение будут иметь состояния определенные по терминологической системе Бетесда, поэтому, к примеру, умеренная дисплазия, тяжелая дисплазия и карцинома in situ = CIN II и CIN III = HSIL, и тактика ведения всех перечисленных состояний многослойного плоского эпителия будет одинакова (категория HSIL).
Расшифровка результатов
Итак, Вы держите в руках онкоцитологическое заключение. Расшифровка результата, а также выбор тактики ведения на его основании (с учетом возраста и особенностей образа жизни), должны проводиться не Вами, а Вашим лечащим врачом! Именно он направляет Вас на необходимые дополнительные исследования и выбирает тактику лечения, в случае необходимости. Но, кто из нас не заглянет в интернет, чтобы посмотреть, что же все-таки обозначают вынесенные в цитологическом заключении аббревиатуры и к чему готовиться? Думаю, любой переживающий о своем здоровье человек.
Ниже рассмотрим расшифровку аббревиатур терминологической системы Бетесда с ориентировочной (согласно действующим клиническим рекомендациям (2017) тактикой ведения.
Если изменены клетки плоского эпителия:
ASC-US
ASC-Н (atypical squamous cells, cannot exclude HSIL, клетки плоского эпителия с атипией неясного значения не исключающие HSIL) – здесь также обнаружены измененные клетки, но вероятная причина их появления – дисплазия. Врач назначит Вам и кольпоскопию с биопсией и ВПЧ – тестирование, дальнейшая тактика будет определена в зависимости от полученных результатов.
HSIL (high grade squamous intraepitelial lesion, плоскоклеточное интраэпителиальное поражение высокой степени) – в мазке обнаружены атипичные клетки, соответствующие диспластическим изменениям тяжелой степени. Врач направит Вас на кольпоскопическое исследование и эксцизию (иссечение участка измененной ткани петлей) / конизацию (удаление конусовидного участка шейки матки включая влагалищную поверхность и нижнюю часть цервикального канала) с последующим гистологическим исследованием полученного биоматериала. К категории HSIL по классификации Бетесда относится и карцинома in situ (см. таблицу 1, описательная система ВОЗ).
Однако цитологическое исследование не дает представления о пространственном расположении клеток с признаками атипии, установить глубину проникновения патологического процесса в ткани позволяет только гистологическое исследование.
Если изменены клетки цилиндрического эпителия:
Вышеприведенные тактики ведения в зависимости от результатов цитологических исследований ориентировочны. Тактику ведения в каждом конкретном случае определяет лечащий врач, учитывая индивидуальные характеристики пациента (возраст, наличие или отсутствие детей, сопутствующие заболевания, факт инфицирования ВПЧ, личные качества).
Дорогие девушки, женщины, призываю Вас регулярно проводить цитологическое исследование и желаю получать исключительно «NILM» в заключении.
Рак шейки матки: болезнь предотвратима
Поделиться:
Рак шейки матки беспощаден. В мире ежегодно регистрируют более 500 000 новых случаев рака шейки матки, около 53 % женщин погибает. В нашей стране это онкозаболевание уносит жизни 21 женщины ежедневно. Мы многое знаем об этой болезни, ведь шейка матки — орган, вполне доступный осмотру. Почему же до сих пор мы ставим диагноз слишком поздно?
Рак шейки матки
Заболевание с хорошо изученной и доказанной причиной. В 2008 году Харальд цур Хаузен стал лауреатом Нобелевской премии, доказав связь ВПЧ-инфекции (вируса папилломы человека) с развитием рака шейки матки. В далеком 1983 году ему удалось открыть самый агрессивный тип вируса — ВПЧ-16. За 34 года исследований, в которых приняли участие более 10 000 пациенток, было доказано, что 95 % случаев рака шейки матки связано с одним из типов — ВПЧ-16 или ВПЧ-18.
Как всегда, новая идея захватила умы и сердца. Тысячи врачей тогда кинулись искать ВПЧ у миллионов женщин, затем последовали чудовищные попытки избавиться от возбудителя любой ценой. На моей памяти с обещанием «исцелить от ВПЧ навсегда» на рынок выходили десятки препаратов. Восторженные отзывы сменялись недоумением и разочарованием. Каждое последующее лекарство становилось дороже предыдущего, к каждому прилагались доказательства эффективности в виде исследований разной степени доморощенности. Смело могу заявить, что мы однозначно добились только одного эффекта — создали ВПЧ-истерию в окружающем нас пространстве. «Лечение ВПЧ» стало настолько популярным, что я перестала удивляться заявлениям, что кто-то вылечился от ВПЧ коровьими лепешками или аллокином-альфа.
Время большого испуга
Сейчас для большинства специалистов очевидно: ВПЧ высокозаразен, большинство сексуально активных женщин, имеющих более одного партнера, встречаются с ВПЧ хотя бы раз в жизни. ВПЧ — эпителиотропный вирус. Он живет в толще эпителиального пласта на шейке матки, стенках влагалища или на коже наружных половых органов. Более того, место его «прописки» мы часто видим в кольпоскоп, а результаты жизнедеятельности в виде атипических клеток попадают в цитологические мазки.
У меня в кабинете часто рыдают женщины, у которых обнаружен ВПЧ. Их последняя надежда — на «волшебную таблетку», исцеляющую от зловредного вируса. На самом деле повода для слез пока нет.
В большинстве случаев ВПЧ-инфекция не требует совершенно никакого лечения, потому что вирус спонтанно элиминируется — самостоятельно покидает организм безо всякого лечения вместе со слущивающимися клетками многослойного плоского эпителия.
Если ВПЧ-тест положительный, но нет кольпоскопических и цитологических признаков поражения — никакое лечение не требуется.
Бессмысленное и беспощадное применение иммунопрепаратов при латентной форме ВПЧ-инфекции наносит урон не только кошельку, но и, возможно, организму. Надо признать, наши действия в отношении иммунной системы подозрительно напоминают пируэты слона в посудной лавке. Мы даже не можем гордо похвастаться: «Я вылечила Ивановой латентную форму ВПЧ!», — потому что невозможно доказать, почему вирус покинул организм. То ли он сделал это добровольно, то ли ему каким-то образом наскучило наше медикаментозное шаманство.
Чем моложе женщина, тем выше вероятность спонтанной элиминации. Большинство экспертов считает нецелесообразным рутинно обследовать на ВПЧ сексуально активных женщин моложе 25 лет. Тем не менее эти пациентки с латентными формами ВПЧ требуют внимательного наблюдения. Нам придется один-два раза в год повторять обследование, чтобы убедиться, что ВПЧ покинул организм. Среднее время самоэлиминации вируса составляет 1,5 года.
Если на протяжении 1,5–2 лет трижды был выявлен один и тот же тип ВПЧ, можно говорить о персистенции. Заподозрить персистенцию можно и при высокой вирусной нагрузке у женщин старше 30 лет. Это ни в коем случае не означает, что у пациентки есть рак шейки матки или его предстадии, но, безусловно, свидетельствует о существенном риске и требует всё того же — тщательного наблюдения.
Персистенция ВПЧ без кольпоскопических и цитологических признаков поражения — не повод для лечения.
А дальше, как у Ходжи Насреддина: или ишак сдохнет, или султан умрет. Или ВПЧ покинет организм, или мы все-таки «поймаем» изменения в цитологии или кольпоскопии.
Зачем сдавать анализы?
Во-первых, для того, чтобы выделить благополучную группу — женщин без ВПЧ. Их можно реже приглашать на скрининг (при условии моногамных сексуальных отношений), риск заболеть раком шейки матки в этой группе минимален.
Уже в 2009 году удалось доказать, что ВПЧ-отрицательные CIN (предстадии рака шейки матки) невозможны. Если результаты цитологического исследования указывают на предраковое состояние шейки, а анализы на ВПЧ отрицательны, значит, кто-то ошибается.
Я часто предлагаю своим пациенткам мантру: «Нет ВПЧ — нет рака шейки матки». Однако необходимо помнить, что человеческий фактор никто не отменял. Ошибки при взятии материала на исследование, ошибки при хранении и транспортировке, ошибки при проведении исследования могут создать картину ложного благополучия. ВПЧ-тестирование — не «золотой стандарт». Всё следует оценивать в комплексе вместе с цитологией и кольпоскопией.
Кому действительно необходимо исследование на ВПЧ:
Рак шейки матки развивается очень медленно. От момента внедрения ВПЧ в организм до развития рака проходят годы, а иногда даже десятилетия. Сперва деятельность вируса практически незаметна, но как только он встроится в геном клеток, мы увидим характерные изменения в цитологических мазках. Появляются койлоциты (типичные для ВПЧ-инфекции «пустые» клетки ) и дикариоз (различные нарушения в ядре клеток, многоядерные клетки). Эта стадия может длиться от 3 до 20 месяцев.
При неблагоприятных условиях на нижних слоях эпителиального пласта, там, где происходит наиболее активное деление клеток, появляются самые настоящие раковые клеточки. Это CIN I (легкая дисплазия или цервикальная интраэпителиальная неоплазия первой степени). Как бы страшно ни звучало, CIN I — не рак, это состояние развивается за многие годы до настоящего рака.
На этапе CIN I болезнь обратима.
У молодых и/или планирующих беременность женщин мы имеем право продолжать наблюдение от 1,5 до 2 лет. Если процесс не собирается регрессировать, проводится лечение. Медикаментозная терапия малоэффективна, может применяться либо в качестве вспомогательного метода, либо не применяться вовсе. А лечение — это полное удаление очага поражения: эксцизия (удаление пораженной области) или конизация (удаление фрагмента шейки матки в виде конуса).
В среднем, CIN I превращается в CIN II–III за 3–5 лет (конечно, процесс будет намного быстрее при сопутствующей ВИЧ-инфекции, хламидиозе или гонорее). Но ничего непоправимого на этих этапах все еще нет. Если мы «поймали» пациентку на стадиях CIN II – CIN III, то проводится широкое иссечение пораженных зон: эксцизия или конизация шейки матки.
Молодая женщина с CIN I, начитавшись страшилок в интернете, горько рыдает:
— Что же вы так плачете?
— Я прочитала, что у меня будет рак! Я умру!
— Но вы же уже здесь. Грош нам цена была б в базарный день, если бы мы не умели выявлять и лечить эту стадию. Ведь именно за этим вы приходили к гинекологу — чтобы не пропустили CIN. Мы и не пропустили. Теперь все аккуратненько удалим и будем наблюдаться дальше.
— А я смогу родить?
— Обязательно.
— А когда можно будет забеременеть?
— Через 6 недель после операции можно начинать.
Широкое иссечение пораженных участков петлей радиоволнового аппарата — несложная процедура. В основном мы делаем это амбулаторно под местной анестезией. Весь удаленный участок отправляется на гистологическое исследование.
Если все так просто, почему женщины до сих пор умирают?
Это жестокий и правильный вопрос. Рак шейки матки — это всегда чья-то ошибка. Хотя, конечно, если женщина 10 лет не заходила в кабинет к гинекологу, лишь время от времени делая УЗИ, вырастить можно было все, что угодно.
Ольге было 44 года. Я листала ее амбулаторную карту: гинеколог, гинеколог, гинеколог… За последние 10 лет она родила троих детей и сделала 4 аборта. В карте ни одного цитологического мазка. В зеркалах — запущенный рак шейки матки, симптоматическое лечение.
Елена, 32 года. Родила 2 детей с интервалом 2 года, пришла на прием через 4 месяца после вторых родов. Цитологические мазки брали дважды во время беременностей, но, вероятно, очень нежно, опасаясь кровянистых выделений. В зеркалах — рак шейки матки, стадия IIb — будем лечиться.
Марина, 38 лет, повар. Регулярно проходит профосмотр, показывает санитарную книжку. В зеркалах — запущенный рак шейки матки, стадия III, будем лечиться, но прогноз весьма сомнителен. Сомневаюсь, что ее вообще осматривали в зеркалах. Возможно, брали мазки на гонорею и трихомониаз не глядя. Самое обидное, что Ольга была уверена, что у нее все в порядке, поскольку она регулярно обследуется.
Рак шейки — болезнь молодых. Пик заболеваемости в нашей стране приходится на возраст 30–35 лет. Шейка матки — объект легкодоступный для исследования, тем страшнее каждый случай запущенного рака. Болезнь легко предотвратить, поймав на этапе CIN. И женщина выйдет замуж, и родит ребенка или трех, и проживет долгую и яркую жизнь.
Самой молодой моей пациентке с инвазивным раком шейки матки было 23 года. Ее привел за руку юноша, чтобы обследоваться на инфекции. Юношу беспокоил неприятный запах выделений возлюбленной. Операция Вертгейма, лучевая терапия, потом рецидив, химиотерапия. Она умерла через 2 года после постановки диагноза.
Нельзя не учитывать человеческий фактор. Кто-не пришел на прием, кто-то не взял цитологический мазок или собрал материал недостаточно хорошо, кто-то не рассмотрел единичные атипические клетки из-за выраженных воспалительных изменений. Причин для поздней диагностики много. От внедрения ВПЧ в геном эпителиальных клеток до начала рака проходят годы, но инвазивный рак растет и прогрессирует очень быстро.
Сегодня в РФ повсеместно внедряется новая стратегия цервикального скрининга — применение жидкостной цитологии с ВПЧ-тестированием. Это значительно повышает шансы ранней диагностики рака. Именно этой проблемой должны заниматься гинекологи, а не «прижиганием эрозий» и беспощадным сражением с ВПЧ.
Давайте ставить цели правильно. Мы стремимся поймать рак на его предстадиях и обезвредить. «Прижигания» всего, что краснеет, никак не помогают диагностике, напротив, создают серьезные трудности, маскируя медленно тлеющий процесс.
Охота на CIN
Выполнение простого алгоритма гарантирует своевременную диагностику изменений шейки матки.
После лечения CIN настоятельно рекомендуется продолжать наблюдение не менее 5 лет. Всякое бывает — болезнь может рецидивировать. Если не теряться из виду на пару-тройку лет, можно вовремя заметить рецидив и не допустить развития инвазивного рака.
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.