какие физические свойства имеют щелочноземельные металлы
Щелочноземельные металлы
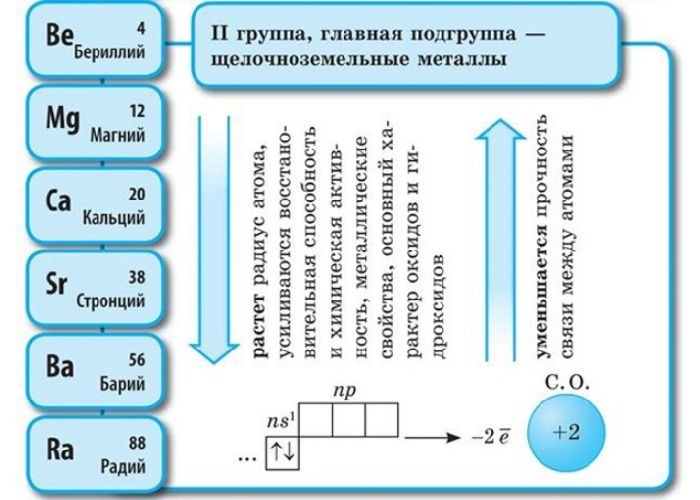
С увеличением заряда ядра атомов элементов, входящих в группу щелочноземельных металлов, энергия ионизации атомов уменьшается, а радиусы атомов и ионов увеличиваются, металлические признаки химических элементов усиливаются.
Физические свойства щелочноземельных металлов
В свободном состоянии Be – металл серо-стального цвета, обладающий плотной гексагональной кристаллической решеткой, достаточно твердый и хрупкий. На воздухе Be покрывается оксидной пленкой, что придает ему матовый оттенок и снижает его химическую активность.
Магний в виде простого вещества представляет собой белый металл, который, также, как и Be, при нахождении на воздухе приобретает матовый оттенок за счет образующейся оксидной пленки. Mg мягче и пластичнее бериллия. Кристаллическая решетка Mg – гексагональная.
Ca, Ba и Sr в свободном виде – серебристо-белые металлы. При нахождении на воздухе мгновенно покрываются желтоватой пленкой, которая представляет собой продукты их взаимодействия с составными частями воздуха. Кальций – достаточно твердый металл, Ba и Sr – мягче.
Ca и Sr имею кубическую гранецентрированную кристаллическую решетку, барий – кубическую объемоцентрированную кристаллическую решетку.
Все щелочноземельные металлы характеризуются наличием металлического типа химической связи, что обуславливает их высокую тепло- и электропроводность. Температуры кипения и плавления щелочноземельных металлов выше, чем щелочных металлов.
Получение щелочноземельных металлов
Получение Be осуществляют по реакции восстановления его фторида. Реакция протекает при нагревании:
Магний, кальций и стронций получают электролизом расплавов солей, чаще всего – хлоридов:
Причем, при получении Mg электролизом расплава дихлорида для понижения температуры плавления в реакционную смесь добавляют NaCl.
Для получения Mg в промышленности используют металло- и углетермические методы:
2(CaO×MgO) (доломит) + Si = Ca2SiO4 + Mg
Основной способ получения Ba – восстановление оксида:
Химические свойства щелочноземельных металлов
Поскольку в н.у. поверхность Be и Mg покрыта оксидной пленкой – эти металлы инертны по отношению к воде. Ca, Sr и Ba растворяются в воде с образованием гидроксидов, проявляющих сильные основные свойства:
Щелочноземельные металлы способны реагировать с кислородом, причем все они, за исключением бария, в результате этого взаимодействия образуют оксиды, барий – пероксид:
Оксиды щелочноземельных металлов, за исключением бериллия, проявляют основные свойства, Be – амфотерные свойства.
При нагревании щелочноземельные металлы способны к взаимодействию с неметаллами (галогенами, серой, азотом и др.):
Щелочноземельные металлы реагируют с кислотами – растворяются в них:
Бериллий реагирует с водными растворами щелочей – растворяется в них:
Качественные реакции
Качественной реакцией на щелочноземельные металлы является окрашивание пламени их катионами: Ca 2+ окрашивает пламя в темно-оранжевый цвет, Sr 2+ — в темно-красный, Ba 2+ — в светло-зеленый.
Примеры решения задач
| Задание | Осуществите ряд превращений: Ca→CaO→Ca(OH)2→Ca(NO3)2 |
| Решение | 2Ca + O2→2CaO |
| Задание | Определите массу кальция, необходимую для получения 300 г 40-%-го раствора гидроксида кальция. |
| Решение | Запишем уравнение реакции: |
Найдем массу образовавшегося гидроксида кальция:
m(Ca(OH)2) = 300×40/100% = 120 г
Вычислим количество вещества гидроксида кальция:
v(Ca(OH)2) = 120/ 74 = 1,62 моль
Щелочноземельные металлы
Щелочноземельные металлы.
К щелочноземельным металлам относятся бериллий Be, магний Mg, кальций Ca, стронций Sr, барий Ba, радий Ra.
Щелочноземельные металлы:
Щелочноземельные металлы – это элементы 2-й группы периодической таблицы химических элементов Д.И. Менделеева (по устаревшей классификации – элементы главной подгруппы II группы):
– бериллий Be,
– кальций Ca,
– стронций Sr,
– барий Ba,
– радий Ra.
Строение атомов щелочноземельных металлов:
Щелочноземельные металлы относятся к элементам s-семейства.
Радиус атома бериллия составляет 112 пм. Потенциал ионизации атома бериллия равен 9,32 эВ (898,8 кДж/моль). Электроотрицательность атома бериллия равна 1,57 (шкала Полинга).
Радиус атома магния составляет 160 пм. Потенциал ионизации атома магния равен 7,64 эВ (737,3 кДж/моль). Электроотрицательность атома магния равна 1,31 (шкала Полинга).
Радиус атома кальция составляет 197 пм. Потенциал ионизации атома кальция равен 6,11 эВ (589,4 кДж/моль). Электроотрицательность атома кальция равна 1,00 (шкала Полинга).
Радиус атома стронция составляет 215 пм. Потенциал ионизации атома стронция равен 5,69 эВ (549,0 кДж/моль). Электроотрицательность атома стронция равна 0,95 (шкала Полинга).
Радиус атома бария составляет 222 пм. Потенциал ионизации атома бария равен 5,21 эВ (502,5 кДж/моль). Электроотрицательность атома бария равна 0,89 (шкала Полинга).
С увеличением порядкового номера у щелочноземельных металлов увеличиваются радиус атома, способность отдавать валентные электроны и восстановительная активность, уменьшается электроотрицательность и энергия ионизации.
Физические свойства щелочноземельных металлов:
Все щёлочноземельные металлы серые или серебристо-белые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение – стронций).
Общими физическими свойствами щелочноземельных металлов являются: их металлический блеск, ковкость, пластичность, высокая тепло- и электропроводность.
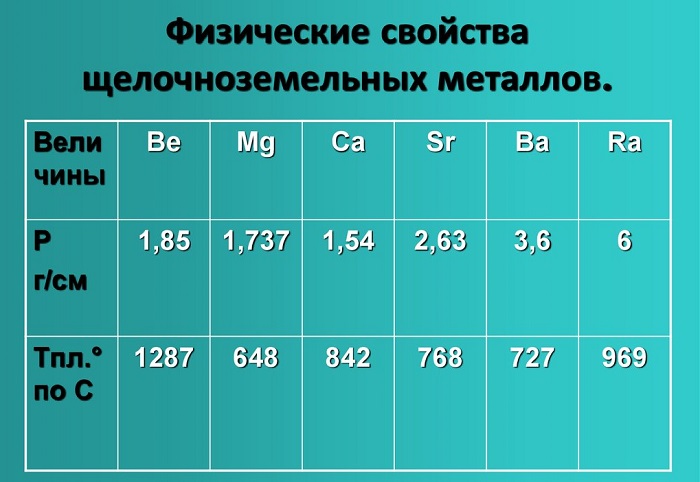
Вместе с тем указанные металлы имеют разные значения температуры плавления, кипения, плотности и другие физические свойства.
При этом с увеличением порядкового номера у щелочноземельных металлов каких-либо закономерностей в изменении физических свойств не проявляется.
Химические свойства щелочноземельных металлов:
В соединениях щелочноземельные металлы проявляют единственную степень окисления +2 (очень редко +1) и валентность II. Они являются сильными восстановителями.
С увеличением порядкового номера у щелочноземельных металлов усиливаются металлические свойства и ослабевают неметаллические свойства, увеличивается восстановительная способность, возрастает химическая активность.
Щёлочноземельные металлы получили свое название за счет своих оксидов, которые сообщают воде щелочные реакции. Изучая химию, очень часто приходится взаимодействовать со сложными и непонятными названиями. Но если разобраться и понять что к чему, то изучать предмет легко и интересно.
Однако при написании формул стоит быть внимательным, не забывая про коэффициенты и признаки реакций.
Положение в периодической системе Менделеева
Щелочноземельные металлы – это химические элементы второй группы периодической системы химических элементов таблицы Менделеева:
Электронное строение и закономерности изменения свойств
Атомы данных металлов на внешнем энергетическом уровне имеют 2 s-электрона. Отсюда следует, что максимальная степень окисления +2.
Также могут иметь нулевую степень окисления, но не отрицательную, так как металлы не могут иметь данную степень.
Общая конфигурация внешнего энергетического уровня nS 2 :
В периоде от Be до Ra металлические свойства, восстановительные, электроотрицательные увеличиваются, а неметаллические, окислительные свойства и радиус атома уменьшается.
Физические свойства щелочноземельных металлов
Физические свойства данной группы имеют следующие характеристики: светло-серый — темно-серый цвет, твердые вещества, не растворимые и нелетучие, без запаха, тепло-электропроводимые, имеют характерный металлический блеск.
Показатели плотности и температуры плавления представлены в таблице:
Химические свойства
Оксиды и гидроксиды щёлочноземельных металлов усиливают основные свойства при движении вниз по второй группе. Следовательно, бериллий имеет меньшие основные свойства, чем радий.
Эти вещества взаимодействуют с любыми растворами кислот от сильной до слабой, а также с образованием солей, образуя белый осадок.
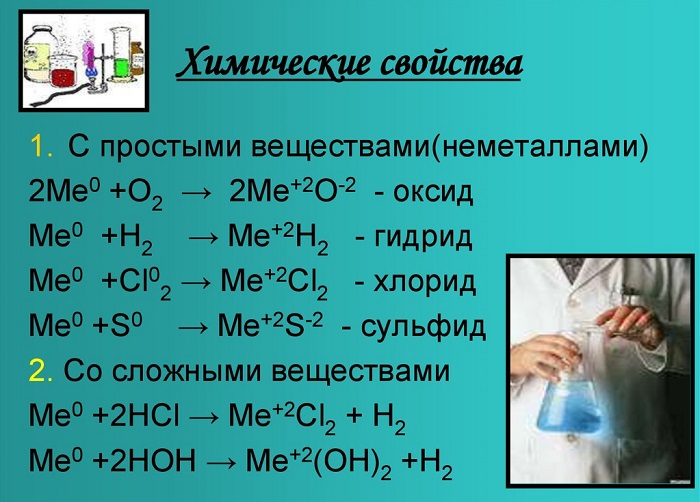
С кислородом образуют реакцию горения и оксид:
Металлы, стоящие в главной подгруппе второй группы (кроме бериллия) реагируют с водой. При проведении данных реакций выделяется водород (H2):
Также реагируют с неметаллами:
Bа + Cl2 = BаCl2 — хлорид бериллия;
Ca + Br2 = CaBr2 — бромид кальция;
Sr + H2 = SrH2 — гидрид стронция.
Химические свойства щелочноземельных металлов показаны на картинке:
Нахождение в природе
Все металлы данного типа встречаются на земле, но не в чистом виде. Часто они представлены в виде минеральных солей. Самый распространённый считается кальций, магний немного уступает, затем идет барий и стронций.
Бериллий и радий являются самыми редкими, однако последний металл в больших количествах находится в урановых рудах.
Способ получения
Магний, кальций и стронций получают электролизом расплавов солей.
Барий получают с помощью восстановления оксида.
При нагревании фторида бария получают сам металл.
Качественные реакции
Одна из качественных реакций-окрашивание пламени.
Список возможных цветов пламени при нагревании данных элементов:
Sr — насыщенный красный;
Металлы данного типа при взаимодействии с щелочами, оксидами или растворами солей выпадают в белый осадок.
Применение щелочноземельных металлов
Бериллий из-за своей прочности добавляют в различные сплавы металлов, также препятствует коррозии. Используется в изготовлении рентгеновских аппаратов.
Магний и кальций активно использует для лекарственных средств, поскольку данные металлы играют большую роль в жизнедеятельности организма. Также в медицине используют радий, но для облучения кожи и злокачественных образований.
Стронций и барий добавляют в различный сплавы, которые работают в агрессивной среде и имеют сверхсильную проводимость.
Данные металлы играют огромную роль в жизни человека, выполняют различные функции и имеют ряд определенных свойств. Они содержатся в земной коре, поэтому довольно широко используются. Однако это не говорит о том, что их нужно расходовать безгранично.
Щелочноземельные металлы и их соединения
Элементы II группы главной подгруппы
Элементы II группы главной подгруппы
Положение в периодической системе химических элементов
Щелочноземельные металлы расположены во второй группе главной подгруппе периодической системы химических элементов Д.И. Менделеева (или просто во 2 группе в длиннопериодной форме ПСХЭ). На практике к щелочноземельным металлам относят только кальций Ca, стронций Sr, барий Ba и радий Ra. Бериллий Be по свойствам больше похож на алюминий, магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них. Однако, согласно номенклатуре ИЮПАК, щелочноземельными принято считать все металлы II группы главной подгруппы.
Электронное строение и закономерности изменения свойств
Рассмотрим некоторые закономерности изменения свойств щелочноземельных металлов.
Физические свойства
Все щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы.
Бериллий Be устойчив на воздухе. Магний и кальций (Mg и Ca) устойчивы в сухом воздухе. Стронций Sr и барий Ba хранят под слоем керосина.
Кристаллическая решетка щелочноземельных металлов в твёрдом состоянии — металлическая. Следовательно, они обладают высокой тепло- и электропроводимостью. Кипят и плавятся при высоких температурах.
Нахождение в природе
Как правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др. Основные минералы, в которых присутствуют щелочноземельные металлы:
Доломит — CaCO3 · MgCO3 — карбонат кальция-магния.
Магнезит MgCO3 – карбонат магния.
Кальцит CaCO3 – карбонат кальция.
Гипс CaSO4 · 2H2O – дигидрат сульфата кальция.
Барит BaSO4 — сульфат бария.
Витерит BaCO3 – карбонат бария.
Способы получения
Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С:
или восстановлением прокаленного доломита в электропечах при 1200–1300°С:
2(CaO · MgO) + Si → 2Mg + Ca2SiO4
Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция:
Барий получают восстановлением оксида бария алюминием в вакууме при 1200 °C:
4BaO+ 2Al → 3Ba + Ba(AlO2)2
Качественные реакции
Цвет пламени:
Ca — кирпично-красный
Sr — карминово-красный (алый)
Ba — яблочно-зеленый
Качественная реакция на ионы магния : взаим одействие с щелочами. Ионы магния осаждаются щелочами с образованием белого осадка гидроксида магния:
Mg 2+ + 2OH — → Mg(OH)2↓
Качественная реакция на ионы кальция, стронция, бария : взаим одействие с карбонатами. При взаимодействии солей кальция, стронция и бария с карбонатами выпадает белый осадок карбоната кальция, стронция или бария :
Ca 2+ + CO3 2- → CaCO3↓
Ba 2+ + CO3 2- → BaCO3↓
Качественная реакция на ионы стронция и бария : взаим одействие с карбонатами. При взаимодействии солей стронция и бария с сульфатами выпадает белый осадок сульфата бария и сульфата стронция :
Ba 2+ + SO4 2- → BaSO4↓
Sr 2+ + SO4 2- → SrSO4↓
Также осадки белого цвета образуются при взаимодействии солей кальция, стронция и бария с сульфитами и фосфатами.
Химические свойства
1.1. Щелочноземельные металлы реагируют с галогенами с образованием галогенидов при нагревании.
1.2. Щелочноземельные металлы реагируют при нагревании с серой и фосфором с образованием сульфидов и фосфоридов.
Ca + S → CaS
Кальций взаимодействует с фосфором с образованием фосфидов:
1.4. С азотом магний взаимодействует при комнатной температуре с образованием нитрида:
Остальные щелочноземельные металлы реагируют с азотом при нагревании.
1.5. Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов.
Ca + 2C → CaC2
Бериллий реагирует с углеродом при нагревании с образованием карбида — метанида:
2Be + C → Be2C
1.6. Бериллий сгорает на воздухе при температуре около 900°С:
2Be + O2 → 2BeO
Магний горит на воздухе при 650°С с выделением большого количества света. При этом образуются оксиды и нитриды:
2Mg + O2 → 2MgO
Щелочноземельные металлы горят на воздухе при температуре около 500°С, в результате также образуются оксиды и нитриды.
Видеоопыт : горение кальция на воздухе можно посмотреть здесь.
2. Щелочноземельные металлы взаимодействуют со сложными веществами:
2 Ca 0 + 2 H2 + O = 2 Ca + ( OH)2 + H2 0
2.2. Щелочноземельные металлы взаимодействуют с минеральными кислотами (с соляной, фосфорной, разбавленной серной кислотой и др.). При этом образуются соль и водород.
2Mg + 2HCl → MgCl2 + H2↑
2.3. При взаимодействии щелочноземельных металлов с концентрированной серной кислотой образуется сера.
При взаимодействии щелочноземельных металлов с очень разбавленной азотной кислотой образуется нитрат аммония:
2.5. Щелочноземельные металлы могут восстанавливать некоторые неметаллы (кремний, бор, углерод) из оксидов.
2Ca + SiO2 → 2CaO + Si
2Mg + CO2 → 2MgO + C
Ca + CuCl2 → CaCl2 + Cu
Оксиды щелочноземельных металлов
Способы получения
1. О ксиды щелочноземельных металлов можно получить из простых веществ — окислением металлов кислородом :
2Ca + O2 → 2CaO
3. Оксиды магния и бериллия можно получить термическим разложением гидроксидов :
Химические свойства
1. Оксиды кальция, стронция, бария и магния взаимодействуют с кислотными и амфотерными оксидами :
2. Оксиды щелочноземельных металлов взаимодействуют с кислотами с образованием средних и кислых солей (с многоосновными кислотами).
CaO + 2HCl → CaCl2 + H2O
3. Оксиды кальция, стронция и бария активно взаимодействуют с водой с образованием щелочей.
CaO + H2O → 2Ca(OH)2
Оксид магния реагирует с водой при нагревании:
MgO + H2O → Mg(OH)2
Оксид бериллия не взаимодействует с водой.
4. Оксид бериллия взаимодействует с щелочами и основными оксидами.
При взаимодействии оксида бериллия с щелочами в расплаве или с основными оксидами образуются соли-бериллаты.
При взаимодействии оксида бериллия с щелочами в растворе образуются комплексные соли.
Гидроксиды щелочноземельных металлов
Способы получения
Оксид магния взаимодействует с водой только при нагревании:
2. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих металлов с водой.
Магний взаимодействует с водой только при кипячении:
Химические свойства
1. Гидроксиды кальция, стронция и бария реагируют с всеми кислотами (и сильными, и слабыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов.
Гидроксид магния взаимодействует только с сильными кислотами.
в растворе образуется комплексная соль — тетрагидроксоалюминат:
4. Гидроксиды кальция, стронция и бария взаимодействуют с кислыми солями. При этом образуются средние соли, или менее кислые соли.
Например : гидроксид кальция реагирует с гидрокарбонатом кальция с образованием карбоната кальция:
5. Гидроксиды кальция, стронция и бария взаимодействуют с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода). Взаимодействие щелочей с неметаллами подробно рассмотрено в статье про щелочные металлы.
В растворе образуются комплексная соль и водород:
7. Гидроксиды кальция, стронция и бария вступают в обменные реакции с растворимыми солями. Как правило, с этими гидроксидами реагируют растворимые соли тяжелых металлов (в ряду активности расположены правее алюминия), а также растворимые карбонаты, сульфиты, силикаты, и, для гидроксидов стронция и бария — растворимые сульфаты.
Также с гидроксидами кальция, стронция и бария взаимодействуют соли аммония.
8. Гидроксид кальция разлагается при нагревании до 580 о С, гидроксиды магния и бериллия разлагаются при нагревании:
Ba(OH)2 ↔ Ba 2+ + 2OH —
Гидроксид магния — нерастворимое основание. Гидроксид бериллия проявляет амфотерные свойства.
При взаимодействии гидроксида бериллия с избытком раствора щелочи образуется комплексная соль:
Соли щелочноземельных металлов
Нитраты щелочноземельных металлов
Нитраты кальция, стронция и бария при нагревании разлагаются на нитриты и кислород. Исключение — нитрат магния. Он разлагается на оксид магния, оксид азота (IV) и кислород.
Карбонаты щелочноземельных металлов
1. Карбонаты щелочноземельных металлов при нагревании разлагаются на оксид и углекислый газ.
2. Карбонаты щелочноземельных металлов под действием воды и углекислого газа превращаются в растворимые в воде гидрокарбонаты.
3. Карбонаты щелочноземельных металлов взаимодействуют с более сильными кислотами с образованием новой соли, углекислого газа и воды.
Более сильные кислоты вытесняют менее сильные из солей.
4. Менее летучие оксиды вытесняют углекислый газ из карбонатов при сплавлении. К менее летучим, чем углекислый газ, оксидам относятся твердые оксиды — оксид кремния (IV), оксиды амфотерных металлов.
Менее летучие оксиды вытесняют более летучие оксиды из солей при сплавлении.
Жесткость воды
Постоянная и временная жесткость
Жесткость воды — это характеристика воды, обусловленная содержанием в ней растворенных солей щелочноземельных металлов, в основном кальция и магния (солей жесткости).
Временная (карбонатная) жесткость обусловлена присутствием гидрокарбонатов кальция Ca(HCO3)2 и магния Mg(HCO3)2 в воде.
Постоянная (некарбонатная) жесткость обусловлена присутствием солей, не выделяющихся при кипячении из раствора: хлоридов (CaCl2) и сульфатов (MgSO4) кальция и магния.
Способы устранения жесткости
Существуют химические и физические способы устранения жесткости. Химические способы устранения временной жесткости:
1. Кипячение. При кипячении гидрокарбонаты кальция и магния распадаются на нерастворимые карбонаты, углекислый газ и воду:
2. Добавление извести (гидроксида кальция). При добавлении щелочи растворимые гидрокарбонаты переходят в нерастворимые карбонаты:
Химические способы устранения постоянной жесткости — реакции ионного обмена, которые позволяют осадить ионы кальция и магния из раствора:
1. Добавление соды (карбоната натрия). Карбонат натрия связывает ионы кальция и магния в нерастворимые карбонаты:
CaCl2 + Na2CO3 → CaCO3↓+ 2NaCl
2. Добавление фосфатов. Фосфаты также связывают ионы кальция и магния: