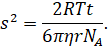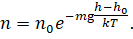какие силы действуют между молекулами твердых тел
Какие силы действуют между молекулами твердых тел
Можно ли объяснить свойства вещества во всех его агрегатных состояниях строением вещества, движением и взаимодействием его частиц?
Силы взаимодействия молекул.
Молекулы взаимодействуют друг с другом. Без этого взаимодействия не было бы ни твёрдых, ни жидких тел.
Доказать существование значительных сил взаимодействия между атомами или молекулами несложно. Попробуйте-ка сломать толстую палку! А ведь она состоит из молекул. Но одни силы притяжения не могут обеспечить существования устойчивых образований из атомов и молекул. На очень малых расстояниях между молекулами обязательно действуют силы отталкивания. Благодаря этому молекулы не проникают друг в друга и куски вещества никогда не сжимаются до размеров порядка размеров одной молекулы.
Молекула — это сложная система, состоящая из отдельных заряженных частиц: электронов и атомных ядер.
В целом молекулы электрически нейтральны, тем не менее между ними на малых расстояниях действуют значительные электрические силы: происходит взаимодействие электронов и атомных ядер соседних молекул.
Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не сказываются.
На расстояниях, превышающих 2—3 диаметра молекул, действуют силы притяжения. По мере уменьшения расстояния между молекулами сила их взаимного притяжения сначала увеличивается, но одновременно увеличивается и сила отталкивания. При определённом расстоянии r0 сила притяжения становится равной силе отталкивания. Это расстояние считается равным диаметру молекулы.
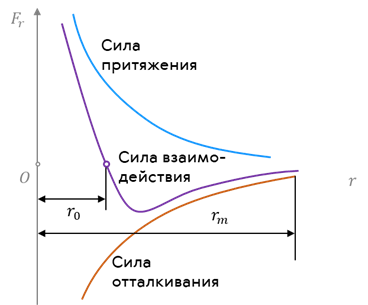
При дальнейшем уменьшении расстояния электронные оболочки атомов начинают перекрываться и быстро увеличивается сила отталкивания. На рисунке 8.5 показаны графики зависимости потенциальной энергии взаимодействия молекул (рис. 8.5, а) и сил притяжения (1) и отталкивания (2) (рис. 8.5, б) от расстояния между молекулами. При r = r0 потенциальная энергия минимальна, сила притяжения равна силе отталкивания. При r > r0 сила притяжения больше силы отталкивания; при r
Молекулы жидкости находятся непосредственно друг возле друга. При уменьшении объёма силы отталкивания становятся очень велики. Этим и объясняется малая сжимаемость жидкостей.
Жидкости: 1) малосжимаемы;
2) текучи, т. е. не сохраняют своей формы.
Объяснить текучесть жидкостей можно так. Внешняя сила заметно не меняет числа перескоков молекул в секунду. Но перескоки молекул из одного оседлого положения в другое происходят преимущественно в направлении действия внешней силы. Вот почему жидкость течёт и принимает форму сосуда.
В жидкостях средняя кинетическая энергия теплового движения молекул сравнима со средней потенциальной энергией их взаимодействия. Наличие поверхностного натяжения доказывает, что силы взаимодействия молекул жидкостей существенны, и ими пренебрегать нельзя.
Твёрдые тела.
Атомы или молекулы твёрдых тел, в отличие от атомов и молекул жидкостей, колеблются около определённых положений равновесия. По этой причине твёрдые тела сохраняют не только объём, но и форму.
В твёрдых телах средняя потенциальная энергия взаимодействия молекул много больше средней кинетической энергии их теплового движения.
Если соединить центры положений равновесия атомов или ионов твёрдого тела, то получится правильная пространственная решётка, называемая кристаллической.
На рисунках 8.6 и 8.7 изображены кристаллические решётки поваренной соли и алмаза. Внутренний порядок в расположении атомов кристаллов приводит к правильным внешним геометрическим формам.
Какие силы действуют между молекулами твердых тел
Силы взаимодействия молекул
Атом состоит из положительно заряженного ядра и отрицательно заряженной электронной оболочки. Заряд ядра равен суммарному заряду всех электронов, поэтому в целом атом электрически нейтрален.
Молекула, состоящая из одного или нескольких атомов, тоже электрически нейтральна.
Рассмотрим взаимодействие между молекулами на примере двух неподвижных молекул.
Между телами в природе могут существовать гравитационные и электромагнитные силы.
Так как массы молекул крайне малы, ничтожно малые силы гравитационного взаимодействия между молекулами можно не рассматривать.
На очень больших расстояниях электромагнитного взаимодействия между молекулами тоже нет.
Но, при уменьшении расстояния между молекулами молекулы начинают ориентироваться так, что их обращенные друг к другу стороны будут иметь разные по знаку заряды (в целом молекулы остаются нейтральными), и между молекулами возникают силы притяжения.
При еще большем уменьшении расстояния между молекулами возникают силы отталкивания, как результат взаимодействия отрицательно заряженных электронных оболочек атомов молекул.
В итоге на молекулу действует сумма сил притяжения и отталкивания. На больших расстояниях преобладает сила притяжения (на расстоянии 2-3 диаметров молекулы притяжение максимально), на малых расстояниях сила отталкивания.
Существует такое расстояние между молекулами, на котором силы притяжения становятся равными силам отталкивания. Такое положение молекул называется положением устойчивого равновесия.
Находящиеся на расстоянии друг от друга и связанные электромагнитными силами молекулы обладают потенциальной энергией.
В положении устойчивого равновесия потенциальная энергия молекул минимальна.
В веществе каждая молекула взаимодействует одновременно со многими соседними молекулами, что также влияет на величину минимальной потенциальной энергии молекул.
Кроме того, все молекулы вещества находятся в непрерывном движении, т.е. обладают кинетической энергией.
Таким образом, структура вещества и его свойства (твердых, жидких и газообразных тел) определяются соотношением между минимальной потенциальной энергией взаимодействия молекул и запасом кинетической энергии теплового движения молекул.
Строение и свойства твердых, жидких и газообразных тел
Строение тел объясняется взаимодействием частиц тела и характером их теплового движения.
Твердое тело
Твердые тела имеют постоянную форму и объем, практически несжимаемы.
Минимальная потенциальная энергия взаимодействия молекул больше кинетической энергии молекул.
Сильное взаимодействие частиц.
Тепловое движение молекул в твердом теле выражается только лишь колебаниями частиц (атомов, молекул) около положения устойчивого равновесия.
Из-за больших сил притяжения молекулы практически не могут менять свое положение в веществе, этим и объясняется неизменность объема и формы твердых тел.
Жидкость
Жидкости имеют определенный объем, но не имеют своей формы, они принимают форму сосуда, в которой находятся.
Минимальная потенциальная энергия взаимодействия молекул сравнима с кинетической энергией молекул.
Слабое взаимодействие частиц.
Тепловое движение молекул в жидкости выражено колебаниями около положения устойчивого равновесия внутри объема, предоставленного молекуле ее соседями
Молекулы не могут свободно перемещаться по всему объему вещества, но возможны переходы молекул на соседние места. Этим объясняется текучесть жидкости, способность менять свою форму.
В жидкостях молекулы достаточно прочно связаны друг с другом силами притяжения, что объясняет неизменность объема жидкости.
В жидкости расстояние между молекулами равно приблизительно диаметру молекулы. При уменьшении расстояния между молекулами (сжимании жидкости) резко увеличиваются силы отталкивания, поэтому жидкости несжимаемы.
По своему строению и характеру теплового движения жидкости занимают промежуточное положение между твердыми телами и газами.
Хотя разница между жидкостью и газом значительно больше, чем между жидкостью и твердым телом. Например, при плавлении или кристаллизации объем тела изменяется во много раз меньше, чем при испарении или конденсации.
Газы не имеют постоянного объема и занимают весь объем сосуда, в котором они находятся.
Минимальная потенциальная энергия взаимодействия молекул меньше кинетической энергии молекул.
Частицы вещества практически не взаимодействуют.
Газы характеризуются полной беспорядочностью расположения и движения молекул.
Расстояние между молекулами газа во много раз больше размеров молекул. Малые силы притяжения не могут удержать молекулы друг около друга, поэтому газы могут неограниченно расширяться.
Газы легко сжимаются под действием внешнего давления, т.к. расстояния между молекулами велики, а силы взаимодействия пренебрежимо малы.
Давление газа на стенки сосуда создается ударами движущихся молекул газа.
Виды межмолекулярного взаимодействия твердых тел
Межмолекулярное взаимодействие в химии, суть процесса
Различные атомы и группы атомов, входящие в состав молекулы вещества могут осуществлять внутримолекулярное и межмолекулярное взаимодействие, приводящее к образованию нового типа связей — межмолекулярных связей.
Межмолекулярным называют взаимодействие частиц (атомов, молекул или ионов), проявляющееся на расстояниях, значительно превышающих размеры этих частиц.
Данное явление объясняет отличие идеальных газов от реальных, нахождение одних и тех же веществ в разных агрегатных состояниях и влияет на такие физические свойства, как плотность, электро- и теплопроводность, температура кипения и плавления, твердость и другие.
Первым понятие межмолекулярного взаимодействия ввел голландский ученый Йоханнес Дидерик ван-дер-Ваальс в 1873 году, когда изучал свойства реальных газов и жидкостей. Поэтому силы, обеспечивающие межмолекулярное взаимодействие, также называют ван-дер-ваальсовыми силами.
Отличия межмолекулярного взаимодействия от химической связи:
Основные виды межмолекулярного взаимодействия
Ван-дер-ваальсовы взаимодействия (силы) имеют электростатический характер и образуются за счет диполей (молекул, содержащих два одинаковых по величине, но разных по знаку заряда, находящимися на расстоянии друг от друга). В зависимости от вещества механизм образования диполей различен, поэтому выделяют три составляющие ван-дер-ваальсовых сил:
Влияние агрегатного состояния вещества на ван-дер-ваальсовы взаимодействия
Атомы или молекулы газообразных веществ постоянно двигаются в разных направлениях, поэтому большую часть времени находятся на значительных (по сравнению с собственными размерами) расстояниях друг от друга. Силы межмолекулярного взаимодействия между ними настолько малы, что его даже не учитывают, кроме тех случаев, когда газ находится под высоким давлением.
Частицы веществ в конденсированном состоянии (жидком или твердом) находятся ближе друг к другу, а силы взаимодействия достаточно велики для того, чтобы удержать их в таком положении. Поэтому жидкие и твердые вещества имеют, в отличие от газов, постоянный при данной температуре объем.
Для твердых тел (кристаллов) силы межмолекулярного взаимодействия обеспечивают сохранение не только объема, но и формы. Правильная геометрическая форма (кристаллическая решетка), в узлах которой находятся электрически нейтральные частицы, называется молекулярным кристаллом.
Для некоторых твердых тел свойственно наличие сразу нескольких видов связи. Примером такого вещества является графит с гексагональной решеткой:
Мягкость графита и скольжение его слоев друг относительно друга обусловлена этими факторами.
Водородная связь — частный случай ориентационных межмолекулярных сил, образующихся между положительно поляризованным атомом водорода одной группы или молекулы и отрицательно поляризованным атомом другой. Функцию отрицательного полюса выполняет атом с высокой отрицательностью (кислород, фтор, азот и др.).
Если представить соединение с формулой X-H, то водородная связь будет выглядеть так: X-H⋅⋅⋅Y (или H⋅⋅⋅Y), где Y — атом с высокой отрицательностью, входящий в состав какого либо вещества, образующего с X-H водородные связи.
В силу высокой прочности (сравнительно с другими вариантами межмолекулярного взаимодействия), широкой распространенности и важности в объяснении свойств различных соединений водородная связь рассматривается как отдельный тип межмолекулярных связей.
Значение водородной связи:
Водородные связи могут быть как внутримолекулярными (образуются между фрагментами одной молекулы), так и межмолекулярными (возникают между частями разных молекул).
Энергия межмолекулярного взаимодействия молекул
Энергия ориентационного взаимодействия Еориент растет при увеличении дипольных моментов частиц, уменьшается при повышении температуры.
Энергия индукционного взаимодействия Еинд увеличивается с ростом дипольного момента полярной молекулы и с увеличением поляризуемости неполярной. Не зависит от температуры.
Энергия дисперсионного взаимодействия Едисп пропорциональна квадрату поляризуемости частиц. Низкая поляризуемость характерна для многих соединений фтора, следовательно, они проявляют слабое дисперсионное взаимодействие. Доказательством этого является сравнительная таблица 1 температур кипения соединений фтора и хлора, похожих по строению:
| CF4 | CCl4 | OF2 | OCl2 | |
| tкип, °C | -128 | 76 | -144 | 3,8 |
Электрический момент диполя,
Общая энергия межмолекулярного взаимодействия выражается суммой энергий трех видов взаимодействия:
Еобщ = Еориент + Еинд +Едисп.
Вклад каждого из слагаемых определяется полярностью и поляризуемостью частиц. Во взаимодействие сильно полярных и легко поляризующихся молекул наибольший вклад вносят Еориент + Еинд, хотя значение Еинд обычно сравнительно невелико. У малополярных молекул дисперсионное взаимодействие выходит на первое место, а у неполярных оно является единственной составляющей.
§ 56. Силы взаимодействия молекул. Строение газообразных, жидких и твёрдых тел
Подумайте, можно ли объяснить свойства вещества во всех его агрегатных состояниях строением вещества, движением и взаимодействием его частиц.
Силы взаимодействия молекул. Молекулы взаимодействуют друг с другом. Без этого взаимодействия не было бы ни твёрдых, ни жидких тел.
Доказать существование значительных сил взаимодействия между атомами или молекулами несложно. Попробуйте-ка сломать толстую палку! А ведь она состоит из молекул. Но одни силы притяжения не могут обеспечить существования устойчивых образований из атомов и молекул. На очень малых расстояниях между молекулами обязательно действуют силы отталкивания. Благодаря этому молекулы не проникают друг в друга и куски вещества никогда не сжимаются до размеров порядка размеров одной молекулы.
Запомни
Молекула — это сложная система, состоящая из отдельных заряженных частиц: электронов и атомных ядер.
Важно
В целом молекулы электрически нейтральны, тем не менее между ними на малых расстояниях действуют значительные электрические силы: происходит взаимодействие электронов и атомных ядер соседних молекул.
Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не сказываются.
На расстояниях, превышающих 2—3 диаметра молекул, действуют силы притяжения. По мере уменьшения расстояния между молекулами сила их взаимного притяжения сначала увеличивается, но одновременно увеличивается и сила отталкивания. При определённом расстоянии r0 сила притяжения становится равной силе отталкивания. Это расстояние считается равным диаметру молекулы.
При дальнейшем уменьшении расстояния электронные оболочки атомов начинают перекрываться и быстро увеличивается сила отталкивания. На рисунке 8.5 показаны графики зависимости потенциальной энергии взаимодействия молекул (рис. 8.5, а) и сил притяжения (1) и отталкивания (2) (рис. 8.5, б) от расстояния между молекулами. При r = r0 потенциальная энергия минимальна, сила притяжения равна силе отталкивания. При r > r0 сила притяжения больше силы отталкивания; при r Важно
Газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объёма. Многочисленные удары молекул о стенки сосуда создают давление газа.
Молекулы газа с огромными скоростями — сотни метров в секунду — движутся в пространстве. Сталкиваясь, они отскакивают друг от друга в разные стороны подобно бильярдным шарам. Слабые силы притяжения молекул газа не способны удержать их друг возле друга.
В газах средняя кинетическая энергия теплового движения молекул больше средней потенциальной энергии их взаимодействия, поэтому часто потенциальной энергией взаимодействия молекул мы можем пренебречь.
Жидкости. Молекулы жидкости расположены почти вплотную друг к другу поэтому молекула жидкости ведёт себя иначе, чем молекула газа.
В жидкостях существует так называемый ближний порядок, т. е. упорядоченное расположение молекул сохраняется на расстояниях, равных нескольким молекулярным диаметрам.
Молекула колеблется около своего положения равновесия, сталкиваясь с соседними молекулами. Лишь время от времени она совершает очередной «прыжок», попадая в новое положение равновесия.
В положении равновесия сила отталкивания равна силе притяжения, т. е. суммарная сила взаимодействия молекулы равна нулю.
Молекулы жидкости находятся непосредственно друг возле друга. При уменьшении объёма силы отталкивания становятся очень велики. Этим и объясняется малая сжимаемость жидкостей.
Важно
Жидкости: 1) малосжимаемы; 2) текучи, т. е. не сохраняют своей формы.
Объяснить текучесть жидкостей можно так. Внешняя сила заметно не меняет числа перескоков молекул в секунду. Но перескоки молекул из одного оседлого положения в другое происходят преимущественно в направлении действия внешней силы. Вот почему жидкость течёт и принимает форму сосуда.
В жидкостях средняя кинетическая энергия теплового движения молекул сравнима со средней потенциальной энергией их взаимодействия. Наличие поверхностного натяжения доказывает, что силы взаимодействия молекул жидкостей существенны, и ими пренебрегать нельзя.
Твёрдые тела. Атомы или молекулы твёрдых тел, в отличие от атомов и молекул жидкостей, колеблются около определённых положений равновесия. По этой причине
Важно
твёрдые тела сохраняют не только объём, но и форму
В твёрдых телах средняя потенциальная энергия взаимодействия молекул много больше средней кинетической энергии их теплового движения.
Запомни
Если соединить центры положений равновесия атомов или ионов твёрдого тела, то получится правильная пространственная решётка, называемая кристаллической.
На рисунках 8.6 и 8.7 изображены кристаллические решётки поваренной соли и алмаза. Внутренний порядок в расположении атомов кристаллов приводит к правильным внешним геометрическим формам.
Ключевые слова для поиска информации по теме параграфа.
Строение газообразных, жидких и твёрдых тел
Вопросы к параграфу
1. Почему два свинцовых бруска с гладкими чистыми срезами слипаются, если их прижать друг к другу, а кусочки мела не слипаются?
2. Газ способен к неограниченному расширению. Почему существует атмосфера у Земли?
3. Чем различаются траектории движения молекул газа, жидкости и твёрдого тела? Нарисуйте примерные траектории молекул веществ, находящихся в этих состояниях.
Повторите материал главы 8 по следующему плану
1. Выпишите основные понятия и физические величины и дайте им определение.
2. Запишите основные формулы.
3. Укажите единицы физических величин и их выражение через основные единицы СИ.
4. Опишите опыты, подтверждающие основные закономерности.
Броуновское движение. Силы взаимодействия молекул
Урок 25. Физика 10 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Броуновское движение. Силы взаимодействия молекул»
Частицы вещества (атомы, молекулы и ионы) настолько малы, что увидеть их даже с помощью очень сильных оптических микроскопов не предоставляется возможным. Однако существует целый ряд явлений, которые подтверждают дискретность веществ. Одним из таких явлений является диффу́зия, о которой мы говорили с вами на прошлом уроке.
Но, пожалуй, самым убедительным явлением, доказывающим первые два положения МКТ, является броуновское движение.
Броуновским движением называется непрерывное хаотическое движение мельчайших твёрдых частиц, «взвешенных» в жидкости или газе.
«Взвешенными» частицами принято называть частицы, плотность вещества которых сравнима с плотностью среды, в которой они находятся. Броуновское движение было открыто в 1827 году английским ботаником Робертом Броуном (отсюда и название движения). Итак, в своих опытах Броун с помощью микроскопа изучал мелкие споры цветочной пыльцы плауна, помещённые в капельку воды.
Каково было его удивление, когда он заметил, что каждая частичка пыльцы (её называют броуновской) совершала причудливое зигзагообразное движение, которое не замедлялось ни на секунду. Вода в капле была неподвижна, так что объяснить движение частиц с завихрениями течений в капле не удалось. Поэтому учёный изначально приписал спорам пыльцы свойства живых существ.
Первоначально, как это часто бывало в мире науки, учёные не проявили никакого интереса к результатам опыта Броуна. Лишь в 1863 году немецкий математик Людвиг Кристиан Винер, обобщив результаты многочисленных опытов, предположил, что движение броуновской частицы связано с её столкновением с молекулами жидкости.
При беспорядочном движении молекул передаваемые ими броуновской частице импульсы с разных сторон неодинаковы. Поэтому отлична от нуля результирующая сила давления молекул жидкости на броуновскую частицу. Эта сила и вызывает изменение движения частицы.
Поразительно, но схожее объяснение в своей знаменитой поэме «О природе вещей» дал похожему явлению римский философ Тит Лукреций Кар (а это первый век до нашей эры). Мельчайшие невидимые глазом частицы он называет «Первоначалами» вещей….
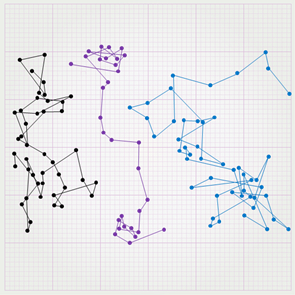
Но опять же, эти идеи были восприняты учёным миром в штыки. Лишь к концу XIX — началу ХХ веков учёные приняли тот факт, что броуновское движение вызвано соударением частицы с молекулами жидкости (или газа). Но все объяснения строились лишь на качественном уровне, пока в 1904)году польский физик Мариан Смолуховский и в мае 1905 года Альберт Эйнштейн смогли дать строгое объяснение и описать математической формулой движение броуновской частицы. В соответствии с теорией Смолухо́вского — Эйнште́йна, среднее значение квадрата смещения броуновской частицы за некоторый промежуток времени прямо пропорционально температуре и обратно пропорционально вязкости жидкости, размеру частицы и постоянной Авогадро:
Оказалось принципиально важным, что в эту формулу входит постоянная Авогадро, которую теперь можно было определить путём количественных измерений перемещения броуновской частицы.
В 1908 году французский физик Жан Батист Перрен на основании теории Смолуховского — Эйнштейна решил вычислить значение постоянной Авогадро. Для этого он получил однородную эмульсию из частичек гуммигута (это такая древесная смола), которую поместил на специальное предметное стекло с цилиндрическим углублением. Вся эта конструкция накрывалась покровным стеклом и помещалась под микроскоп. Наблюдая за броуновскими частицами в микроскоп, Перрен фиксировал положение некоторых из них через каждые 30 с и зарисовывал эти положения в масштабе на листе бумаги. Соединяя полученные точки прямыми, он получал замысловатые треки частиц. Обработав полученные результаты, Перрен доказал, что средний квадрат перемещения броуновской частицы пропорционален времени её движения.
В 1876 году Людвиг Больцман открыл закон распределения молекул воздуха в поле тяготения. Согласно ему, концентрация молекул газа в атмосфере убывает с высотой по экспоненциальному закону:
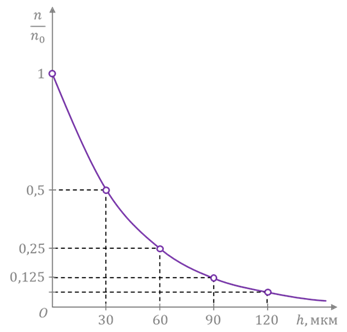
Для проверки этого закона Перрен подсчитал число частиц гуммигута в слоях раствора на разной высоте. Оказалось, что каждые 30 мкм число частиц, или лучше сказать, концентрация частиц уменьшалась почти вдвое. Это свидетельствовало как о справедливости полученного Больцманом закона распределения молекул атмосферного воздуха в поле тяготения, так и о применимости этого закона к распределению числа броуновских частиц по высоте.
Используя теоретическую формулу Больцмана и результаты своего эксперимента, он получил достаточно точное для того времени значение фундаментальной константы — постоянной Авогадро:
После публикации этих результатов большинство противников молекулярной теории строения вещества признали, что «совпадение броуновского движения с требованиями кинетической гипотезы. даёт теперь право самому осторожному учёному говорить об экспериментальном доказательстве атомистической теории материи».
Таким образом, открытие, сделанное Робертом Броуном, неоспоримо доказывает, что все вещества состоят из мельчайших частиц, которые находятся в непрерывном тепловом движении.
А теперь давайте с вами вспомним третье положение МКТ: между молекулами вещества существуют силы взаимодействия. Сам факт существования твёрдых и жидких тел говорит нам о том, что между частицами веществ существуют силы взаимного притяжения. Оно и понятно, не было бы притяжения — не было бы и тел.
С другой стороны, относительно малая сжимаемость жидкостей и твёрдых тел указывает нам на то, что между молекулами вещества существуют и силы отталкивания. В противном случае мы могли бы сжать любое тело до размеров молекулы.
Ну а то, что большинство тел обладают определёнными размерами и формой, говорит о том, что силы притяжения и отталкивания действуют одновременно.
И несмотря на то, что молекулы в целом электрически нейтральны, силы притяжения и отталкивания имеют электромагнитную природу, так как вызваны они взаимодействием электронов и атомных ядер соседних молекул.
График зависимости проекции равнодействующей сил притяжения и отталкивания от расстояния между их центрами:
Расстояние между центрами частиц, при котором силы притяжения уравновешиваются силами отталкивания, называют равновесным.
В различных агрегатных состояниях вещества расстояние между его молекулами различно. Отсюда и различие в силовом взаимодействии молекул и существенное различие в характере движения молекул газов, жидкостей и твёрдых тел.
Например, вы знаете, что расстояние между молекулами в газах достаточно велико (во много раз больше самих молекул). Поэтому силы взаимодействия между молекулами очень малы. Но вот скорости их движения достаточно велики (порядка нескольких сотен метров в секунду). Поэтому даже при редких (в масштабах молекул) столкновениях сил притяжения не хватает, чтобы удержать молекулы друг возле друга. Сталкиваясь, они разлетаются в разные стороны, подобно бильярдным шарам. Поэтому газы не сохраняют ни своей формы, ни объёма и могут неограниченно расширяться.
Всё это приводит к тому, что средняя кинетическая энергия теплового движения молекул газа намного больше средней потенциальной энергии их взаимодействия. Поэтому часто значением последней мы будем пренебрегать.
В жидкостях дела обстоят несколько иначе. Вы знаете, что молекулы жидкостей очень плотно упакованы и колеблются около своего положения равновесия, сталкиваются с соседними молекулами и иногда меняются с ними местами (они своего рода «кочевники»). Плотная упаковка молекул жидкости приводит к тому, что при попытках уменьшить объём жидкости силы межмолекулярного отталкивания резко возрастают. Это приводит к тому, что жидкости легко сохраняют свой объём, но при этом они не могут сохранить свою форму (то есть они текучи).
Текучесть жидкостей на пальцах можно объяснить так. Возьмём сосуд с водой и наклоним его так, чтобы жидкость смогла выливаться. На жидкость действует внешняя сила — сила тяжести. И хотя она не может заметно изменить число «перескоков» молекул с одного равновесного положения в другое, она указывает молекулам в каком направлении следует эти перескоки совершить — по линии действия внешней силы. Вот почему жидкость обладает текучестью и легко меняет свою форму, но не объём.
Что касается твёрдых тел, то в них силы взаимодействия между молекулами так велики, что кинетическая энергия теплового движения оказывается на несколько порядков меньше, чем потенциальная энергия взаимодействия. Поэтому молекулы могут совершать лишь колебания с очень маленькой амплитудой около своих положений равновесия — узлах кристаллической решётки. Это приводит к тому, что твёрдые тела, в отличие от жидкостей и тем более газов, сохраняют и свою форму, и свой объём.