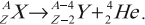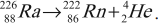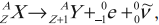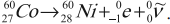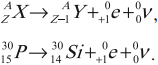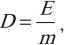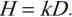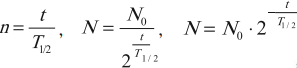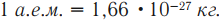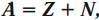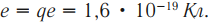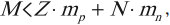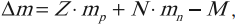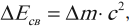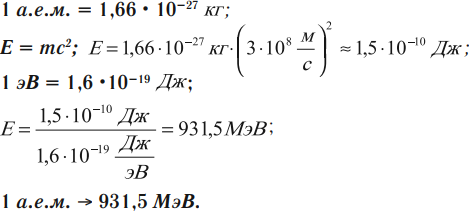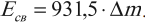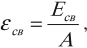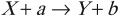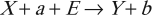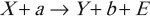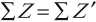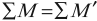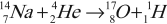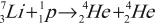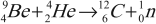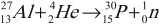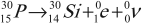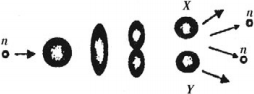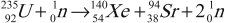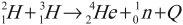какие силы действуют в атомном ядре
Какие силы действуют в атомном ядре
Ядерное взаимодействие свидетельствует о том, что в ядрах существуют особые ядерные силы, не сводящиеся ни к одному из типов сил, известных в классической физике (гравитационных и электромагнитных).
Ядерные силы являются короткодействующими силами. Они проявляются лишь на весьма малых расстояниях между нуклонами в ядре порядка 10 –15 м. Длина (1,5 – 2,2)·10 –15 м называется радиусом действия ядерных сил.
Ядерные силы обнаруживают зарядовую независимость: притяжение между двумя нуклонами одинаково независимо от зарядового состояния нуклонов – протонного или нейтронного. Зарядовая независимость ядерных сил видна из сравнения энергий связи зеркальных ядер. Так называются ядра, в которых одинаково общее число нуклонов, но число протонов в одном равно числу нейтронов другом. Например, ядра гелия 

Разность энергий связи ядер, равная 0,77 МэВ, соответствует энергии кулоновского отталкивания двух протонов в ядре 


Ядерные силы обладают свойством насыщения, которое проявляется в том, что нуклон в ядре взаимодействует лишь с ограниченным числом ближайших к нему соседних нуклонов. Именно поэтому наблюдается линейная зависимость энергий связи ядер от их массовых чисел A. Практически полное насыщение ядерных сил достигается у α-частицы, которая является очень устойчивым образованием.
Ядерные силы зависят от ориентации спинов взаимодействующих нуклонов. Это подтверждается различным характером рассеяния нейтронов молекулами орто- и параводорода. В молекуле ортоводорода спины обоих протонов параллельны друг другу, а в молекуле параводорода они антипараллельны. Опыты показали, что рассеяние нейтронов на параводороде в 30 раз превышает рассеяние на ортоводороде. Ядерные силы не являются центральными.
Итак, перечислим общие свойства ядерных сил:
· малый радиус действия ядерных сил (R
· большая величина ядерного потенциала U
· зависимость ядерных сил от спинов взаимодействующих частиц;
· тензорный характер взаимодействия нуклонов;
· ядерные силы зависят от взаимной ориентации спинового и орбитального моментов нуклона (спин-орбитальные силы);
· зарядовая независимость ядерных сил;
· обменный характер ядерного взаимодействия;
· притяжение между нуклонами на больших расстояниях (r > 1 Фм), сменяется отталкиванием на малых (r
Ядра атомов: в самом сердце материи

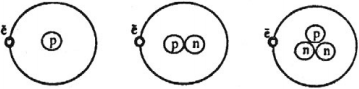
Рис. 1
Ядро атома получается крохотным, его радиус в 10 000–100 000 раз меньше всего атома. Каждое ядро содержит определённое количество протонов (обозначим его Z) и определённое количество нейтронов (обозначим его N), скреплённых вместе в виде шарика, по размеру не сильно превышающего сумму их размеров. Отметим, что протоны и нейтроны вместе часто называют «нуклонами», а Z+N часто называют A – общее количество нуклонов в ядре. Также Z, «атомное число» – количество электронов в атоме.
Типичное мультяшное изображение атома (рис. 1) чрезвычайно преувеличивает размер ядра, но более-менее правильно представляет ядро как небрежно соединённое скопление протонов и нейтронов.
Содержимое ядра
Откуда нам известно, что находится в ядре? Эти крохотные объекты просто охарактеризовать (и это было просто исторически) благодаря трём фактам природы.
1. Протон и нейтрон отличаются по массе всего лишь на тысячную часть, так что если нам не нужна чрезвычайная точность, можно сказать, что у всех нуклонов масса одинакова, и назвать её массой нуклона, mнуклон:
(≈ означает «примерно равно»)
2. Количество энергии, необходимой для удержания вместе протонов и нейтронов в ядре, относительно мало – порядка тысячной доли части энергии массы (E = mc 2 ) протонов и нейтронов, так что масса ядра почти равна сумме масс его нуклонов:
3. Масса электрона равняется 1/1835 массы протона – так что почти вся масса атома содержится в его ядре:
Тут подразумевается наличие четвёртого важного факта: все атомы определённого изотопа определённого элемента одинаковы, как и все их электроны, протоны и нейтроны.
Поскольку в самом распространённом изотопе водорода содержится один электрон и один протон:
масса атома Mатом определённого изотопа просто равна Z+N, помноженному на массу атома водорода
и погрешность этих уравнений примерно равна 0,1%.
Поскольку нейтроны электрически нейтральны, электрический заряд Qядро ядра просто равен количеству протонов, помноженному на электрический заряд протона («e»):
В отличие от предыдущих уравнений, это уравнение выполняется точно.
Эти уравнения проиллюстрированы на рис. 2

Рис. 2
Используя открытия последних десятилетий XIX века и первых десятилетий XX, физики знали, как измерить в эксперименте оба обозначенных красным значения: заряд ядра в e, и массу любого атома в атомах водорода. Так что эти значения были известны уже в 1910-х. Однако правильно интерпретировать их смогли только в 1932 году, когда Джеймс Чедвик определил, что нейтрон (идею которого предложил Эрнест Резерфорд в 1920-м) является отдельной частицей. Но как только стало понятно, что нейтроны существуют, и что их масса практически равна массе протона, сразу же стало ясно, как интерпретировать числа Z и N — количество протонов и нейтронов. А также сразу родилась новая загадка – почему у протонов и нейтронов почти одинаковая масса.
Честно говоря, физикам того времени с научной точки зрения страшно повезло, что всё это было так легко установить. Закономерности масс и зарядов настолько просты, что даже самые долгие загадки были раскрыты сразу после открытия нейтрона. Если бы хотя бы один из перечисленных мною фактов природы оказался неверным, тогда на то, чтобы понять, что происходит внутри атомов и их ядер, ушло бы гораздо больше времени.

Рис. 3
Откуда нам известно, что ядро атома маленькое?
Одно дело – убедить себя, что определённое ядро определённого изотопа содержит Z протонов и N нейтронов; другое – убедить себя, что ядра атомов крохотные, и что протоны с нейтронами, будучи сжатыми вместе, не размазываются в кашу и не разбалтываются в месиво, а сохраняют свою структуру, как подсказывает нам мультяшное изображение. Как это можно подтвердить?
Я уже упоминал, что атомы практически пусты. Это легко проверить. Представьте себе алюминиевую фольгу; сквозь неё ничего не видно. Поскольку она непрозрачная, вы можете решить, что атомы алюминия:
1. Настолько крупные, что между ними нет просветов,
2. Настолько плотные и твёрдые, что свет сквозь них не проходит.
Насчёт первого пункта вы будете правы; в твёрдом веществе между двумя атомами почти нет свободного пространства. Это можно наблюдать на изображениях атомов, полученных при помощи особых микроскопов; атомы похожи на маленькие сферы (краями которых служат края электронных облаков), и они довольно плотно упакованы. Но со вторым пунктом вы ошибётесь.

Рис. 4
Если бы атомы были непроницаемыми, тогда сквозь алюминиевую фольгу ничто не смогло бы пройти – ни фотоны видимого света, ни рентгеновские фотоны, ни электроны, ни протоны, ни атомные ядра. Всё, что вы направили бы в сторону фольги, либо застревало бы в ней, либо отскакивало бы – точно так же, как любой кинутый объект должен отскочить или застрять в гипсокартонной стенке (рис. 3). Но на самом деле электроны высокой энергии легко могут пройти через кусочек алюминиевой фольги, как и рентгеновские фотоны, высокоэнергетические протоны, высокоэнергетические нейтроны, высокоэнергетические ядра, и так далее. Электроны и другие частицы – почти все, если точнее – могут пройти через материал, не потеряв ни энергии, ни импульса в столкновениях с чем-либо, содержащимся внутри атомов. Лишь малая часть их ударится об атомное ядро или электрон, и в этом случае они могут потерять большую часть своей начальной энергии движения. Но большая часть электронов, протонов, нейтронов, рентгеновских лучей и всякого такого просто спокойно пройдут насквозь (рис. 4). Это не похоже на швыряние гальки в стену; это похоже на швыряние гальки в сетчатый забор (рис. 5).

Рис. 5
Чем толще фольга – к примеру, если складывать всё больше и больше листов фольги вместе – тем вероятнее частицы, запущенные в неё, столкнуться с чем-либо, потеряют энергию, отскочат, изменят направление движения или даже остановятся. То же было бы верно, если бы вы наслаивали одну за другой проволочные сетки (рис. 6). И, как вы понимаете, из того, насколько далеко средняя галька может проникнуть сквозь слои сетки и насколько велики разрывы в сетке, учёные могут подсчитать на основании пройденной электронами или атомными ядрами дистанции, насколько атом пустой.

Рис. 6
Посредством таких экспериментов физики начала XX века установили, что внутри атома ничто – ни атомное ядро, ни электроны – не может быть большим, чем одна тысячная миллионных миллионных долей метра, то есть в 100 000 раз меньше самого атома. То, что такого размера достигает ядро, а электроны по меньшей мере в 1000 раз меньше, мы устанавливаем в других экспериментах – например, в рассеянии высокоэнергетических электронов друг с друга, или с позитронов.
Чтобы быть ещё более точным, следует упомянуть, что некоторые частицы потеряют часть энергии в процессе ионизации, в котором электрические силы, действующие между летящей частицей и электроном, могут вырвать электрон из атома. Это дальнодействующий эффект, и столкновением на самом деле не является. Итоговая потеря энергии значительна для летящих электронов, но не для летящего ядра.
Вы можете задуматься над тем, похоже ли то, как частицы проходят сквозь фольгу, на то, как пуля проходить сквозь бумагу – расталкивая части бумаги в стороны. Возможно, первые несколько частиц просто расталкивают атомы в стороны, оставляя большие отверстия, через которые проходят последующие? Мы знаем, что это не так, поскольку мы можем провести эксперимент, в котором частицы проходят внутрь и наружу контейнера, сделанного из металла или стекла, внутри которого вакуум. Если бы частица, проходя через стенки контейнера, создавала отверстия по размеру превышающие атомы, тогда внутрь устремились бы молекулы воздуха, и вакуум бы исчез. Но в таких экспериментах вакуум остаётся!
Также довольно легко определить, что ядро – это не особенно структурированная кучка, внутри которой нуклоны сохраняют свою структуру. Об этом уже можно догадаться по тому факту, что масса ядра очень близка к сумме масс содержащихся в нём протонов и нейтронов. Это выполняется и для атомов, и для молекул – их массы почти равны сумме масс их содержимого, кроме небольшой коррекции на связывающую энергию – и это отражено в том факте, что молекулы довольно легко разбить на атомы (к примеру, нагрев их так, чтобы они сильнее сталкивались друг с другом), и выбить электроны из атомов (опять-таки, при помощи нагрева). Сходным образом относительно легко разбить ядра на части, и этот процесс будет называться расщеплением, или собрать ядро из более мелких ядер и нуклонов, и этот процесс будет называться синтезом. К примеру, относительно медленно двигающиеся протоны или небольшие ядра, сталкивающиеся с более крупным ядром, могут разбить его на части; нет необходимости, чтобы сталкивающиеся частицы двигались со скоростью света.

Рис. 7
Но чтобы понять, что это не является неизбежным, упомяну, что этими свойствами не обладают сами протоны и нейтроны. Масса протона не равняется примерной сумме масс содержащихся в нём объектов; протон нельзя разбить на части; а для того, чтобы протон продемонстрировал что-нибудь интересное, необходимы энергии, сравнимые с энергией массы самого протона. Молекулы, атомы и ядра относительно просты; протоны и нейтроны чрезвычайно сложны.
Физика атомного ядра
Радиоактивность. Альфа-распад. Бета-распад. Гамма-излучение
Радиоактивность – способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений.
Явление естественной радиоактивности открыл в 1896 году французский физик А. Беккерель. Проводя опыты с солями урана, он заметил, что они самопроизвольно испускают лучи неизвестной природы, которые проходят через бумагу, дерево, металлические пластины и делают воздух проводником электричества.
Радиоактивность данного химического элемента не зависит от того, является ли химический элемент чистым или входит в состав какоголибо химического соединения. Радиоактивность не зависит от внешних условий: температуры, освещения, давления. Это означает, что радиоактивность представляет собой внутреннее свойство атомов радиоактивного элемента.
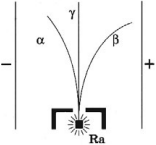
Виды радиоактивных излучений
Излучение радиоактивных веществ имеет сложный характер и состоит из трех видов излучений. Если радиоактивное излучение пропустить через электрическое и магнитное поля, то оно распадается на три части, две из них отклоняются в противоположные стороны, а третий не отклоняется.
При одинаковой энергии частиц разные виды излучений неодинаково взаимодействуют с веществом.
Радиоактивный распад – самопроизвольный распад атомов радиоактивного вещества, в результате которого ядра одних химических элементов превращаются в ядра других химических элементов.
Распадающееся ядро Х называется материнским ядром, ядро продукта распада Y – дочерним ядром.
Правила радиоактивного смещения
Это правила, позволяющие установить, какое ядро возникает в результате распада данного материнского ядра.
\( \gamma \) -излучение сопровождает \( \alpha \) - и \( \beta \) -распады, а также возникает при ядерных реакциях, торможении частиц, их распаде и т. д.
Биологическое действие радиоактивных излучений
Методы защиты от внешнего радиоактивного облучения:
Методы защиты от внутреннего радиоактивного облучения:
В дозиметрии различают поглощенную и эквивалентную дозы.
Поглощенная доза равна энергии радиоактивного излучения, поглощенного единицей массы вещества.
Обозначение – \( D \) , единица измерения в СИ – грей (Гр).
где \( E \) – энергия излучения; \( m \) – масса вещества.
Для характеристики биологического воздействия на организм используется коэффициент качества излучения \( (k) \) , или коэффициент относительной биологической активности.
\( k \) = 1 для \( \gamma \) -квантов, \( k \) = 3 для тепловых нейтронов, \( k \) = 10 для нейтронов с энергией порядка 0,5 МэВ.
Эквивалентная доза равна произведению коэффициента качества излучения и поглощенной дозы.
Обозначение – \( H \) , единица измерения в СИ – зиверт (Зв).
1 зиверт – это эквивалентная доза, при которой поглощенная доза равна 1 Гр при коэффициенте качества, равном 1.
Естественный фон составляет 2 мЗв за год.
Предельно допустимая доза – 5 мЗв за год.
При дозе 0,5 Зв наступает острое лучевое поражение организма.
Допустимая доза облучения за среднее время жизни человека (70 лет) составляет 0,35 Зв.
Закон радиоактивного распада
Если имеется большое количество одинаковых радиоактивных ядер, то вероятность распада каждого из них в любой момент времени одинакова. Радиоактивный распад любого ядра является случайным процессом, поэтому момент его распада предсказать невозможно.
Однако для большого числа частиц, находящихся в образце вещества, выполняется статистический закон радиоактивного распада.
Закон радиоактивного распада:
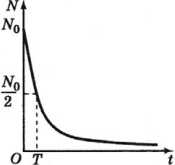
число нераспавшихся атомных ядер при естественном радиоактивном распаде экспоненциально уменьшается с течением времени.
Период полураспада – это время, в течение которого распадается половина способных к распаду ядер.
В начальный момент времени \( t \) = 0, число атомных ядер \( N_0 \) .
Через промежуток времени, равный периоду полураспада \( t=T_ <1>\) , число атомных ядер \( N=\frac
где \( N \) – число нераспавшихся атомных ядер к моменту времени \( t \) ; \( N_0 \) – начальное число атомных ядер; \( T_ <1>\) – период полураспада.
На рисунке период полураспада соответствует времени, в течение которого число радиоактивных ядер (активность) уменьшается вдвое.
Нуклонная модель ядра. Заряд ядра. Массовое число ядра
Элементарные частицы:
Нуклон – это частица, входящая в состав атомного ядра.
Атомное ядро любого химического элемента состоит из протонов и нейтронов.
Массовое число – это число, которое определяет количество протонов и нейтронов в ядре и равно округленному до целого значению массы атомного ядра в а.е.м.
Обозначение – \( A \) , единица измерения – 1 атомная единица массы (а.е.м.).
Массовое число равно сумме количества протонов и нейтронов в ядре:
где \( A \) – массовое число; \( Z \) – количество протонов в ядре; \( N \) – количество нейтронов в ядре.
Зарядовое число – это число, которое показывает количество протонов в ядре.
Зарядовое число равно сумме зарядов протонов, входящих в состав ядра, выраженной в элементарных электрических зарядах.
Элементарный электрический заряд равен заряду электрона:
\( Z \) – порядковый номер химического элемента в периодической таблице Менделеева.
Если некоторый химический элемент обозначить \( <>^A_ZX \) , это означает, что в его ядре \( Z \) – протонов и \( N=A-Z \) – нейтронов.
Измерения массы атомов показали, что практически все химические элементы имеют изотопы.
Изотопы – это атомы одного и того же химического элемента, имеющие одинаковое количество протонов, но отличающиеся количеством нейтронов в ядре.
Изотопы водорода: водород имеет два стабильных изотопа – водород \( <>^1_1H \) , дейтерий \( <>^2_1H \) и один радиоактивный изотоп тритий \( <>^3_1H \) .
Энергия связи нуклонов в ядре. Ядерные силы
Между нуклонами ядра действуют самые мощные силы природы – ядерные силы.
Ядерные силы – это силы притяжения, связывающие протоны и нейтроны в атомном ядре и обеспечивающие существование устойчивых ядер.
Свойства ядерных сил:
Массу ядра можно точно определить с помощью масс-спектрографов, которые разделяют заряженные частицы с разными удельными зарядами с помощью электрических и магнитных полей.
Опытным путем было установлено, что благодаря действию сил притяжения масса ядра всегда меньше суммы масс протонов и масс нейтронов, входящих в состав этого ядра:
где \( M \) – масса ядра.
Дефект масс – это величина, равная разности суммы масс входящих в ядро нуклонов и массы ядра:
где \( \Delta m \) – дефект масс.
Благодаря ядерным силам ядра атомов обладают огромной энергией связи.
Энергия связи – это энергия, которую необходимо затратить, чтобы разделить ядро на составляющие его нуклоны, или энергия, которая выделяется при образовании ядра из отдельных нуклонов:
где \( \Delta E_ <св>\) – энергия связи, \( c \) – скорость света.
Если в формуле энергии связи массы протона и нейтрона выражены в килограммах, а скорость света – в метрах в секунду, то энергия связи будет измерена в джоулях. Однако в физике атома и атомного ядра энергию ядер и элементарных частиц чаще выражают в мегаэлектронвольтах (МэВ).
Энергетический эквивалент 1 а.е.м.
Поэтому энергию связи можно рассчитать следующим образом:
В этом случае энергия связи измеряется в мегаэлектронвольтах (МэВ).
Для характеристики прочности ядра используется величина, которая называется удельной энергией связи.
Удельная энергия связи – это энергия связи ядра, приходящаяся на один нуклон ядра:
где \( A \) – массовое число.
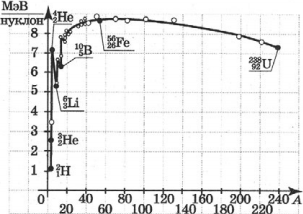
Удельная энергия связи неодинакова для разных химических элементов и даже для изотопов одного и того же химического элемента. Удельная энергия связи нуклона в ядре меняется в среднем в пределах от 1 МэВ у легких ядер до 8,6 МэВ у ядер средней массы (с массовым числом \( A \) ≈ 100). У тяжелых ядер ( \( A \) ≈ 200) удельная энергия связи нуклона меньше, чем у ядер средней массы, приблизительно на 1 МэВ, так что их превращение в ядра среднего веса (деление на 2 части) сопровождается выделением энергии в количестве около 1 МэВ на нуклон, или около 200 МэВ на ядро. Превращение легких ядер в более тяжелые ядра дает еще больший энергетический выигрыш в расчете на нуклон.
Зависимость удельной энергии связи от массового числа установили экспериментально. Из рисунка хорошо видно, что, не считая самых легких ядер, удельная энергия связи примерно постоянна и равна 8 МэВ/нуклон. Отметим, что энергия связи электрона и ядра в атоме водорода, равная энергии ионизации, почти в миллион раз меньше этого значения. Кривая на рисунке имеет слабо выраженный максимум. Максимальную удельную энергию связи (8,6 МэВ/нуклон) имеют элементы с массовыми числами от 50 до 60, т. е. железо и близкие к нему по порядковому номеру элементы. Ядра этих элементов наиболее устойчивы.
У тяжелых ядер удельная энергия связи уменьшается за счет возрастающей с увеличением \( Z \) кулоновской энергии отталкивания протонов. Кулоновские силы стремятся разорвать ядро.
Ядерные реакции. Деление и синтез ядер
Атомные ядра при взаимодействиях испытывают превращения. Эти превращения сопровождаются увеличением или уменьшением кинетической энергии участвующих в них частиц.
Ядерные реакции – это изменения атомных ядер при взаимодействии их с элементарными частицами или друг с другом.
Ядерные реакции происходят, когда частицы вплотную приближаются к ядру и попадают в сферу действия ядерных сил. Одноименно заряженные частицы отталкиваются друг от друга, поэтому сближение положительно заряженных частиц с ядрами (или ядер друг с другом) возможно, если этим частицам (или ядрам) сообщена достаточно большая кинетическая энергия. Эта энергия сообщается протонам, ядрам дейтерия, α-частицам и другим более тяжелым ядрам с помощью ускорителей.
Для осуществления ядерных реакций такой метод гораздо эффективнее, чем использование ядер гелия, испускаемых радиоактивными элементами. Во-первых, с помощью ускорителей частицам может быть сообщена энергия порядка 105 МэВ, т. е. гораздо большая той, которую имеют \( \alpha \) -частицы (максимально 9 МэВ). Во-вторых, можно использовать протоны, которые в процессе радиоактивного распада не появляются (это целесообразно потому, что заряд протонов вдвое меньше заряда α-частиц, и поэтому действующая на них сила отталкивания со стороны ядер тоже в 2 раза меньше). В-третьих, можно ускорить ядра более тяжелые, чем ядра гелия.
Наиболее распространенный вид ядерной реакции:
где \( X \) и \( Y \) – исходное и конечное ядра; \( a \) и \( b \) – бомбардирующая и испускающая частицы.
Эндотермическая реакция – это реакция с поглощением энергии:
Экзотермическая реакция – это реакция с выделением энергии:
При ядерных реакциях выполняются следующие законы.
Примеры ядерных реакций
Изотоп фосфора оказался радиоактивным: его ядро распадается с испусканием позитрона и нейтрино:
Классификация ядерных реакций
Ядерные реакции классифицируются:
Деление ядер – это деление атомного ядра урана на несколько более легких ядер (осколков), чаще всего на два ядра, близких по массе.
Механизм деления ядер (капельная модель)
В тяжелых ядрах действуют значительные ядерные силы, которые удерживают ядро от распада. Под влиянием поглощенного нейтрона ядро возбуждается и начинает деформироваться, приобретая вытянутую форму. Оно растягивается до тех пор, пока силы отталкивания половинок ядра не начинают преобладать над силами притяжения, действующими в перешейке. В результате ядро разрывается на два осколка X и Y.
Под действием сил кулоновского отталкивания осколки разлетаются со скоростью, равной приблизительно 1/30 скорости света. Одновременно испускается излучение высокой частоты.
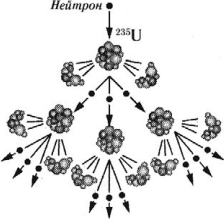
В 1939 году было обнаружено, что при попадании нейтрона в ядро изотопа урана-235 происходит деление ядра на два или три осколка с испусканием 2–3 нейтронов:
Эти нейтроны способны вызвать деление 2–3 новых ядер урана с испусканием 4–9 новых нейтронов и т. д., процесс может продолжаться самостоятельно, вовлекая все большее число новых ядер.
Условия протекания цепной ядерной реакции:
Минимальное количество вещества, необходимое для осуществления цепной ядерной реакции, называется критической массой.
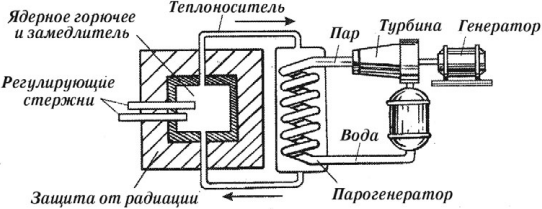
Устройства, в которых осуществляются управляемые цепные ядерные реакции, называются ядерными реакторами.
Основные элементы ядерного реактора:
Термоядерный синтез
График зависимости удельной энергии связи нуклонов в ядре от массового числа показывает, что кроме реакции деления тяжелых ядер с выделением энергии идут реакции синтеза легких ядер.
Синтез ядер – это слияние ядер в одно ядро, сопровождающееся выделением энергии.
Для осуществления реакции синтеза легких ядер требуются высокие энергии сливающихся частиц, так как необходимо преодолеть кулоновское отталкивание. Этого можно достичь за счет высокой температуры вещества.
Термоядерная реакция – это реакция синтеза легких атомных ядер в более тяжелые, происходящая при сверхвысоких температурах (порядка 10 7 К и выше).
В природе термоядерные реакции происходят в недрах звезд.
При термоядерном синтезе энергетический выход на единицу массы топлива оказывается выше, чем при реакции деления тяжелых ядер урана.
Пример реакции синтеза:
Синтез гелия из тяжелых изотопов водорода – дейтерия и трития – происходит при температуре около 5·10 7 К.
При синтезе 1 г гелия из дейтерия и трития выделяется 4,2·10 11 Дж – такая же энергия выделяется при сгорании 10 т дизельного топлива.
Термоядерный синтез может стать одним из возможных альтернативных источников энергии. Поиск таких источников энергии важен, так как запасы нефти и газа на Земле ограничены.
В настоящее время ведется испытание установок для осуществления управляемых термоядерных реакций синтеза гелия из водорода. Запасы водорода на Земле практически неисчерпаемы. Количество дейтерия в океанической воде составляет примерно 4·10 11 т, чему соответствует энергетический запас 10 17 МВт·год. Наиболее заманчивой является возможность извлечения энергии дейтерия, содержащегося в обычной воде.