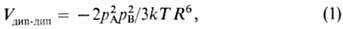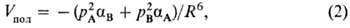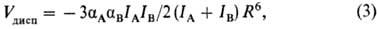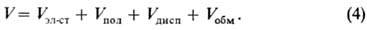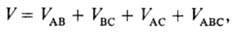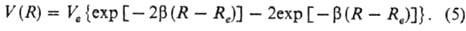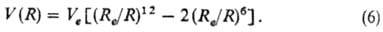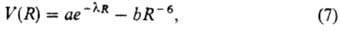какие существуют типы межмолекулярного взаимодействия
Виды межмолекулярных взаимодействий
Введение
Центральным понятием химии является химическая связь. Связи в молекулах органических веществ бывают ионными и ковалентными. Но помимо них существуют и другие формы взаимодействия, которые сильно влияют на физические свойства и реакционную способность веществ.
Цель:рассмотреть слабые межмолекулярные взаимодействия в органических соединениях.
1. Что такое межмолекулярные взаимодействия в органических соединениях.
2. Рассмотреть виды слабых межмолекулярных взаимодействий.
3. Привести примеры таких взаимодействий.
4. Сделать вывод о том, как влияют слабые межмолекулярные взаимодействия на химические и физические свойства органических соединений.
Понятие о межмолекулярном взаимодействии
Виды межмолекулярных взаимодействий
1.1 Ориентационное (или диполь-дипольное) взаимодействие – характеризуется взаимной ориентацией разноименнозаряженных полюсов полярных молекул при их приближении друг к другу Энергия такого взаимодействия определяется электрическим дипольным моментом молекул. Чем выше дипольный момент и меньше расстояние между молекулами, тем больше энергия взаимодействия.
1.2 Поляризационное (индукционное) взаимодействие– Обусловлено электростатическим взаимодействием полярной и неполярной молекул. Полярная молекула своим полем воздействует на неполярную, в результате чего появляется наведенный (индуцированный) диполь, способный притягиваться к диполю полярной молекулы. Индуцированный диполь усиливает дипольный момент полярной молекулы. Энергия такого взаимодействия определяется электрическим диполем полярной молекулы и поляризуемостью неполярной молекулы.
1.3 Дисперсионное взаимодействие – появляется, как результат притяжения мгновенных диполей (микродиполей). Такие диполи появляются, если не совпадают электрические центры тяжести электронного облака и ядер, что вызвано их независимыми колебаниями. Одновременное появление и исчезновение микродиполей молекул сопровождается их притяжением. Если синхронность отсутствует, происходит отталкивание. Дисперсионное взаимодействие может проявляться между любыми молекулами, а потому является универсальным.
Примеры межмолекулярных взаимодействий в органических соединениях.
2) Индукционное взаимодействие:
3) Ориентационное (или диполь-дипольное) взаимодействие:
4) Дисперсионное взаимодействие:
Вывод
В данном реферате я изучила явление межмолекулярного взаимодействия, рассмотрела виды межмолекулярного взаимодействия. Выяснила, как влияют межмолекулярные взаимодействия на физические свойства соединений, например, диполь-дипольное притяжение обусловливает втягивание молекул воды с поверхности внутрь жидкости. Это объясняет существование вогнутого мениска воды в стеклянном стакане, а также сферическую форму капель воды. Водородная связь в некоторых соединениях объясняет аномально высокие значения их температур плавления и кипения. Ярким примером индукционного влияния у спиртов служит различие свойств триметилкарбинола и трифторметилдиметилкарбинола:
В то время как первый представляет собой один из наименее кислых спиртов, второй является кислотой, вытесняющей угольную кислоту из ее солей. Ван-дер-ваальсовы силы оказывают значительное влияние на многие физические свойства веществ (теплоту испарения жидкости либо теплоту возгонки кристалла, температуры плавления и кипения), а также на количественные характеристики некоторых химических реакций: тепловой эффект и энергию активации (температура активации либо минимальная для активизации реакции частота излучения) образования и диссоциации молекулярных комплексов, молекул и сложных ионов.
Типы межмолекулярных взаимодействий



Связи, при образовании которых перестройка электронных оболочек не происходит, называются взаимодействием между молекулами. К основным видам взаимодействия молекул следует отнести вандерваальсовы силы, водородные связи и донорно-акцепторное взаимодействие.
При сближении молекул появляется притяжение, что обуславливает возникновение конденсированного состояния вещества (жидкого, твердого с молекулярной кристаллической решеткой). Силы, которые способствуют притяжению молекул, получили название вандерваальсовых. Они характеризуются тремя видами межмолекулярного взаимодействия:
а) ориентационное взаимодействие, которое проявляется между полярными молекулами, стремящимися занять такое положение, при котором их диполи были бы обращены друг к другу разноименными полюсами, а векторы моментов этих диполей были бы ориентированы по одной прямой (по-другому оно называется диполь-дипольное взаимодействие);
б) индукционное, которое возникает между индуцированными диполями, причина образования которых является взаимная поляризация атомов двух сближающихся молекул;
в) дисперсионное, которое возникает в результате взаимодействия микродиполей, образующихся за счет мгновенных смещений положительных и отрицательных зарядов в молекулах при движении электронов и колебаний ядер.
Дисперсионные силы действуют между любыми частицами. Ориентационное и индукционное взаимодействие для частиц многих веществ, например: He, Ar, H2, N2, CH4, не осуществляется. Для молекул NH3 на дисперсионное взаимодействие приходится 50 %, на ориентационное – 44,6 % и на индукционное – 5,4 %. Полярная энергия вандерваальсовых сил притяжения характеризуется невысокими значениями. Так, для льда она составляет 11 кДж/моль, т.е. 2,4 % энергии ковалентной связи H-O (456 кДж/моль). Вандерваальсовы силы притяжения – это физические взаимодействия.
Водородная связь – это физико-химическая связь между водородом одной молекулы и ЭО элементом другой молекулы. Образование водородных связей объясняется тем, что в полярных молекулах или группах поляризованный атом водорода обладает уникальными свойствами: отсутствием внутренних электронных оболочек, значительным сдвигом электронной пары к атому с высокой ЭО и очень малым размером. Поэтому водород способен глубоко внедряться в электронную оболочку соседнего отрицательно поляризованного атома. Как показывают спектральные данные, в образовании водородной связи существенную роль играет также и донорно-акцепторное взаимодействие ЭО атома как донора и атома водорода как акцептора. Водородная связь может быть межмолекулярной или внутримолекулярной.
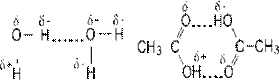 |
| Водородная связь изображена точками |
Если водородные связи образуются внутри молекул, то понижается вязкость, температура кипения и плавления, эти вещества боле летучи, не образуют ассоциаты, водородные связи внутри молекул приводят к поперечному сливанию цепочечных молекул. Таким образом, водородная связь занимает промежуточное положение между ковалентной и вандерваальсовой силами притяжения.
Донорно-акцепторное взаимодействие, как отмечалось ранее, приводит к образованию ковалентной полярной связи, т.е. относится к химическим видам взаимодействия. Донорно-акцепторное взаимодействие объясняет образование комплексных соединений. Например, при взаимодействии сульфата меди и аммиака образуется сложное соединение:
которое выражается формулой [Сu(NH3)4]SO4. Сложные соединения, у которых имеются ковалентные связи, образованные по донорно-акцепторному механизму, получили название комплексных или координационных соединений.
Таким образом, имеется обширный класс соединений, называемых комплексными, в которых существуют ковалентные связи, образованные по донорно-акцепторному механизму между центральным атомом или ионом (комплексообразователем-акцептором) и координируемыми им лигандами, имеющими неподеленные пары электронов (донорами).
Виды межмолекулярного взаимодействия твердых тел
Межмолекулярное взаимодействие в химии, суть процесса
Различные атомы и группы атомов, входящие в состав молекулы вещества могут осуществлять внутримолекулярное и межмолекулярное взаимодействие, приводящее к образованию нового типа связей — межмолекулярных связей.
Межмолекулярным называют взаимодействие частиц (атомов, молекул или ионов), проявляющееся на расстояниях, значительно превышающих размеры этих частиц.
Данное явление объясняет отличие идеальных газов от реальных, нахождение одних и тех же веществ в разных агрегатных состояниях и влияет на такие физические свойства, как плотность, электро- и теплопроводность, температура кипения и плавления, твердость и другие.
Первым понятие межмолекулярного взаимодействия ввел голландский ученый Йоханнес Дидерик ван-дер-Ваальс в 1873 году, когда изучал свойства реальных газов и жидкостей. Поэтому силы, обеспечивающие межмолекулярное взаимодействие, также называют ван-дер-ваальсовыми силами.
Отличия межмолекулярного взаимодействия от химической связи:
Основные виды межмолекулярного взаимодействия
Ван-дер-ваальсовы взаимодействия (силы) имеют электростатический характер и образуются за счет диполей (молекул, содержащих два одинаковых по величине, но разных по знаку заряда, находящимися на расстоянии друг от друга). В зависимости от вещества механизм образования диполей различен, поэтому выделяют три составляющие ван-дер-ваальсовых сил:
Влияние агрегатного состояния вещества на ван-дер-ваальсовы взаимодействия
Атомы или молекулы газообразных веществ постоянно двигаются в разных направлениях, поэтому большую часть времени находятся на значительных (по сравнению с собственными размерами) расстояниях друг от друга. Силы межмолекулярного взаимодействия между ними настолько малы, что его даже не учитывают, кроме тех случаев, когда газ находится под высоким давлением.
Частицы веществ в конденсированном состоянии (жидком или твердом) находятся ближе друг к другу, а силы взаимодействия достаточно велики для того, чтобы удержать их в таком положении. Поэтому жидкие и твердые вещества имеют, в отличие от газов, постоянный при данной температуре объем.
Для твердых тел (кристаллов) силы межмолекулярного взаимодействия обеспечивают сохранение не только объема, но и формы. Правильная геометрическая форма (кристаллическая решетка), в узлах которой находятся электрически нейтральные частицы, называется молекулярным кристаллом.
Для некоторых твердых тел свойственно наличие сразу нескольких видов связи. Примером такого вещества является графит с гексагональной решеткой:
Мягкость графита и скольжение его слоев друг относительно друга обусловлена этими факторами.
Водородная связь — частный случай ориентационных межмолекулярных сил, образующихся между положительно поляризованным атомом водорода одной группы или молекулы и отрицательно поляризованным атомом другой. Функцию отрицательного полюса выполняет атом с высокой отрицательностью (кислород, фтор, азот и др.).
Если представить соединение с формулой X-H, то водородная связь будет выглядеть так: X-H⋅⋅⋅Y (или H⋅⋅⋅Y), где Y — атом с высокой отрицательностью, входящий в состав какого либо вещества, образующего с X-H водородные связи.
В силу высокой прочности (сравнительно с другими вариантами межмолекулярного взаимодействия), широкой распространенности и важности в объяснении свойств различных соединений водородная связь рассматривается как отдельный тип межмолекулярных связей.
Значение водородной связи:
Водородные связи могут быть как внутримолекулярными (образуются между фрагментами одной молекулы), так и межмолекулярными (возникают между частями разных молекул).
Энергия межмолекулярного взаимодействия молекул
Энергия ориентационного взаимодействия Еориент растет при увеличении дипольных моментов частиц, уменьшается при повышении температуры.
Энергия индукционного взаимодействия Еинд увеличивается с ростом дипольного момента полярной молекулы и с увеличением поляризуемости неполярной. Не зависит от температуры.
Энергия дисперсионного взаимодействия Едисп пропорциональна квадрату поляризуемости частиц. Низкая поляризуемость характерна для многих соединений фтора, следовательно, они проявляют слабое дисперсионное взаимодействие. Доказательством этого является сравнительная таблица 1 температур кипения соединений фтора и хлора, похожих по строению:
| CF4 | CCl4 | OF2 | OCl2 | |
| tкип, °C | -128 | 76 | -144 | 3,8 |
Электрический момент диполя,
Общая энергия межмолекулярного взаимодействия выражается суммой энергий трех видов взаимодействия:
Еобщ = Еориент + Еинд +Едисп.
Вклад каждого из слагаемых определяется полярностью и поляризуемостью частиц. Во взаимодействие сильно полярных и легко поляризующихся молекул наибольший вклад вносят Еориент + Еинд, хотя значение Еинд обычно сравнительно невелико. У малополярных молекул дисперсионное взаимодействие выходит на первое место, а у неполярных оно является единственной составляющей.
Межмолекулярное взаимодействие
Из Википедии — свободной энциклопедии
Межмолекулярное взаимодействие — взаимодействие между молекулами и/или атомами, не приводящее к образованию ковалентных (химических) связей.
Межмолекулярное взаимодействие имеет электростатическую природу. Предположение о его существовании было впервые использовано Я. Д. Ван-дер-Ваальсом в 1873 году для объяснения свойств реальных газов и жидкостей. В наиболее широком смысле под ним можно понимать такие взаимодействия между любыми частицами (молекулами, атомами, ионами), при которых не происходит образования химических, то есть ионных, ковалентных или металлических связей. Иными словами, эти взаимодействия существенно слабее ковалентных и не приводят к существенной перестройке электронного строения взаимодействующих частиц.
На больших расстояниях преобладают силы притяжения, которые могут иметь ориентационную, поляризационную (индукционную) и дисперсионную природу (см. подробнее в статьях Силы Ван-дер-Ваальса и Дисперсионные силы). При усреднении по вращению частиц, происходящему вследствие теплового движения, потенциал межмолекулярных сил обратно пропорционален шестой степени расстояния, а ион-дипольных (как с постоянным, так и с наведенным диполем) — четвёртой степени. На малых расстояниях начинают преобладать силы отталкивания электронных оболочек частиц. Особым случаем является водородная связь — возникающее на малом расстоянии взаимодействие между атомом водорода одной молекулы и электроотрицательным атомом другой, когда эти атомы несут достаточно большой эффективный заряд.
Упаковку частиц и расстояние между ними в конденсированной фазе, определяющиеся равновесием между притяжением и отталкиванием, можно предсказать, исходя из ван-дер-ваальсовых радиусов составляющих молекулы атомов (ионных в случае ионов): расстояния между атомами разных молекул не должны превышать суммы радиусов этих атомов. Для моделирования межмолекулярных взаимодействий используют эмпирические потенциалы, среди которых наиболее известны потенциалы Леннард-Джонса (отталкивание описывается двенадцатой степенью обратного расстояния, притяжение — шестой) и Бакингема (с более физически обоснованным экспоненциальным отталкиванием), из которых первый более удобен для расчетов. В конденсированной фазе, где мультипольное разложение для молекул плохо применимо из-за близости молекул друг к другу, может применяться метод атом-атомных потенциалов, основанный на тех же потенциалах, но уже для парных взаимодействий атомов и с добавкой кулоновских членов, описывающих взаимодействие их эффективных зарядов.
МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ
МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ, взаимод. молекул между собой, не приводящее к разрыву или образованию новых хим. связей. Межмолекулярное взаимодействие определяет отличие реальных газов от идеальных, существование жидкостей и мол. кристаллов. От межмолекулярного взаимодействия зависят мн. структурные, спектральные, термодинамич., теплофиз. и др. св-ва в-в. Появление понятия межмолекулярного взаимодействия связано с именем Й. Д. Ван-дер-Ваальса, к-рый для объяснения св-в реальных газов и жидкостей предложил в 1873 ур-ние состояния, учитывающее межмолекулярное взаимодействие (см. Ван-дер-Ваальса уравнение). Поэтому силы межмолекулярного взаимодействия часто называют ван-дер-ваальсовыми.
Виды межмолекулярного взаимодействия. Основу межмолекулярного взаимодействия составляют кулоновские силы взаимод. между электронами и ядрами одной молекулы и ядрами и электронами другой. В экспериментально определяемых св-вах в-ва проявляется усредненное взаимод., к-рое зависит от расстояния R между молекулами, их взаимной ориентации, строения и физ. характеристик (ди-польного момента, поляризуемости и др.). При больших R, значительно превосходящих линейные размеры l самих молекул, вследствие чего электронные оболочки молекул не перекрываются, силы межмолекулярных взаимодействий можно достаточно обоснованно подразделить на три вида-электростатические, поляризационные (индукционные) и дисперсионные. Электростатич. силы иногда называют ориентационными, однако это неточно, поскольку взаимная ориентация молекул может обусловливаться также и поляризац. силами, если молекулы анизотропны.
При малых расстояниях между молекулами (R
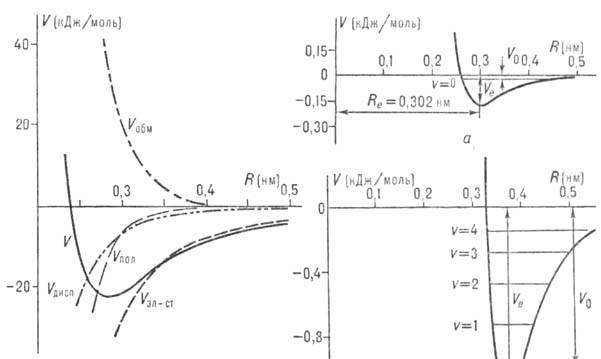
П о л я р и з а ц и о н н о е в з а и м о д е й с т в и е обусло влено деформацией электронной оболочки одной молекулы под влиянием электрич. поля другой, что всегда приводит к понижению энергии (притяжению молекул). При больших расстояниях между нейтральными молекулами главный вклад в поляризац. энергию V пол дает взаимод. постоянного диполя полярной молекулы с индуцированным диполем другой. Поэтому это взаимод. иногда называют индукционным. Согласно ф-ле Дебая,
Дисперсионное межмолекулярное взаимодействие определяется корреляцией движения электронов двух взаимодействующих молекул, в результате чего среднее расстояние между электронами этих молекул несколько увеличивается. Это приводит к уменьшению энергии их взаимодействия, т.е. к притяжению молекул. Дисперсионное взаимод. имеет универсальный характер: оно существует между любыми молекулами. Энергия дисперсионного взаимод. V дисп двух атомов или сферически симметричных молекул при R>>l приближенно описывается ф-л о й Л о н д о н а:
Энергия о б м е н н о г о в з а и м о д е й с т в и я молекул V обм обусловлена тем, что в соответствии с принципом Паули в одном и том же квантовом состоянии не могут находиться два электрона с одинаковыми спинами. Вследствие этого электронная плотность в пространстве между молекулами при перекрывании их электронных оболочек уменьшается (подробнее см. Обменное взаимодействие).
Полная энергия межмолекулярного взаимодействия, или межмолекулярный потенциал, V приблизительно равняется сумме вкладов отдельных видов межмолекулярного взаимодействия:
При R >> l последний член обращается в нуль, а первые три можно вычислить по ф-лам (1)-(3). При малых расстояниях между молекулами эти ф-лы, строго говоря, не пригодны для количеств. определения V, однако во мн. случаях они дают правильную качеств. картину межмолекулярного взаимодействия. Если обе или одна из молекул имеет электрич. заряд, то ф-ла (4) остается в силе, однако каждое слагаемое изменится и будет отражать действие дополнит. заряда одной молекулы на другую.
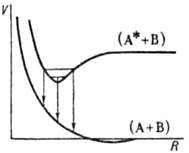
Мол. комплексы образуются и при т. наз. резонансном взаимодействии. Оно возникает, как правило, между одинаковыми молекулами, если сначала (при R >> R e )одна из них находится в возбужденном состоянии, а другая-в основном состоянии. При сближении молекул возникают два возбужденных уровня энергии, смещенных в разные стороны по отношению к энергии исходного возбужденного состояния. Величину этого сдвига называют резонансной энергией. Энергия ниж. уровня часто имеет минимум при нек-ром R, что соответствует образованию квазиравновесного комплекса (димера) в возбужденном состоянии (рис. 3).
Рис. 3. Кривые потенциальной энергии V для эксимера; (А + В)-основное состояние, (А* + В)-первое электрон но-возбужденное состояние. Стрелки указывают пути излучат. перехода из верхнего состояния в нижнее.
Многочастичные межмолекулярные взаимодействия. Для системы, состоящей более чем из двух молекул, полная энергия межмолекулярного взаимодействия отличается от суммы парных взаимодействий (неаддитивность). Так, при взаимод. трех частиц А, В, С энергию межмолекулярного взаимодействия можно записать в след. виде:
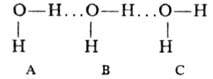
где первые три слагаемых представляют собой энергии парных межмолекулярных взаимодействий, а последний член-энергию тройного межмолекулярного взаимодействия, к-рое обусловливает отступление от аддитивности. Влияние многочастичных взаимод. на св-ва в-в обнаруживается экспериментально даже в случае инертных газов. Напр., равновесные расстояния различны в димерах (в газовой фазе) и в кристаллах вследствие неаддитивности обменной и дисперсионной энергий (электростатич. энергия межмолекулярного взаимодействия всегда аддитивна). Наиб. заметно влияние многочастичных взаимод. для комплексов полярных молекул и для ион-молекулярных комплексов. В них неаддитивность межмолекулярного взаимодействия обусловливают гл. обр. поляризационные силы, причем абс. величина и знак отклонения от аддитивности в энергии зависят от взаимного расположения частиц. Механизм многочастичного взаимод. полярных молекул можно пояснить на примере воды. При последоват. расположении трех молекул
39%, чем в газовой фазе; для воды соотв. значения составляют 6% и
Одним из распространенных потенциалов является п от е н ц и а л М о р с а (М о р з е):
содержащий эмпирич. параметры а, b и l.
Приведенные модельные потенциалы не учитывают взаимной ориентации взаимод. частиц. Для расчета взаимод. многоатомных молекул произвольной формы Т. Хиллом, а затем А.И.Китайгородским был разработан метод атом-атомных потенциалов. Согласно этому методу, межмол. потенциал V записывается в виде суммы потенциалов V ab парных взаимод. каждого атома а одной молекулы с каждым атомом b другой, причем V ab выражается к.-л. простой аналит. ф-цией, напр. потенциалом Букингема (7). Для каждой пары валентно не связанных атомов из эксперимента определяют эффективные значения входящих в V ab параметров, к-рые предполагаются универсальными, не зависящими от того, в какие молекулы входит данная пара атомов. Метод применим к мол. кристаллам, полимерам, сложным мол. комплексам. С его помощью рассчитывают конформации мол. изомеров, взаимные расположения моле кул в элементарной ячейке, теплоты сублимации кристаллов и др. Приближенность метода заключается, в частности, в том, что многочастичные взаимод. учитываются только косвенно, выбором эффективных значений параметров в атом-атомном потенциале.
Существует ряд методов, позволяющих в простых случаях определять межмол. потенциалы непосредственно из экспе-рим. данных, не прибегая к модельным потенциалам, напр. по вращательно-колебат. спектрам мол. комплексов, по рассеянию молекул при столкновениях или по данным о вязкости газов.
М ежмолекулярные взаимодействия изучают разл. физ. методами, основные из к-рых-молекулярных пучков метод, дифракционные методы, в частности газовая электронография, масс-спектрометрия по-выш. давления, ЯМР, микроволновая спектроскопия, ЯКР, колебат. спектроскопия (инфракрасная и комбинац. рассеяния), вакуумная УФ спектроскопия; изучение температурных зависимостей вириальных коэф., коэф. вязкости, диффузии, теплопроводности и др. Важную роль в исследовании межмолекулярных взаимодействий играют расчетные методы квантовой химии.
===
Исп. литература для статьи «МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ» : Гиршфельдер Дж., Кертисс Ч., Бэрд Р., Молекулярная теория газов и жидкостей, пер. с англ., М., 1961; Межмолекулярные взаимодействия; от двухатомных молекул до биополимеров, пер. с англ., М., 1981; Каплан И. Г., Введение в теорию межмолекулярных взаимодействий, М., 1982; Molecular interactions, ed. by H. Ratajczak, W.J. Orville-Thomas, v. 1-3, Chichester, 1980-82.
Страница «МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ» подготовлена по материалам химической энциклопедии.