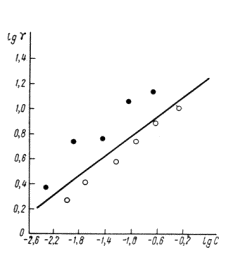
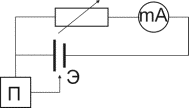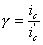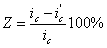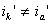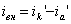какие утверждения о методе анодной защиты справедливы
Статьи
Анодная защита от коррозии
Анодная электрохимическая защита менее распространена, чем катодная электрохимическая защита. Это обусловлено тем, что она применяется для конструкций и сооружений, которые изготавливаются из низколегированных нержавеющих, углеродистых сталей, железистых высоколегированных сплавов, титана, и других разнородных пассивирующихся (способных к самостоятельной защите от коррозии) металлов. Анодная защита может применяться в хорошо электропроводных коррозионных средах.
При использовании анодной защиты, потенциал защищаемого металла смещается в более положительную сторону до тех пор, пока не будет достигнуто пассивное устойчивое состояние системы. При этом, достоинством анодной электрохимической защиты является не только очень значительное замедление скорости коррозии конструкции, но также и тот факт, что в производимый продукт и окружающую среду не попадают продукты коррозии.
Существуют несколько способов применения анодной защиты: смещение потенциала в положительную сторону используя источник внешнего электрического тока или введение в коррозионную среду окислителей или элементов в сплав, повышающих эффективность катодного процесса на поверхности металла. Анодная защита с использованием окислителей по механизму защиты схожа с анодной поляризацией.
При использовании пассивирующих ингибиторов с окисляющими свойствами, защищаемая поверхность переходит в пассивное состояние под воздействием возникающего тока. К таким ингибиторам относят бихроматы, нитраты и др. Однако их использование достаточно сильно загрязняет окружающую технологическую среду.
Реакция восстановления деполяризаторов, протекающая на катоде, при введении в сплав добавок, проходит с меньшим перенапряжением, чем на защищаемом металле. Введение таких добавок осуществляется, в основном, с помощью легирования благородными металлами.
При пропускании электрического тока через защищаемую конструкцию, происходит смещение её потенциала в положительную сторону.
Установка для анодной электрохимической антикоррозионной защиты состоит из источника внешнего тока, электрода сравнения, катода и самого защищаемого объекта.
Для того, чтобы узнать, имеется ли возможность применить анодную электрохимическую защиту для определенного объекта, снимают анодные поляризационные кривые, помогающие определить потенциал коррозии исследуемой конструкции в определенной коррозионной среде, область устойчивой пассивности и плотность тока в этой области.
При изготовления катодов используют малорастворимые металлы, к которым относят высоколегированные нержавеющие стали, тантал, никель, свинец, платину.
Для того, чтобы анодная электрохимическая защита в определенной среде была эффективной, возникает необходимость использования легкопассивируемых металлов и сплавов. При этом электрод сравнения и катод должны все время находится в растворе, а также соединительные элементы должны быть выполнены качественно. Для каждого индивидуального случая анодной защиты схема расположения катодов проектируется отдельно.
Чтобы анодная защита была эффективной для определенного объекта, необходимо, чтобы он отвечал следующим требованиям:
— все сварные швы должны быть выполнены качественно;
— материал, из которого выполнен защищаемый объект, в технологической среде должен переходить в пассивное состояние;
— количество щелей и воздушных карманов должно быть минимальным;
— на конструкции не должны присутствовать заклепочные соединения;
— в защищаемом устройстве электрод сравнения и катод должны всегда находиться в растворе.
Часто для реализации анодной защиты в химической промышленности используют теплообменники и установки, которые имеют цилиндрическую форму.
Электрохимическая анодная защита нержавеющих сталей используется для производственных хранилищ серной кислоты, минеральных удобрений, растворов на основе аммиака, а также всевозможных цистерн, сборников, мерников.
Анодная защита также применяется для недопущения коррозионного разрушения ванн химического никелирования, теплообменных установок на производствах искусственного волокна и серной кислоты.
ЗАЩИТА ОТ РЖАВЧИНЫ. Анодная защита
В этом видео мы вам расскажем как можно остановить коррозию.
Коррозия это процесс разрушения металлов под воздействием влаги и воздуха.
Из-за коррозии страны всего мира теряют от 2 до 4 процентов ВВП, это миллиарды долларов.
Для нашего опыта по замедлению коррозии, мы взяли полотно от ножовки. Полотно защищено краской, которую мы сняли. Сломав полотно, мы получили два одинаковых куска стали.
Для защиты от коррозии мы используем кусочек магниевой ленты. Магний намного активнее железа. При соприкосновении магния и стали, окисляться будет только магний. Таким образом, сталь будет защищена от коррозии. Такая защита называется анодной.
Для ускорения коррозии в тысячи раз нам поможет пищевая соль. Автомобилисты знают что соль это страшный враг кузова автомобиля.
Растворяем соль и опускаем в раствор два куска стали, один из них мы обмотали магниевой лентой.
Спустя два дня, можно увидеть результат.
Магний окислялся и мы несколько раз перематывали магниевую ленту и периодически очищали место контакта. Лучше было использовать болтик и гайку. Магниевая лента стала тонкой и легко рвется, потому что часть магния перешло в раствор.
На стальной пластине с анодной защитой образовался тонкий металлические налет,
Не защищенный кусок стали, сильно корродировал, то есть подвергся коррозии по всей поверхности, которая была опущена в раствор соли. Часть ржавчины осела на дне кружки.
Сталь показала плохую устойчивость к коррозии. Теперь вы понимаете зачем трубы, автомобили и другие стальные предметы подвергаются оцинковке. Хотя цинк хуже защищает от коррозии, но он в 3 раза дешевле магния.
Лекция 7. Электрохимическая защита от коррозии
Электрохимическая защита от коррозии
2. Протекторная защита
1. Наиболее важный метод борьбы с коррозией – катодная защита. Она заключается в приложении к корродирующему металлу катодной поляризации внешним током. При этом не происходит разрушение металла в течение длительного времени.
На практике катодную защиту можно применять для предупреждения – коррозии стали, меди, свинца, латуни в почве и в водных средах.
— коррозионное растрескивание под напряжением латуней, сталей (в т. ч. нержавеющих), магния, алюминия;
— межкристаллическую коррозию нержавеющих сталей.
Невозможно применение катодной защиты для непроводящих сред (атмосфера) и для электрически экранированных поверхностей.
История применения катодной защиты.
В 1824 г. англ. Х. Дэви сообщил, что медь можно успешно защищать от коррозии в соленой воде, если обеспечить ее контакт с железом или цинком. Он предложил осуществлять защиту медной обшивки кораблей с использованием прикрепленных к корпусу жертвенных железных блоков. В то время метод не получил развития, т. к. медь, катодно защищенная, обрастала микроорганизмами. И вплоть до 1950 г. возможность применения катодной защиты морских судов не изучалась.
Впервые положение внешнего электрического тока (-) было применено для защиты подземных сооружений в Англии и США в гг. В настоящее время катодной защитой эффективно защищают тысячи км подземных трубопроводов и кабелей. Применяют также катодную защиту для емкостей, баков, нефтяных установок и химического оборудования.
Теория катодной защиты.
Рассмотрим поляризационную коррозионную диаграмму, иллюстрирующую принцип катодной защиты.
К – катодная кривая
Из рис. 1 следует, что если за счет внешней катодной поляризации сместить потенциал анода от потенциала коррозии до ЕнА (до потенциала начального (в отсутствии тока )), то потенциалы Ен и ЕА будут одинаковы и металл не будет корродировать. Т. о. пока к металлу приложен внешний ток, он не будет корродировать.
Схема катодной защиты
Для катодной защиты необходим источник постоянного тока – выпрямитель1 (дизельный генератор), вспомогательный анод 3, расположенный на некотором расстоянии от защищаемого объекта. «+» источника тока подключается к вспомогательному аноду и на нем идет анодная реакция, отрицательный полюс подключается к защищаемому сооружению, на котором протекает катодная реакция восстановления кислорода, которая не приводит к разрушению трубопровода.
Материал анодов и засыпка
Вспомогательные аноды, используемые при катодной защите подземных трубопроводов, представляют собой чугунный лом или графит. Чугунный лом расходуется со скоростью 6-9 кг/(А∙год) и должен периодически заменяться. Графитовые аноды расходуются медленнее 0,9 кг/(А∙год). Но графит дороже чугуна, затраты электроэнергии выше в течение всего времени эксплуатации, т. к. графитовый анод имеет более высокий потенциал. Графит также более хрупкий, чем чугунный лом, и требует поэтому осторожного обращения при монтаже.
В морской воде используются аноды из меди, платинированной платиной – срок службы более 15 лет.
Для уменьшения сопротивления грунта, окружающего анод, анод помещают в засыпку, которая состоит из толстого слоя кокса с добавлением 3-4 части гипса (CaSO4∙H2O) и 1 часть NaCl.
Требуемая плотность защитного тока
Плотность тока, необходимая для полной зашиты, зависит от защищаемого материала и коррозионной среды.
Рис. 1 показывает, что плотность защитного тока (Iвнеш) всегда превышает плотность тока, эквивалентную скорости коррозии металла в этой же среде. Т. е., чем выше скорость коррозии, тем выше должна быть плотность защитного тока.
Важнейшим условием точного определения плотности тока, необходимого для полной защиты, является измерение величины потенциала защищаемого объекта. Эта величина Е должна обеспечить iзащ>iкор.
Приблизительные значения плотности тока для стали в различных средах при катодной защите
Вода морская – 0,03-0,15 А/м2
Вода с O2, гор. – 0,15 А/м2
Вода пресная – 0,05 А/м2
Минимальные величины потенциалов, при которых обеспечивается катодная защита для различных металлов
Эти потенциалы отвечают образованию гидроксидов соответствующих металлов Ме(ОН)2, которыми покрыта поверхность металлов.
Перезащита – превышение Iзащ над величиной, полученной по коррозионной диаграмме рис. 1
Незначительная перезащита не приводит к значительным отрицательным последствиям, только при этом происходят потери электроэнергии и увеличивается расход вспомогательных анодов. При значительном превышении защитной плотности тока возникают условия для дополнительного разрушения металла, вследствие выделения Н2 (охрупчивание стали, отслаивание покрытий).
Большую опасность представляет перезащита амфотерных металлов (Al, Zn). Создается щелочная среда, в которой эти металлы разрушаются с водородной деполяризацией.
2. Протекторная защита – разновидность катодной защиты, присоединение к «-» металлу.
Протекторную защиту целесообразно использовать в тех случаях, когда катодная защита невозможна (нет источника постоянного тока).
Проволоку припаивают к стальному наконечнику, который приваривают к трубе электродуговой сваркой. На трубопроводах, защищенных покрытием, изолируют место контакта и все открытые участки металла.
В том случае, если вспомогательный анод изготовлен из более активного металла (более электроотрицательного), чем защищаемый, то внешний источник тока можно не использовать, а электрод называется протектором (магний, цинк и сплавы на их основе). Они особенно целесообразны, когда имеются трудности с подачей электроэнергии и сооружать дополнительную линию электропередачи нецелесообразно.
На протекторы из магниевых сплавов для катодной защиты в США ежегодно расходуется 5,5 млн. тонн магния.
Для защиты резервуаров-хранилищ с сырой нефтью, в которых коррозия происходит из-за попадания воды, применяется алюминиевые протекторы, которые изготавливаются из сплава Al-Zn
с 2,5 % Zn. Для защиты требуется 71 шт., общей массой 1370 кг. Алюминиевые протекторы привариваются и устанавливаются внутри по днищу резервуара. Они защищают дно и боковые стенки на высоту до 1 м. Площадь защищаемой поверхности 2120 м2. Без протекторной защиты существует опасность сквозной коррозии днища за счет образования коррозионных микроэлементов. Срок службы – 24 года.
Радиус действия протектора
Действие протектора ограничивается определенным расстоянием от защищаемого металла. Максимально возможное удаление протектора от защищаемой конструкции называется радиусом действия протектора. Радиус действия увеличивается при увеличении электропроводности коррозионной среды и разности потенциалов между протектором и защищаемым металлом.
Экономические аспекты катодной защиты
Для подземных трубопроводов стоимость катодной защиты намного ниже, чем при использовании любых других способов, обеспечивающих аналогичную эффективность. В катодно защищенных трубопроводах исключены сквозные разрушения, что позволяет применять более высокие давления при транспортировке нефти
и газа. Благодаря этому толщина труб определяется только внутренним давлением. В современных условиях при катодной защите с использованием тока или протекторов используется одновременно лакокрасочные (при обычной температуре), эмалевые (при повышенной температуре) и различные изоляционные покрытия (битумные, каменноугольные и др.). Распределение защитного тока более экономично, необходимое число протекторов и величина защитного тока меньше, а участок трубопровода, защищаемый одним анодом, больше. Так, с помощью одного магниевого протектора можно защищать до 8 км трубопровода с покрытием. Для непокрываемого трубопровода защита простирается лишь на 30 м.
Предельная длина участка трубы, защищаемого одним анодом, определяется величиной снижения потенциала защиты по формуле:
Ех – потенциал на расстоянии х от места соединения с источником постоянного тока;
ЕА – потенциал источника тока;
RL – сопротивление трубы единичной длины и радиуса r;
z – сопротивление единицы поверхности покрытой трубы.
Применяется при транспортировке концентрированной H2SO4, фосфорной кислоты, солевых растворов:
Нержавеющая сталь в 0,5 М Na2 SO4
0,1-0,7 M щавелевой кислоты при 50 0С.
Для анодной защиты, в отличии от катодной, характерно, что скорость коррозии хоть и мала, но не равна 0. Но, с другой стороны, в агрессивных кислотах необходима значительно более низкая плотность тока, чем при катодной защите. Также при анодной защите достигается высокая рассеивающая способность (т. е. защита на удаленном от катода расстоянии). Это связано с высокими защитными свойствами образуются на аноде продуктов.
При анодной защите титана и сплавов титана токами в несколько мкА/см2 снижение скорости коррозии составляет:
В 40 % H2 SO4 – в 33000 раз
За счет анодной поляризации от внешнего источника электрической энергии можно перевести способный к этому металл в пассивное состояние и тем уменьшить скорость коррозии на несколько порядков.
Требования к анодной защите
Существуют требования, которым должна удовлетворять система, чтобы к ней можно было применить анодную защиту.
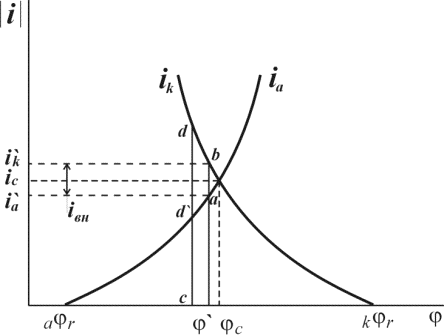
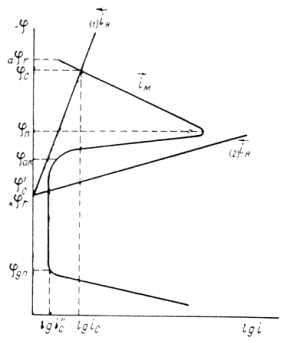
1. Прежде всего, нужно надежно знать анодную поляризационную кривую для выбранного металла в данной агрессивной среде рис.4. Чем выше iП, тем большая сила тока потребуется для перевода металла в пассивное состояние; чем шире диапазон ∆EП, тем большие колебания потенциала можно допустить, т. е. тем легче поддерживать металл в пассивном состоянии.
2. Нужна уверенность в том, что в области ∆EП металл корродирует равномерно. В противном случае, даже при малой величине iПП, возможно образование язв и сквозного разъедания стенки изделия. Форма защищаемой поверхности может быть довольно сложной, что затрудняет поддержание одинакового значения потенциала на всей поверхности; в этом отношении большая величина ∆EП особенно желательна.
3. Хорошая электропроводность среды.
Анодная защита может осуществляться несколькими способами.
1. Простое наложение постоянной э. д.с. от постороннего источника электрической энергии. Положительный полюс подключается к защищаемому изделию, а около его поверхности помещают катоды сравнения малого размера. Они размещаются в таком количестве и на таком расстоянии от защищаемой поверхности, чтобы обеспечить по возможности равномерную анодную поляризацию изделия. Этот способ применяется в том случае, если ∆EП достаточно велик и нет опасности, при некоторой неизбежной неравномерности распределения потенциала анода, активации или перепассивации, т. е. выхода за пределы ∆EП.
Таким способом можно защищать изделия из титана или циркония в серной кислоте. Нужно только помнить, что для пассивации сначала потребуется пропускание тока большей силы, что связано с переводом потенциала за ∆EП. Для начального периода целесообразно иметь дополнительный источник энергии. Следует учитывать также большую поляризацию катодов, плотность тока на которых велика вследствие их малых размеров. Однако, если область пассивного состояния велика, то изменение потенциала катода даже на несколько десятых вольта не представляет опасности.
2. Периодическое включение и выключение тока защиты, когда изделие уже запассивировано. При выключении анодного тока потенциал изделия смещается в отрицательную сторону, причем может произойти депассивация. Но поскольку иногда это происходит довольно медленно, простая автоматика может обеспечить включение и выключение защитного тока в нужное время. Когда потенциал дойдет до величины E′ПП, т. е. до начала перепассивации, ток выключается; когда потенциал сдвинется в отрицательную сторону до EПП (начало активации), ток снова включается. Смещение потенциала в катодную сторону происходит тем медленнее, чем меньше iПП. Чем ближе был потенциал к величине E′ПП, тем медленнее он смещается в отрицательную сторону (в направлении EПП) при выключении тока. Например, для хрома в 0,1 Н растворе H2 SO4 при 75 0С, если выключение тока произошло при E=0,35В, активация наступит через 2 часа; выключение тока при E=0,6В вызовет активацию через 5 часов; выключение же при E=1,05В увеличивает срок начала активации более чем до 127 часов. Столь большое время, необходимое для депассивации, позволяет делать значительные перерывы в подаче тока. Тогда одной и той же установкой можно обслужить несколько объектов.
3. Если область пассивного состояния (∆EП) мала, то необходимо применение потенциостата, поддерживающего заданную величину потенциала (относительно некоторого электрода сравнения) в узких границах. Потенциостат должен быть способен давать большую силу тока.
Недостатки анодной защиты
Использование анодной защиты связано со значительными трудностями. В то время как катодная защита может употребляться для защиты многих металлов, погруженных в любую электропроводящую среду, например твердую или жидкую, анодная защита применяется только для защиты целых секций химических установок, которые изготовлены из металла, способного пассивироваться в рабочей среде. Именно это и ограничивает ее применение. Кроме того, анодная защита потенциально опасна, поскольку при перерывах подачи тока без немедленного восстановления защиты на рассматриваемом участке начнется очень быстрое растворение, т. к. разрыв в пленке образует путь с низким сопротивлением в условиях анодной поляризации металла.
Использование анодной защиты требует тщательного проектирования химической установки. Последняя должна иметь такую систему контроля, чтобы любая потеря защиты немедленно привлекла внимание оператора. Для этого может быть достаточным только локальное повышение анодного тока, однако в наихудшем случае может потребоваться немедленное опорожнение всей установки.
Анодная защита не обеспечивает стойкости в присутствии агрессивных ионов. Так, хлоридные ионы разрушают пассивную пленку, а потому их концентрация должна поддерживаться низкой, за исключением защиты титана, который может пассивироваться в хлористоводородной кислоте.
Анодная поляризационная кривая для пассивирующего металла.
Электрохимические методы защиты металлов от коррозии
кафедра физической химии
Курсовая работа по электрохимии
Тема : «Электрохимические методы защиты металлов от коррозии»
Выполнила студентка III курса
35-й группы ХБГ факультета
СОДЕРЖАНИЕ
Понятие коррозии. 3
Значение термина «коррозия». 3
Химическое и электрохимическое окисление металлов. 3
Общие положения электрохимической теории коррозии. 4
Другие способы изображения коррозионных диаграмм. 8
Методы защиты металлов от коррозии. 8
Явление пассивности. 12
Анодная защита. Использование пассивности в практике защиты от коррозии. 14
Покрытия, как метод защиты металлов от коррозии. 18
Понятие коррозии.
Значение термина «коррозия»
Самопроизвольное окисление металлов, вредное для промышленной практики (уменьшающее долговечность изделий), называется коррозией[1]. Среда, в которой металл подвергается коррозии (корродирует), называется коррозионной, или агрессивной. При этом образуются продукты коррозии: химические соединения, содержащие металл в окисленной форме.
В тех случаях, когда окисление металла необходимо для осуществления какого-либо технологического процесса, термин «коррозия» употреблять не следует. Например, нельзя говорить о коррозии растворимого анода в гальванической ванне, поскольку анод должен окислятся, посылая свои ионы в раствор, чтобы протекал нужный процесс. Нельзя также говорить о коррозии алюминия при осуществлении алюмотермического процесса. Но физико-химическая сущность изменений, происходящих с металлом во всех подобных случаях, одинакова: металл окисляется.
Следовательно, термин «коррозия» имеет не столько научное, сколько инженерное значение. Правильнее было бы употреблять термин «окисление», независимо от того вредно или полезно оно для нашей практики.
Коррозия является естественным процессом, обусловленным термодинамической нестойкостью металлов в условиях службы. Естественно поэтому, что изучение коррозии и разработка методов защиты металлов от нее представляют несомненный теоретический интерес и имеют большое народнохозяйственное значение.
Химическое и электрохимическое окисление металлов.
Кинетика процессов окисления зависит от природы среды, содержащий окислитель. Если среда представляет собой электролит (очень частый случай), окисление протекает по электрохимическому механизму:
n ox + z e à m red (2)
где ox-окислитель, а red- восстановленная форма его.
Реакции (1) и (2) протекают сопряженно на анодных и катодных участках, площадью 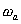
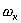
Если окислитель не является электролитом, то обмен электронами совершается непосредственно между металлом и окислителем:
Здесь окисление протекает по химическому механизму.
Таким образом, принято различать электрохимическую и химическую коррозию, хотя такое разделение в некоторой степени условно.
Общие положения электрохимической теории коррозии.
Рассмотрим схему коррозионного процесса. Сложность его заключается в том, что на одной и той же поверхности происходят одновременно два процесса, противоположные по своему химическому смыслу: окисление металла и восстановление окислителя. Оба процесса должны протекать сопряженно, чтобы сохранялось равенство числа электронов, отдаваемых металлом и присоединяющихся к окислителю в единицу времени. Только в этом случае может наступить стационарное состояние.
Независимое, но сопряженное протекание процессов окисления и восстановления позволяет рассматривать коррозию при помощи анодных и катодных поляризационных кривых. На рис.1 показана коррозионная диаграмма для металла и окислителя. Чтобы окисление металла окислителем могло иметь место, 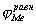
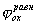
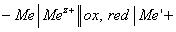
Для получения коррозионной диаграммы необходимо построить электрическую цепь, изображённую на рисунке 2. Проведя несколько измерений, изменяя величину сопротивления, и соответственно наблюдая за изменением силы тока, а также потенциала в цепи, строят зависимость 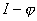
При разомкнутой цепи мы измерили бы э.д.с. 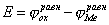
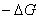
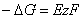
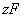
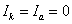
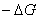
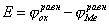
Если не пользоваться гальваническим элементом, а просто погрузить металл в раствор, содержащий окислитель, то стационарное состояние будет возможно только в том случае, если скорость реакции окисления металла (1) будет равна скорости восстановления окислителя (2).
Это означает, что при стационарном потенциале 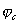
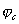
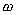
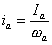
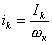
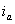
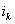
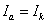
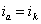

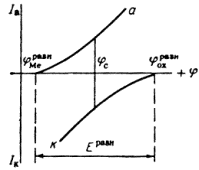
На рис.1 изображены анодная а и катодная к поляризационные кривые для данного металла в растворе определенного состава и для данного окислителя на поверхности того же металла. Наклон кривых а и к определяет кинетику процесса. Таким образом, рисунок содержит сведения о термодинамической возможности коррозии данного металла некоторым окислителем и о скорости этого процесса, определяемой кинетикой реакций (1) и (2), т.е. зависимостью их скоростей от смещения соответствующих потенциалов от равновесного значения. Коррозия возможна только в том случае, если 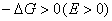
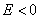
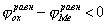
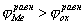
Рис. 3. Поляризационные кривые, отвечающие случаю, когда 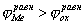
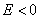
Легко понять, что при данном 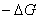
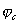
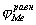

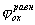
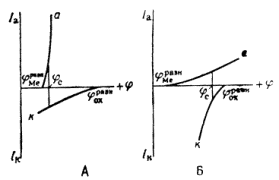
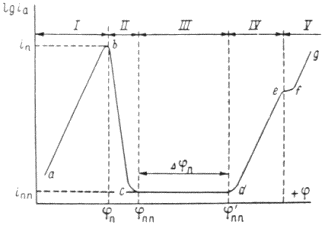
Рис. 4. Коррозионные диаграммы, отвечающие катодному контролю (А) и анодному контролю (Б).
Другие способы изображения коррозионных диаграмм
Применяемый в этой главе способ рассмотрения процессов коррозии при помощи поляризационных диаграмм весьма распространен. В том виде, в котором мы его использовали выше, он был предложен К. Вагнером и В. Траудом и подробно разработан А. М. Шультиным Способ этот характеризуется тем, что анодный и катодный токи, выражающие скорость противоположных по химическому смыслу процессов, откладываются в противоположные стороны от оси абсцисс. По оси абсцисс откладывается потенциал.
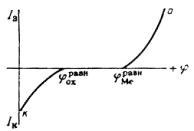
Однако весьма распространен и другой метод, предложенный Ю. Р. Эвансом, при котором ток, измеряющий скорость окисления и восстановления, откладывается в одном направлении и принимается за аргумент (абсцисса). Потенциал (ордината) откладывается так, что иногда вверх растет положительное значение, а иногда – отрицательное
Легко убедиться, что все способы изображения коррозионных диаграмм по существу равноценны. Дальше мы будем использовать различные способы изображения, для того чтобы научиться разбираться и в тех, и в других.
Методы защиты металлов от коррозии.
В зависимости от характера коррозии и условий ее протекания применяются различные методы защиты. Выбор того или иного способа определяется его эффективностью в данном конкретном случае, а также экономической целесообразностью. Любой метод защиты изменяет ход коррозионного процесса, либо уменьшая скорость, либо прекращая его полностью. Коррозионные диаграммы, наиболее полно характеризующие коррозионный процесс, должны отражать и те изменения в ходе протекания, какие наблюдаются в условиях защиты. Коррозионные диаграммы можно использовать, поэтому при разработке возможных путей предохранения металлов от коррозии. Они служат основой для выяснения принципиальных особенностей того или иного метода. В связи с этим при рассмотрении существующих методов защиты поляризационные диаграммы будут использованы в их несколько упрощенном виде (4). На таких диаграммах постулируется линейная зависимость между плотностью и потенциалом каждой частной реакции. Это упрощение оказывается вполне допустимым при качественной оценке особенностей большинства методов
где 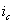
Катодная защита
Из всех методов защиты основанных на изменении электрохимических свойств металла под действием поляризующего тока, наибольшее распространение получила защита металлов при наложении на них катодной поляризации (катодная защита). При смещении потенциала металла в сторону более электроотрицательных значений (по сравнению с величиной стационарного потенциала коррозии) скорость катодной реакции увеличивается, а скорость анодной падает (см. рис. 4). Если при стационарном потенциале 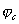
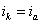
то при более отрицательном значении 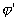
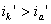
Рис. 5. Поляризационная диаграмма коррозионного процесса.
Уменьшение скорости анодной реакции при катодной поляризации эквивалентно уменьшению скорости коррозии. Коэффициент торможения при выбранном потенциале j / (см.рис.4) будет равен двум

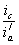
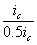
а степень защиты достигает 50%
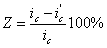
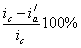
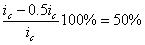
Внешний ток 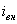

Защита металла катодной поляризацией применяется для повышения стойкости металлических сооружений в условиях подземной (почвенной) и морской коррозии, а также при контакте металлов с агрессивными химическими средами. Она является экономически оправданной в тех случаях, когда коррозионная среда обладает достаточной электропроводностью, и потери напряжения (связанные с протеканием защитного тока), а следовательно, и расход электроэнергии сравнительно невелик. Катодная поляризация защищаемого металла достигается либо наложением тока от внешнего источника (катодная защита), либо созданием макрогальванической пары с менее благородным металлом (обычно применяются алюминий, магний, цинк и их сплавы). Он играет здесь роль анода и растворяется со скоростью, достаточной для создания в системе электрического тока необходимой силы (протекторная защита). Растворимый анод при протекторной защите часто называют “жертвенным анодом”.
Применение для катодной защиты метода приложения тока облегчает регулирование системы и часто дешевле, чем использование анодов – протекторов, которые, конечно, нуждаются в регулярных заменах.
На практике катодная защита редко применяется без дополнительных мероприятий. Требуемый для полной защиты ток обычно бывает чрезмерно велик, и помимо дорогостоящих электрических установок для его обеспечения следует иметь в виду, что такой ток часто будет вызывать вредный побочный эффект, например чрезмерное защелачивание. Поэтому катодная защита применяется в сочетании с некоторыми видами покрытий. Требуемый при этом ток мал и служит только для защиты обнаженных участков поверхности металла.
Явление пассивности.
Давно известно, что скорость коррозии многих металлов часто значительно меньше в растворах сильных окислителей, чем в растворах окислителей более слабых. Сюда относятся такие металлы, как железо, хром, никель, титан, цирконий, алюминий и многие другие. Резкое уменьшение скорости коррозии (на несколько порядков) в сильных окислителях, казалось бы противоречащее термодинамическим свойствам металла и окислителя, называется пассивацией, а состояние металла – пассивным.
Некоторые металлы находятся в пассивном (или близком к пассивному) состоянии даже в таких слабых окислителях, как вода. Это дает возможность практически использовать в качестве конструкционных материалов магний, титан, алюминий и многие другие.
М.В. Ломоносов был, по-видимому, первым исследователем, обратившим внимание на пассивность железа в концентрированной азотной кислоте. Железу посвящены наблюдения М. Фарадея и Х. Шенбейна. М. Фарадей сделал удивительную по научной дальновидности попытку объяснить пассивность железа образованием на поверхности слоя (пленки) окисла или же существованием поверхностных атомов металла в таком состоянии, которое равноценно окислению.
Очень большое практическое значение пассивности, часто определяющее возможность получения сплавов, химически стойких в агрессивных средах, вызвало огромное количество исследований, посвященных изучению пассивного состояния. Если отбросить некоторые несущественные различия, высказываемые на основании сопоставления экспериментальных данных, сказав, что пассивное состояние обусловлено образованием очень тонкой пленки окисла, представляющего собой отдельную фазу, или слоя хемисорбированного кислорода, а может быть и других частиц. Ограничимся представлением о некотором кислородном «барьере», образующемся на поверхности металла в подходящем окислителе и сильно тормозящем анодный процесс.
Рис. 6. Полная анодная поляризационная кривая: I – активное растворение; II – переход в пассивное состояние; III – пассивность; IV – перепассивация; V – выделение кислорода.
При изменение потенциала в обратном направлении кривая, вообще говоря, имеет такой же ход. В таком случае 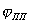
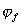
В настоящее время вопрос сводится к изучению природы защитных образований на металле, в которых обычно участвует кислород.
При более высоком потенциале становится возможным процесс выделения кислорода:
Зависимость времени запассивации от потенциала включения легко объяснима при помощи концепции фазового окисла (образуется более толстый слой окисла, растворение которого требует больше времени). Труднее объяснить это явление десорбцией пассивирующего кислорода. Конечно, с ростом положительного значения потенциала прочность связи в адсорбционном слое должна увеличиваться. Но при включении тока разряд двойного слоя происходит сравнительно быстро, хотя адсорбционный слой, возможно, сохраняется долго.
3. Если область пассивного состояния (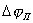
В настоящее время уже имеется ряд установок для анодной защиты, осуществленных в промышленном масштабе. Защищаются изделия и из обычной углеродистой стали. При анодной защите не только увеличивается срок службы аппаратуры, но также уменьшается загрязнение агрессивной среды продуктами коррозии. Например, в олеуме углеродистая сталь корродирует очень медленно и в этом смысле не нуждается в защите. Но в сосудах для хранения этого продукта происходит загрязнение его железом. Так, без анодной защиты в одной из промышленных установок содержание железа в олеуме составляло ≈ 0,12 %. После наложения защиты концентрация железа снизилась до ≈ 0,004 %, что соответствует его содержанию в исходном продукте. Загрязнение продуктов химической промышленности примесями соединений металлов, являющееся следствием коррозии аппаратуры, во многих случаях весьма нежелательно и даже недопустимо.
Однако, использование анодной защиты связано со значительными трудностями. В то время как катодная защита может употребляться для защиты многих металлов, погруженных в любую электропроводящую среду, например твердую или жидкую, анодная защита применяется только для защиты целых секций химических установок, которые изготовлены из металла, способного пассивироваться в рабочей среде. Именно это и ограничивает ее применение. Кроме того, анодная защита потенциально опасна, поскольку при перерывах подачи тока без немедленного восстановления защиты на рассматриваемом участке начнется очень быстрое растворение, так как разрыв в пленке образует путь с низким сопротивлением в условиях анодной поляризации металла.
Использование анодной защиты требует тщательного проектирования химической установки. Последняя должна иметь такую систему контроля, чтобы любая потеря защиты немедленно привлекала внимание оператора. Для этого может быть достаточным только локальное повышение анодного тока, однако в наихудшем случае может потребоваться немедленное опорожнение всей установки.
Анодная защита не обеспечивает стойкости в присутствии агрессивных ионов. Так, хлоридные ионы разрушают пассивную пленку, а потому их концентрация должна поддерживаться низкой, за исключением защиты титана, который может пассивироваться в хлористоводородной кислоте. В условиях анодной защиты имеет место хорошая рассеивающая способность электролитов и поэтому для поддержания ее установленной защиты требуется сравнительно небольшое количество электродов. Однако при проектировании установок анодной защиты следует учитывать, что в условиях, предшествующих пассивации, рассеивающая способность хуже.
Анодная защита потребляет очень мало энергии и может применяться для защиты обычных конструкционных металлов, способных пассивироваться, например углеродистой и нержавеющей стали, во многих средах. Эта защита легко подвергается контролю и измерениям и не требует дорогостоящей обработки поверхности металла, так как использует самопроизвольный эффект реакции между стенками емкостей и их содержимым. Способ изящен, и его применение, по-видимому, будет расширяться, как только будут преодолены сложности измерения и контроля.
Покрытия, как метод защиты металлов от коррозии.
Защита металлов, основанная на изменение их свойств, осуществляется или специальной обработкой их поверхности, или легированием. Обработка поверхности металла с целью уменьшения коррозии проводится одним из следующих способов: покрытием металла поверхностными пассивирующими пленками из его трудно растворимых соединений (окислы, фосфаты, сульфаты, вольфраматы или их комбинации), созданием защитных слоев из смазок, битумов, красок, эмалей и т.п. и нанесением покрытий из других металлов, более стойких в данных конкретных условиях, чем защищаемый металл (лужение, цинкование, меднение, никелирование, хромирование, свинцование, родирование и т.д.).
Защитное действие большинства поверхностных пленок можно отнести за счет вызванной ими механической изоляции металла от окружающей среды. По теории локальных элементов, их эффект следует рассматривать как результат увеличения электрического сопротивления (рис. 8).
Рис. 7. Коррозионная диаграмма, показывающая, что уменьшение скорости коррозии при нанесении поверхностных защитных слоёв может быть объяснено как увеличением омического сопротивления (а), так и повышением частных коррозионных реакций (б).
Повышение устойчивости железных и стальных изделий при покрытии их поверхности осадками других металлов обусловлено и механической изоляцией поверхности, и изменением ее электрохимических свойств. При этом может наблюдаться или смещение обратимого потенциала анодной реакции в сторону более положительных значений (покрытия медью, никелем, родием), или увеличение поляризации катодной реакции – повышение водородного перенапряжения (цинк, олово, свинец). Как следует из диаграмм (рис.8), все эти изменения уменьшают скорость коррозии.
Обработку поверхности металлов применяют для предохранения машин, оборудования, аппаратов и предметов домашнего обихода при временной защите в условиях транспортировки, хранения и консервации (смазка, пассивирующие пленки) и для более длительной защиты при их эксплуатации (лаки, краски, эмали, металлические покрытия). Общим недостатком этих металлов является то, что при удалении (например, вследствие износа или повреждения) поверхностного слоя скорость коррозии на поврежденном месте резко возрастает, а повторное нанесение защитного покрытия не всегда бывает возможно.
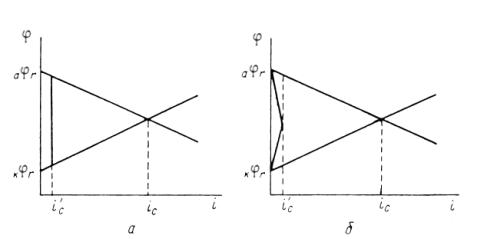
В этом отношении легирование является значительно более эффективным (хотя и более дорогим) методом повышения коррозионной стойкости металлов. Примером повышения коррозийной стойкости металла легированием являются сплавы меди с золотом. Для надежной защиты меди необходимо добавлять к ней значительное количество золота (не менее 52,2 ат.%). Атомы золота механически защищают атомы меди от их взаимодействия с окружающей средой. Несравненно меньше количество легирующих компонентов требуется для повышения устойчивости металла, если эти компоненты способны образовывать с кислородом защитные пассивирующие пленки. Так, введение хрома в количестве нескольких процентов резко увеличивает коррозионную стойкость сталей. Теоретический и практический интерес представляет повышение коррозионной стойкости легированием катодными добавками (Томашов). Для выяснения принципов, на которых основан этот метод, можно, следуя Колотыркину, рассмотреть потенциостатические кривые. В отсутствие внешнего поляризующего тока металл находится при стационарном потенциале 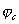
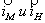
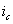
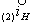
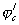
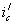
Рис. 8. Поляризационная диаграмма, показывающая возможность защиты пассивирующегося металла от коррозии при увеличении скорости катодного процесса.
Ингибиторы.
Скорость коррозии можно снизить также изменением свойств коррозионной среды. Это достигается или соответствующей обработкой среды, в результате которой уменьшается ее агрессивность, или введением в коррозионную среду небольших добавок специальных веществ, так называемых замедлителей или ингибиторов коррозии.
Обработка среды включает в себя все способы, уменьшающие концентрацию ее компонентов, особенно опасных в коррозионном отношении. Так, например, в нейтральных солевых средах и пресной воде одним из самых агрессивных компонентов является кислород. Его удаляют деаэрацией (кипячение, дистилляция, барботаж инертного газа) или смазывают при помощи соответствующих реагентов (сульфиты, гидразин и т.п.). Уменьшение концентрации кислорода должно почти линейно снижать предельный ток его восстановления, а следовательно, и скорость коррозии металла. Агрессивность среды уменьшается также при ее подщелачивании, снижение общего содержания солей и замене более агрессивных ионов менее агрессивными. При противокоррозионной подготовке воды для уменьшения накипеобразования широко применяется ее очистка ионнообменными смолами.
Ингибиторы коррозии разделяют, в зависимости от условий их применения, на жидкофазные и парофазные или летучие. Жидкофазные ингибиторы делят в свою очередь на ингибиторы коррозии в нейтральных, щелочных и кислых средах. В качестве ингибиторов для нейтральных растворов чаще всего применяются неорганические вещества анионного типа. Их тормозящее действие связано, по-видимому, или с окислением поверхности металла (нитриты, хроматы), или с образованием пленки труднорастворимого соединения между металлом, данным анионом и, возможно, кислородом (фосфаты, гидрофосфаты). Исключение представляют в этом отношении соли бензойной кислоты, ингибирующий эффект которых связан, главным образом, с адсорбционными явлениями. Все ингибиторы для нейтральных сред тормозят преимущественно анодную реакцию, смещая стационарный потенциал в положительную сторону. До настоящего времени еще не удалось найти эффективных ингибиторов коррозии металлов в щелочных растворах. Некоторым тормозящим действием обладают лишь высокомолекулярные соединения.
В качестве ингибиторов кислотной коррозии применяются почти исключительно органические вещества, содержащие азот, серу или кислород в виде амино-, имино-, тиогрупп, а также в виде карбоксильных, карбонильных и некоторых других групп. Согласно наиболее распространенному мнению, действие ингибиторов кислотной коррозии связано с их адсорбцией на границе раздела металл – кислота. В результате адсорбции ингибиторов наблюдается торможение катодного и анодного процессов, снижающие скорость коррозии.
В связи с преобладающим адсорбционным эффектом органических ингибиторов кислотной коррозии особое значение для понимания механизма их действия и для рационального подхода к созданию новых ингибиторов приобретает величина заряда поверхности корродирующего металла, т.е. величина его 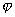
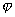
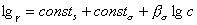
где 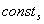
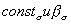
Адсорбция, однако, является лишь необходимым условием проявления ингибирующего действия органических веществ, но не определяет полностью фактического эффекта ингибиторов. Последний зависит также от многих других факторов – электрохимических особенностей протекания данного коррозионного процесса, характера катодной реакции, величины и природы перенапряжения водорода (при коррозии с водородной деполяризацией), возможных химических превращений ингибитора в ходе коррозии и т.д.
Действие большинства ингибиторов кислотной коррозии усиливается при одновременном введении добавок поверхностно – активных анионов: галогенидов, сульфидов и роданидов.
Ингибирование – сложный способ защиты, и его успешное применение в различных условиях требует широких познаний.
[1] От латинского corrodere-разъедать.