мази с гепарином для вен список лучших
Гепариновая мазь: описание, инструкция, цена
Гепариновую мазь, купить которую без рецепта можно в аптеках Екатеринбурга, изготавливают из гепарина натрия и вспомогательных компонентов. Препарат является антикоагулянтом прямого действия, способствующим нейтрализации воспалительных процессов и рассасыванию имеющихся, а также препятствующим образованию новых тромбов.
Фармакология
Фармакокинетика
Процесс всасывания препарата с поверхностного слоя эпидермиса характеризуется незначительными показателями. Белково-плазменная связь доходит до 95%, распределительный объем составляет 0,06 литра/кг. Плацентарного проникновения, как и смешивания компонентов с грудным молоком, не наблюдается. Основной областью концентрации, ввиду активной клеточной деятельности, являются печень и селезенка. Печеночный метаболизм осуществляется при активном воздействии N-десульфамидазы, а также тромбоцит-гепариназы, вступающей на поздних стадиях.
Продолжительность полувыведения низкомолекулярных фрагментов зависит от клинической картины – при стандартных показателях варьируется в пределах 1-1,5 часов, однако наличие негативных факторов, таких как ожирение, вирусные инфекции, онкология и т.д., может увеличить данный период до шести часов. Вывод осуществляется в процессе почечной активности. Бензилникотинат, несмотря на проникновение в каждый слой эпидермиса, не попадает в общую систему кровотока. Абсорбция бензокаина практически равна нулю.
Показания и противопоказания
Методика применения
Мазь наносится на пораженный участок тонким слоем, после чего аккуратно втирается легкими движениями. Продолжительность цикла применения варьируется от трех до семи дней (нанесение производится два-три раза в сутки), более длительные периоды требуют согласования с лечащим врачом. Использование препарата для лечения наружного геморроя предусматривает применение специальных ректальных тампонов – в данном случае мазью покрывается прокладка, фиксируемая на тромбированном узле. Продолжительность курса зависит от сроков исчезновения симптомов патологии, и, как правило, составляет от трех дней до двух недель.
Побочные эффекты
Стоимость препарата
Состав выпускается в тубах под брендами различных фармакологических компаний. Цены на гепариновую мазь зависят от объема упаковки, а также дополнительных факторов – так, отечественный препарат объемом 30 г (Лавенум) может обойтись в 150-170 рублей, тогда как стоимость импортных аналогов (Лиотон) доходит до 500 рублей за тот же объем.
Гепариновая мазь (Hepariniointment)



Состав и форма выпуска
Цены в аптеках
| Вещество | Количество |
|---|---|
| Гепарин натрий | 0,617 мг/1 г |
| Бензокаин | 40 мг/1 г |
Фармакологические свойства
фармакодинамика. Гепариновая мазь — антикоагулянт прямого действия, оказывает противовоспалительное и местное обезболивающее действие, предотвращает образование тромбов, способствует рассасыванию образовавшихся тромбов.
Фармакокинетика. Не определяли.
Показания Гепариновая мазь
профилактика и лечение тромбофлебита поверхностных вен; постинъекционный и постинфузионный флебит, трофические язвы голени, слоновость, поверхностный перифлебит, лимфангиит; наружный геморрой, воспаление геморроидальных узлов после родов; поверхностный мастит; локализованные инфильтраты и отеки, травмы и ушибы без нарушения целостности кожных покровов (в том числе мышечной ткани, сухожилий, суставов).
Применение Гепариновая мазь
препарат применяют у взрослых местно.
При тромбофлебите поверхностных вен конечностей мазь нанести на зону поражения тонким слоем (из расчета 0,5–1 г (2–4 см мази) на участок диаметром 3–5 см) и осторожно втирать в кожу 2–3 раза в сутки в течение 3–7 сут до исчезновения признаков воспаления. Возможность проведения длительного курса лечения определяет врач.
При тромбозе геморроидальных вен мазь следует нанести на салфетку из ткани, которую непосредственно накладывают на геморроидальные узлы, и зафиксировать повязкой (возможно применение тампона с нанесенной на него мазью, который следует ввести в задний проход) 2–3 раза в сутки до исчезновения признаков воспаления, в среднем 3–14 сут. Возможность длительного применения определяет врач индивидуально.
Противопоказания
гиперчувствительность к любому из компонентов препарата. Язвенно-некротические процессы, травматическое нарушение целостности кожных покровов, открытые инфицированные раны, геморрагический диатез, пурпура, тромбоцитопения, гемофилия, склонность к кровотечениям.
Побочные эффекты
покраснение, кожная сыпь, крапивница, ангионевротический отек, геморрагии, иногда возможно возникновение небольших пустул, пузырьков или пузырей. Возможно местное раздражающее действие, проявляющееся в виде жжения, зуда или незначительного отека кожи. Наличие в составе препарата метилпарагидроксибензоата (Е218) может вызвать аллергические реакции (возможно, замедленного типа), при нанесении на обширные участки кожи возможны системные аллергические реакции, гиперемия.
Особые указания
при длительном применении мази на обширных участках и одновременном применении пероральных лекарственных средств, влияющих на свертывающую систему крови и/или кроветворение, следует контролировать время свертывания и протромбиновое время. В случае необходимости длительного курса лечения и нанесения на обширные участки поражения у женщин в возрасте ≥65 лет рекомендуется проведение аналогичного контроля.
Не следует наносить на открытые раны при наличии гнойных процессов. Применение мази не рекомендуется при глубоком венозном тромбозе.
Препарат не следует назначать при кровотечениях, наносить на слизистые оболочки, инфицированные участки кожи, внутрь глаза и на участки вокруг глаз, на язвы и волдыри. В случае нарушения свертывания крови не рекомендуется наносить на обширные участки кожи.
При тромбоцитопении и повышенной склонности к кровотечениям препарат применять под контролем врача.
Применение в период беременности или кормления грудью. Не применять в период беременности и кормления грудью.
Дети. Не использовать.
Способность влиять на скорость реакции при управлении транспортными средствами или работе с другими механизмами. Не влияет.
Взаимодействия
действие мази усиливают антикоагулянты, ацетилсалициловая кислота и другие НПВП. Эффективность мази снижают препараты наперстянки, тетрациклины, никотин, антигистаминные препараты. Применение гепарина может обусловливать удлинение протромбинового времени у больных, принимающих пероральные антикоагулянты. Не рекомендован прием препарата сочетанно с лекарственными средствами для местного применения, например с лекарственными средствами, содержащими тетрациклин, гидрокортизон, салициловую кислоту, с антикоагулянтами.
Передозировка
вследствие низкого уровня всасывания гепариновой мази ее передозировка невозможна.
Условия хранения
при температуре 8–20 °С в недоступном для детей месте.
Актуальная информация
Гепариновая мазь в качестве действующего вещества содержит антикоагулянт прямого действия гепарин. Данное лекарственное средство применяется топически для терапии и профилактики венозного тромбоза различного генеза, включая постинъекционный флебит, перифлебит и геморрой.
Гепарин при местном применении оказывает антикоагулянтное, противовоспалительное и обезболивающее действие. Исходя из этих свойств, Гепариновая мазь может применяться также в лечении мастита, травм и ушибов, слоновости, трофических язв и лимфангиита.
Гепариновая мазь: нестареющая классика
Гепарин относится к группе полисахаридов гликозаминогликанов, его химическая структура характеризуется чередованием дисахаридов гексуроновой кислоты и гексозамина. При этом гепарин является высокосульфатированной молекулой, и благодаря этому свойству обладает очень высоким отрицательным зарядом, который позволяет ему связываться с широким спектром положительно заряженных молекул. Средняя молекулярная масса находится в пределах 14–18 кДа (Page С., 2013).
2016 г. ― это год 100-летнего юбилея с момента открытия гепарина студентом Джеем Маклином (Jay McLean), работавшим под руководством Уильяма Хауэлла (William Howell). Свое название гепарин получил в 1918 г. (Rák K., 1998). Оно было дано этому веществу двумя учеными ― Эметтом Холтом (Emmett Holt) и Уильямом Хауэллом (William Howell) (Ong C.S. et al., 2019). Уже в 40-х годах ХХ в. началось широкое клиническое применение гепарина. Именно внедрение гепарина в клиническую практику позволило совершить прорыв в кардио-пульмональной хирургии, лечении ТЭЛА (тромбоэмболии легочных артерий), ведении больных с ХПН (хронической почечной недостаточностью) и тяжелыми отравлениями, а именно сделало возможным проведение гемодиализа (Messmore H.L. еt al., 2004).
Гепарин применяется в качестве антикоагулянта более 80 лет. Несмотря на его широкое применение, точный механизм антикоагулянтной активности гепарина не был выяснен до 1960-х годов, а специфическая полисахаридная последовательность в молекуле гепарина, ответственная за антикоагулянтный эффект, была определена только в 1980-е годы (Page С., 2013). В дальнейшем было выявлено, что только часть молекулы гепарина обладает высоким сродством к антитромбину и обеспечивает антикоагулянтное действие, и синтезированы низкомолекулярные производные гепарина (Messmore H.L. еt al., 2004).
Гепариновая мазь: чем обусловлены противовоспалительные свойства
В настоящее время имеются весомые доказательства того, что гепарин также проявляет противовоспалительную активность, подтвержденную в исследованиях как in vitro, так и in vivo. Важно, что во многих случаях противовоспалительное действие гепарина не зависит от его антикоагулянтной активности ― ведутся поиски лекарственных средств на основе гепарина, обладающих его противовоспалительными свойствами, но не проявляющих антикоагулянтного эффекта. Гепарин проявляет противовоспалительную активность посредством различных механизмов, включая нейтрализацию катионных медиаторов, ингибирование молекул адгезии и гепараназы, угнетение миграции лейкоцитов в периферические ткани (Page С., 2013).
Так, тучные клетки содержат множество гранул с медиаторами воспаления. Также было установлено, что в тучных клетках содержатся гранулы с гепарином. В дальнейшем было зафиксировано, что многие белки, участвующие в каскаде воспалительных реакций, имеют в своей структуре гепаринсвязывающие домены, и гепарин способен ингибировать действие этих белков. Таким образом, эндогенный гепарин может играть важную роль в контроле локального воспалительного ответа, а не только в системе свертывания. Имеются убедительные доказательства возможности клинического применения этих свойств гепарина. Однако применение самого гепарина в качестве противовоспалительного лекарственного средства в настоящее время ограничено антикоагулянтной активностью молекулы. В то же время в исследованиях продемонстрировано, что при применении гепарина в виде ингаляций даже в высоких дозах антикоагулянтного действия не отмечено (Page С., 2013).
Гепарин может ингибировать активацию ряда воспалительных клеток. Этот эффект частично объясняется связыванием и нейтрализацией медиаторов воспаления и ферментов, высвобождаемых во время воспалительного ответа. Также было установлено, что некоторые ферменты и цитотоксические медиаторы, высвобождаемые из этих клеток, участвующие в каскаде реакций воспалительного ответа и последующем повреждении и ремоделировании ткани, также ингибируются гепарином, включая эластазу, катепсин G, эозинофилы пероксидазы, эозинофильный катионный белок, некоторые хемо- и цитокины.
Факторы роста, в том числе основной фактор роста фибробластов и трансформирующий фактор роста бета-1, участвуют в регуляции пролиферации гладких мышц (особенность ремоделирования тканей наблюдается при таких заболеваниях, как БА, атеросклероз и коронарный стеноз) и связываются гепарином (тем самым угнетается пролиферация гладкомышечных клеток). Гепарин ингибирует пролиферацию клеток гладких мышц сосудов, и этот эффект не зависит от его антикоагулянтного действия.
Также известно, что гепарин ингибирует дегрануляцию тучных клеток человека в ответ на различные раздражители и, следовательно, ингибирует высвобождение гистамина. Цитотоксическое действие TNF-α-активированных эозинофилов на эндотелиальные клетки также заметно ингибируется гепарином, как и гомотипическая агрегация и хемотаксис эозинофилов в ответ на фактор комплемента C5a, еще один медиатор воспаления. Кроме того, нефракционированный гепарин ингибирует индуцированную липополисахаридами активацию эндотелиальных клеток (Page С., 2013).
Было установлено, что гепарин связывается с поверхностью нейтрофилов и может ингибировать их дегрануляцию, агрегацию, продукцию супероксидных анионов, активность лизосомальных ферментов и способность нейтрофилов активировать тромбоциты.
Важным компонентом воспалительного ответа являются адгезия (прилипание) воспалительных клеток к эндотелию сосудов и их последующий диапедез (перемещение) в ткани. Таким образом, гепарин ингибирует все стадии миграции провоспалительных клеток в ткани и лейкоцитарно-эндотелиальную адгезию как in vitro, так и in vivo.
В исследованиях был продемонстрирован потенциал гепарина в лечении муковисцидоза, БА и ХОБЛ. У пациентов с аллергическим ринитом после воздействия аллергена местное применение гепарина снижает уровень эозинофилов на слизистой оболочке носа (Page С., 2013).
В настоящее время изучается возможность применения гепарина в терапии онкологических заболеваний. Анализ исследований применения гепарина у больных раком указывает на улучшение показателя выживаемости. Считается, что ингибирование активности гепараназы, P- и L-селектина и тканевого фактора роста гепарином могут способствовать угнетению ангиогенеза и метастазирования (Page С., 2013).
Гепариновая мазь: применение при поверхностном венозном тромбозе
Поверхностный венозный тромбоз (ПВТ) является распространенным заболеванием и фактором риска тромбоэмболических осложнений. В этом отношении важно своевременное обращение пациента за медицинской помощью, установление диагноза и подбор лечения с целью снижения значительных осложнений (de Almeida M.J. еt al., 2019). У 6–40% пациентов ПВТ может сочетаться с тромбозом глубоких вен. Среди его осложнений следует отметить тромбоэмболию легочной артерии (ТЭЛА), которая отмечается в 22–46% случаев ПВТ. При этом в 20–33% случаев ТЭЛА мелких ветвей может иметь бессимптомное течение или маскироваться другими заболеваниями.
ПВТ характеризуется образованием тромбов в поверхностных венах с частичным вовлечением или окклюзией просвета и воспалительной реакцией по ходу вены. Визуально определяется покрасневший, теплый на ощупь тяж по ходу вены. Пациенты жалуются на боль, также наблюдается отек окружающих зону тромбофлебита тканей. Клинический диагноз, как правило, прост, но необходимы дополнительные тесты и обследования для подтверждения распространения тромбоза и возможных тромбоэмболических осложнений (de Almeida M.J. еt al., 2019).
Факторами риска развития ПВТ являются варикозная болезнь, иммобилизация, травма, послеоперационные состояния, период беременности, послеродовой период, злокачественные новообразования, некоторые аутоиммунные заболевания, применение оральных контрацептивов или заместительная гормональная терапия, пожилой возраст, ожирение и ранее перенесенный тромбофлебит.
По данным исследований, местное лечение прямыми антикоагулянтами (гепарином) и НПВП является эффективным в уменьшении выраженности симптомов ПВТ и предупреждении дальнейшего распространения тромбоза (Nisio M.D., 2018).
Местное применение препаратов гепарина обеспечивает не только уменьшение выраженности боли и отека, но и местной воспалительной реакции (de Almeida M.J. еt al., 2019).
Место Гепариновой мази в терапии геморроя
Другим распространенным заболеванием, при котором эффективна Гепариновая мазь, является геморрой. Геморрой считается одним из самых частых неинфекционных заболеваний среди населения. Его истинная распространенность неясна ввиду того, что значительная часть больных не обращаются за медицинской помощью и прибегают к самолечению. В 1990 г., по данным эпидемиологического исследования в США, распространенность геморроя составила 4,4%. В то же время в результате исследования, проведенного в Южной Корее, выявили, что распространенность геморроя — 14,4%. А согласно проведенному в Австрии исследованию распространенность геморроя в этой стране составила 38,8%. Считается, что 25% британцев и до 75% граждан США отмечали симптомы геморроя по крайней мере 1 раз в жизни (Lohsiriwat V., 2015).
Клинически геморрой характеризуется безболезненным ректальным кровотечением при дефекации с или без выпадения слизистой оболочки прямой кишки. Факторами риска геморроя являются период беременности, пожилой возраст, запоры и многие другие, включая сидячий образ жизни, регулярное поднятие тяжестей (из-за повышения внутрибрюшного давления) и наследственность. Как правило, геморрой можно разделить на два типа: внутренний и наружный (Lohsiriwat V., 2015). В результате клинических исследований было установлено, что большая часть симптомов геморроя поддается консервативному лечению (Hall J.F., 2013). Наиболее частым осложнением наружного геморроя является тромбоз геморроидальных узлов. При этом пациенты отмечают увеличение геморроидальных узлов, их болезненность, зуд, дискомфорт в анальной области. Местная терапия гепарином уже многие годы считается неотъемлемым компонентом консервативного лечения геморроя (Ogawa P., de Figueiredo J.C., 1966). Именно применение Гепариновой мази является патогенетически обусловленым в случае тромбоза геморроидальных узлов.
Другие потенциальные возможности применения гепарина, входящего в состав Гепариновой мази
В последние годы установлено, что гепарин может способствовать восстановлению тканей и ингибировать воспаление у пациентов с ожогами.
Флеботоники в терапии хронической венозной недостаточности нижних конечностей
В настоящее время практикующие врачи становятся свидетелями бурного развития фармацевтического рынка в нашей стране. Новые препараты как зарубежного, так и отечественного производства появляются достаточно регулярно. Арсенал фармакологических средств,
В настоящее время практикующие врачи становятся свидетелями бурного развития фармацевтического рынка в нашей стране. Новые препараты как зарубежного, так и отечественного производства появляются достаточно регулярно. Арсенал фармакологических средств, применяемых для лечения того или иного заболевания, постоянно растет, что создает определенные трудности в их выборе. Ситуация еще более осложняется тем, что различные фирмы-производители, как правило, дают свои наименования препаратам, в основе которых лежит одно и то же действующее вещество. В этом обилии информации первостепенно важным является знание и выделение основных звеньев патогенеза заболевания, на основе чего вырабатываются принципы и тактика лечения.
Сегодня все шире распространяется ошибочное мнение о всемогуществе лекарств. Причин для этого много, и не будет преувеличением в качестве основной из них назвать активную рекламу того или иного фармакологического препарата со стороны фирмы-производителя. Вследствие этого многие пациенты, особенно пожилого возраста, принимают с десяток различных препаратов, периодически путаясь в дозировках и частоте их применения, а с каждым посещением врача меняют этот «набор таблеток» и при этом несут весьма ощутимые денежные потери.
Проблема неадекватного назначения лекарственных препаратов не обошла стороной и сферу лечения хронической венозной недостаточности (ХВН) нижних конечностей. Если всего несколько десятилетий назад хирургический метод лечения был ведущим и даже более того считался единственным заслуживающим серьезного внимания, то сейчас нередко наблюдается другая крайность — попытки преподнести фармакотерапию как основу лечения, а остальные методы лечебного воздействия считать дополнением к «фармакотерапевтическому базису».
Учитывая вышесказанное, считаем необходимым определить тактику применения современных флеботропных препаратов у пациентов с ХВН нижних конечностей. Флеботропные препараты являются базисными в лечении ХВН. Безусловно, тяжелые нарушения оттока из нижних конечностей обусловливают необходимость применения препаратов других фармакологических групп — дезагрегантов, нестероидных противовоспалительных средств, антибиотиков, энзимов и др. Однако к их назначению следует подходить с осторожностью, а период их использования должен быть четко ограничен реализацией той или иной задачи лечения.
Основными целями медикаментозного лечения при ХВН нижних конечностей являются: купирование симптомов ХВН, предотвращение осложнений, профилактика в группах риска, предоперационная подготовка, послеоперационная реабилитация.
Исходя из патогенеза ХВН нижних конечностей, задачи консервативной терапии можно представить следующим образом: повышение тонуса венозной стенки, улучшение лимфооттока, воздействие на микроциркуляторные изменения, коррекция гемореологических нарушений, купирование воспалительных проявлений.
Как уже говорилось выше, флеботропные препараты являются основой медикаментозного лечения больных с ХВН. Это достаточно большая группа фармакологических препаратов, обладающих способностью увеличивать венозный отток из нижних конечностей. Данный эффект флеботропных препаратов достигается путем суммирования воздействий на различные звенья микроциркуляторного русла, а у многих из них — прямым действием на сократимость венозной стенки. Безусловно, флеботоническое воздействие следует признать основным эффектом флебопротективных препаратов. Однако все они обладают поливалентным механизмом действия: стимулируют лимфоотток, обладают противовоспалительной активностью, улучшают гемореологию. Именно эта особенность, позволяющая воздействовать на основные звенья патогенеза ХВН, объединила многие препараты в группу флебопротекторов и сделала их базовыми в консервативном лечении пациентов с ХВН нижних конечностей.
Когда следует назначать флеботропные препараты? Показанием к применению флебопротективных средств является наличие симптомов ХВН нижних конечностей. Необходимо сразу предостеречь врачей от весьма распространенной ошибки. Развитие острого нарушения оттока крови при тромбозе вен нижних конечностей не требует применения этой группы фармакологических средств. Более того, использование флеботоников следует считать противопоказанным у пациентов с острым венозным тромбозом. Венозная стенка при остром тромботическом процессе маловосприимчива к флеботоническому воздействию, а его реализация только усугубит остро возникшие нарушения оттока крови.
В дальнейшем, в случае развития посттромботической болезни, когда процессы посттромботической окклюзии и реканализации в различных венозных сегментах уравновесятся, когда сформируются патологические венозные рефлюксы крови и, следовательно, будет иметь место та или иная степень ХВН, показания к назначению флебоактивных препаратов следует считать оправданными.
Безусловным показанием к применению флебопротекторов являются так называемые функциональные (ортостатические и гормонпродуцируемые) флебопатии. В этих случаях изменение образа жизни с исключением продуцирующего фактора, прием флеботоников и эластическая компрессия дают отчетливый положительный эффект.
И наконец, использование флебопротективных препаратов, безусловно, показано при варикозной болезни вен нижних конечностей — заболевании, являющемся наиболее частой причиной развития ХВН.
У пациентов с ранними стадиями варикозной болезни, когда симптомов декомпенсации оттока крови еще нет, а превалируют жалобы эстетического характера, основной целью применения флебопротекторов является главным образом профилактика прогрессирования заболевания. Флеботоники таким пациентам целесообразно назначать короткими (1–1,5 мес) курсами. Интервал между курсами фармакотерапии должен составлять 3–4 нед.
Появление отеков нижних конечностей — достоверный признак декомпенсации оттока крови. У больных с отечным синдромом задачами фармакотерапии являются: купирование проявлений ХВН (отеков, тяжести в нижних конечностях), улучшение лимфооттока, коррекция микроциркуляторных расстройств, профилактика прогрессирования заболевания. Больным с декомпенсацией оттока крови флеботоники назначают более длительными курсами (2–2,5 мес). Временной интервал между курсами не должен превышать 1 мес.
У пациентов с трофическими расстройствами мягких тканей нижних конечностей следует особо тщательно подходить к выбору программы консервативной терапии. Выраженность трофических изменений кожи диктует необходимость назначения препаратов, относящихся к различным фармакологическим группам, а стадийность раневого процесса и склонность больных к аллергическим реакциям — тщательного индивидуального подбора лекарственных средств. Показания к применению различных групп препаратов зависят от многих факторов, в том числе от стадии и тяжести течения заболевания, риска развития осложнений. Средства медикаментозного лечения должны назначаться в зависимости от фазы раневого процесса.
На первом этапе, когда преобладают проявления острого воспаления и деструкции мягких тканей, основными целями применения фармакологических препаратов являются быстрое устранение симптомов воспаления, борьба с инфекцией. В этот период проводят терапию нестероидными противовоспалительными средствами (диклофенак, индометацин, кетопрофен, мелоксикам и др.), дезагрегантами (ацетилсалициловая кислота, дипиридамол, клопидогрель), антигистаминными препаратами (кетотифен, клемастин, прометазин), антиоксидантами (витамин Е, эмоксипин, милдронат). Длительное время считалось, что для применения антибиотиков абсолютным показанием служит наличие трофической язвы нижних конечностей. В настоящее время взгляды на эту проблему несколько изменились. Показания к проведению антибактериальной терапии: обширные трофические нарушения, протекающие с выраженным перифокальным воспалением, наличие гнойного отделяемого из трофической язвы. Местное применение антибиотиков в настоящее время признано неэффективным. С учетом микробного пейзажа наиболее эффективными антибактериальными средствами являются полусинтетические пенициллины, цефалоспорины II, III поколений, фторхинолоны. Применение флеботропных препаратов в этот период считаем нецелесообразным.
Таким образом, основные цели фармакотерапии ХВН нижних конечностей в стадии трофических расстройств на первом этапе — это купирование воспаления в зоне трофических расстройств, лечение осложнений, остановка процесса деструкции тканей. Основные средства: антиагреганты, антибиотики, антигипоксанты, нестероидные противовоспалительные средства, антигистаминные препараты.
На втором этапе, когда остановлен процесс деструкции тканей и купированы явления острого воспаления, основной задачей фармакотерапии является коррекция микроциркуляторных расстройств. На данном этапе необходимо создать условия для «старта» регенерации тканей, перехода от катаболической фазы в фазу анаболизма. В этот период назначают поливалентные флеботропные препараты, а также продолжают применение дезагрегантов и антиоксидантную терапию.
Итак, основными целями фармакотерапии при ХВН нижних конечностей в стадии трофических расстройств на втором этапе являются: инициирование процессов репарации тканей, уменьшение симптомов венозной недостаточности. Основные средства: флеботропные препараты, антиагреганты, антиоксиданты.
Полное купирование воспалительных проявлений, начало активной эпителизации язвенного дефекта свидетельствуют об успешности проводимого лечения, и на этом, третьем этапе основная цель — это закрепление достигнутых эффектов, а основное средство — флеботропные препараты.
Необходимо отметить, что эффективное лечение ХВН нижних конечностей возможно лишь при использовании комплексного лечебного подхода с применением хирургических методов, эластической компрессии и современных фармакологических средств. Поэтому флеботропные препараты целесообразно использовать как до операции, так и в комплексе послеоперационного реабилитационного лечения.
Ниже мы более подробно остановимся на некоторых современных флебопротекторных препаратах, собственный опыт использования которых позволяет нам рекомендовать их для применения в лечении больных ХВН нижних конечностей.
В состав препарата детралекса входят 450 мг диосмина и 50 мг гесперидина.Основными механизмами действия данного препарата при ХВН являются: повышение тонуса вен, купирование воспалительных реакций, стимуляция лимфооттока, устранение микроциркуляторных расстройств.
По нашим данным, применение детралекса у более чем 250 пациентов с начальными формами ХВН в большинстве случаев (83%) вызывает существенное клиническое улучшение, а также оказывает положительное влияние на гемодинамику вен и эффективность икроножного насоса. Необходимо отметить также высокую безопасность данного флеботропного препарата. Даже при длительном (12 мес) приеме детралекса побочные проявления возникали крайне редко, переносимость лечения оценивали как умеренную и высокую 93% больных.
При исследовании микроциркуляторного кровотока с помощью лазерной допплеровской флоуметрии удалось выявить, что к окончанию курса консервативного лечения у пациентов с варикозной болезнью отмечается достоверное повышение исследуемого показателя, свидетельствующее об усилении перфузии мягких тканей (рис.).
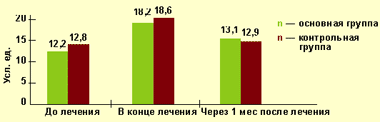 |
| Рисунок. Динамика индекса микроциркуляции в основной и контрольной группах в различные сроки лечения |
Препарат гинкор форт содержит 14 мг экстракта гингко билоба, 300 мг троксерутина и 300 мг гептаминола гидрохлорида. Экстракт гингко билоба обладает антиоксидантным, антигипоксическим действием, реализующимся за счет подавления синтеза и высвобождения медиаторов воспаления и реакций окисления с участием свободных радикалов кислорода. Антиагрегационный и ангиопротекторный эффект препарата обусловлен подавлением выработки фосфодиэстеразы, что приводит к накоплению в гладких клетках циклогуанидинаминофосфорной кислоты и снижению тонуса артериол. Троксерутин относится к группе рутозидов. Его ангиопротективный эффект реализуется за счет блокирования гиалуронидазы и достигающейся тем самым стабилизации гиалуроновой кислоты — одной из основных составляющих клеточных мембран и межуточного вещества. Гептаминол, помимо воздействия на основной фактор венозного возврата — «мышечно-венозную помпу», повышает сократительную активность правых камер сердца, способствует адекватной оксигенации крови и защищает эндотелий сосудов от гипоксии.
Важной особенностью препарата гинкор форт является возможность его применения во II и III триместрах беременности. Проведенные исследования подтвердили эффективность этого препарата, применяющегося для купирования симптомов ХВН во время беременности.
В последнее время на отечественном рынке появился новый флеботропный препарат — антистакс. Действующим веществом данного лекарственного средства является экстракт красных листьев винограда, содержащий фармакологически активные биофлавоноиды, основными из которых являются кверцетин-глюкоронид и изокверцетин. Препарат оказывает защитное действие на эпителий сосудов, стабилизируя мембраны, увеличивает эластичность сосудов, нормализуя сосудистую проницаемость. Снижение проницаемости сосудистой стенки для плазмы, белков и воды из сосудов в окружающую ткань замедляет образование отеков и уменьшает уже существующие отеки.
Препарат выпускается в виде капсул, содержащих 180 мг действующего вещества. Показанием к применению являются начальные формы ХВН, проявляющиеся синдромом «тяжелых ног«, отеками, снижением толерантности к статическим нагрузкам. Препарат принимают по 1 капсуле 2 раза в сутки.
В зарубежной литературе опубликованы результаты нескольких крупных клинических исследований, посвященных эффективности препарата антистакса, применяющегося в лечении больных ХВН. Показано его положительное влияние на купирование отечного синдрома (по данным волюметрии) и других проявлений ХВН (боль, усталость, тяжесть в ногах).
Начальный опыт использования антистакса в отечественной клинической практике можно признать обнадеживающим. Следует отметить хорошую переносимость этого препарата и отсутствие значимых побочных эффектов.
Таким образом, современные флеботропные препараты благодаря поливалентному механизму действия, высокой биодоступности, незначительно выраженным побочным эффектам являются эффективным средством фармакологической коррекции ХВН. Их использование в комплексе с хирургическим лечением, эластической компрессией, склеротерапией, физиотерапией позволяет достичь хороших результатов в лечении пациентов с хроническим нарушением оттока крови из нижних конечностей.
Ю. М. Стойко, доктор медицинских наук, профессор
Н. А. Ермаков, кандидат медицинских наук
НМХЦ им. Н. И. Пирогова, Москва