Симптомы нетипичные это как
Нетипичные симптомы сердечно-сосудистой патологии
В статье представлены варианты течения сердечно-сосудистой патологии с преобладанием клинической симптоматики гастроэнтерологических, бронхолегочных и неврологических заболеваний. Приведены клинические примеры нетипичной симптоматики. Рассмотрены основные
The article presents variants of cardiovascular pathology with prevalence of clinical symptoms of gastrointestinal, broncho-pulmonary, and neurological diseases. The author analyzes clinical examples of atypical symptoms and main problems of differential diagnostics in these patients.
Каждый практикующий врач, независимо от специальности, регулярно встречается со сложными случаями заболеваний, протекающих с нетипичной симптоматикой. Нехарактерные проявления зачастую становятся причиной поздней диагностики и несвоевременного начала адекватной терапии, что существенно ухудшает прогноз и увеличивает частоту летальных исходов среди таких больных. Патология сердечно-сосудистой системы чаще других протекает с различными симптомами, типичными для другой локализации нарушений. Причина этого заключается в том, что сердечная мышца и сосуды обеспечивают кровотоком с необходимыми питательными веществами и кислородом все органы. Недостаточное поступление крови закономерно сопровождается нарушениями функционирования той или иной ткани, что проявляется симптоматикой соответствующей локализации.
Пациенты не всегда ощущают хорошо известные, типичные для поражения коронарных артерий, приступы интенсивных загрудинных болей [1]. Локализация может быть иной: как в других отделах грудной клетки, так и в области плечевых суставов, в животе. Непосредственная близость сердечной мышцы к органам, находящимся в эпигастрии, становится причиной болевого синдрома в верхних отделах живота, что может наблюдаться при расширении желудочков сердца на фоне ишемии миокарда, кардиосклероза, некоторых нарушений ритма сердца, порока или кардита [2, 3]. Снижение фракции выброса левого желудочка, независимо от непосредственной причины, вызывает недостаточность кровоснабжения всех органов брюшной полости, что формирует соответствующую патологию: ишемические энтероколит, гастрит, панкреатит, гепатит [4]. Нарушение функции этих органов в той или иной степени сопровождается тошнотой, иногда — рвотой, изменениями стула, болевым синдромом, что нередко становится поводом для обращения к гастроэнтерологу. Результаты эндоскопического, ультразвукового и лабораторного обследования выявляют отклонения в соответствии с той или другой патологией. Однако стандартная терапия, в отсутствие адекватного лечения кардиологического заболевания, не дает ожидаемого результата.
В качестве иллюстрации течения ишемического гастроэнтероколита на фоне ишемической болезни сердца привожу клинический пример № 1.
Мужчина Я., 46 лет, обратился к терапевту с жалобами на появление коликообразных болей по всему животу с императивными позывами к дефекации при занятиях бегом, что требовало прекращения нагрузки. В течение нескольких часов после тренировки обращал внимание на неоформленный кашицеобразный стул 2–3 раза в течение нескольких часов.
Из анамнеза: боли появились впервые около недели назад. В этот период отметил нарастание утомляемости, но одышку и сердцебиения отрицает. Ранее активными занятиями спортом на любительском уровне занимался регулярно, в течение 25 лет, в соревнованиях не участвовал. Ежегодное плановое обследование в рамках диспансеризации проходил регулярно, хронической патологии ранее выявлено не было, препаратов для постоянного приема не назначали.
При осмотре: состояние удовлетворительное. Кожные покровы немного бледные. Отеков нет. Аускультативно дыхание везикулярное, хрипов нет, частота дыхательных движений — 17 в минуту. Тоны сердца слегка приглушены, 78 ударов в минуту, ритмичны, шумов не выслушивается. Артериальное давление — 125/80 мм рт. ст. Живот мягкий, печень не увеличена. Предварительный диагноз: синдром раздраженного кишечника. Назначено дополнительное обследование: анализы крови клинический и биохимический; анализы кала: копрограмма, бактериологический и на дисбактериоз; ультразвуковое исследование органов брюшной полости, эзофагогастродуоденоскопия (ЭГДС), колоноскопия. Терапия: лоперамид 2 мг — по 2 капсулы 2 раза в день, пробиотики, седативная фитотерапия.
По результатам дополнительного обследования: в анализе крови клиническом отклонений от нормы нет. В анализе крови биохимическом: холестерин общий — 5,6 ммоль/л, липопротеиды низкой плотности — 4,3 ммоль/л, триглицериды — 3,2 ммоль/л, аспартатаминотрансфераза — 56 ЕД/л, аланинаминотрансфераза — 21 ЕД/л, общий билирубин — 13 мкмоль/л. В анализах кала: обнаружены остатки непереваренной пищи, умеренное количество перевариваемой клетчатки, в остальном — без патологии, патогенных возбудителей и дисбиотических изменений нет. По данным ультразвукового исследования органов брюшной полости также патологических изменений не выявлено. По результатам ЭГДС: хронический гастрит, патологогистологическое заключение: хронический умеренно выраженный неактивный гастрит без атрофии и метаплазии, тест на хеликобактер — отрицательный. По результатам колоноскопии: патологии не выявлено.
Через 7 дней, несмотря на регулярный прием назначенных препаратов, жалобы сохраняются.
В связи с отсутствием эффекта от лечения, значимых данных за гастроэнтерологическое заболевание, но вместе с тем повышением аспартатаминотрансферазы при нормальных значениях аланинаминотрансферазы и общего билирубина [5, 6], назначено электрокардиографическое исследование (ЭКГ).
На ЭКГ: ритм синусовый, 74 удара в минуту, нормальное положение электрической оси сердца, суправентрикулярная и вентрикулярная экстрасистолия. Для уточнения характера нарушения ритма проведено холтеровское мониторирование ЭКГ.
По анализу записи выявлена частая суправентрикулярная и вентрикулярная экстрасистолия 4б/5-го типа по Лауну–Райяну, преимущественно на фоне физических нагрузок, эпизоды синусовой тахикардии. Зарегистрировано 7728 суправентрикулярных экстрасистол, в том числе куплетов — 25, а также 5458 полиморфных (3-го типа) вентрикулярных экстрасистол, в том числе куплетов — 12, триплетов — 4.
На рис. 1 показан участок записи суточного мониторирования ЭКГ, содержащий суправентрикулярную и вентрикулярные экстрасистолы в изолированном виде, а также триплет. Пример выявленных вентрикулярных куплетов представлен на рис. 2, а суправентрикулярных — на рис. 3. На участке записи ЭКГ во II стандартном отведении в течение 1,5 минут (рис. 4) видна частая экстрасистолия, зарегистрированная у этого пациента.
По данным эхокардиографии (проведена на фоне частой экстрасистолии): фракция выброса 52% (по Тейхольцу), гипертрофия межжелудочковой перегородки (18 мм), нарушение диастолической функции левого желудочка I типа, зон локальной гипокинезии и акинезии не выявлено, данных за порок сердца нет.
При дополнительном исследовании в сыворотке крови: МВ-креатинкиназа — 18 ЕД/л, тропонин I — отрицательный, С-реактивный белок — 7 мг/л, обнаружены антимиофибриллярные антитела к миокарду в титре 1:80, что свидетельствует о воспалительном процессе в миокарде.
На основании полученных данных сформулирован диагноз: вероятный миокардит, суправентрикулярная и вентрикулярная экстрасистолия. Диагноз подтвержден по результатам магнитно-резонансной томографии сердца с контрастированием и ЭКГ-синхронизацией, что соответствует современным требованиям диагностики этих заболеваний [7].
Таким образом, представленный пример демонстрирует возможность течения кардиологической патологии с симптомами, более характерными для гастроэнтерологического заболевания. Однако появление или нарастание жалоб при увеличении физической нагрузки указывает на сердечную недостаточность как непосредственную причину. Снижение кровоснабжения органов желудочно-кишечного тракта может происходить при снижении фракции выброса левого желудочка как за счет самого воспалительного процесса в сердечной мышце, так и независимо от этого, вследствие частой вентрикулярной экстрасистолии. В других случаях это возможно и при нарастании коронарной недостаточности у пациентов с ишемической болезнью сердца. С целью дифференциальной диагностики необходимо обращать внимание на состояние кожных покровов, возможные отеки, при аускультации — на снижение звучности тонов сердца, новые шумы или нарушения ритма [8]. Это, несомненно, снизит вероятность ошибочного диагноза.
Нетипичная картина при кардиологической патологии может развиваться с преобладанием и совершенно других симптомов. Нарушение кровоснабжения головного мозга на фоне различной патологии сердца проявляется типичными для дисциркуляторной энцефалопатии жалобами на головокружения, иногда — обморочные состояния, неустойчивость при ходьбе, ухудшение восприятия информации и запоминания, шум или звон в ушах [9]. Возможно ухудшение зрения и/или слуха. В некоторых случаях: при эндокардитах с образованием вегетаций на клапанах и внутренней стенке левого желудочка, при мерцательной аритмии выраженной дилатации камер сердца с отсутствием адекватной антитромботической терапии, ухудшение состояния пациента связано с тромбоэмболией. В таких ситуациях клиническая картина, как правило, соответствует острому нарушению мозгового кровоснабжения, что подтверждается результатами компьютерной или магнитно-резонансной томографии. Также, как и при гастроэнтерологических проявлениях, для купирования неврологической симптоматики необходимо применение в первую очередь адекватных схем лечения кардиологической патологии.
Снижение кровоснабжения почек закономерно приводит к формированию почечной недостаточности, что сопровождается характерными сдвигами, в первую очередь, в лабораторных показателях: повышением креатинина и мочевины в сыворотке крови. Нередко присоединяются и другие отклонения: гиперкалиемия, гиперурикемия, гиперкальциемия. Жалобы на слабость, кожный зуд, отеки с преимущественной локализацией в области лица и с максимальной выраженностью после сна, появляются, как правило, позднее. Признаки почечной недостаточности у пациентов с кардиологической патологией, сопровождающейся снижением фракции выброса, возможны в отсутствие какого-либо самостоятельного заболевания паренхимы почек или чашечно-лоханочной системы. Успешная коррекция показателей работы сердца у таких больных приводит к значимому улучшению функции почек и купированию клинической симптоматики.
Практика показывает, что пациенты с кардиологической патологией зачастую предъявляют жалобы на боли в суставах, спине, мышцах. Нормализация фракции выброса левого желудочка и купирование реологических нарушений во многих случаях приводит к заметному улучшению субъективных и объективных характеристик двигательной функции и выраженному снижению интенсивности болевого синдрома.
Левожелудочковая сердечная недостаточность при любой патологии сердца закономерно сопровождается накоплением объема крови в малом круге кровообращения. Пациентов обычно беспокоит сухой или влажный кашель, иногда — с прожилками крови [1, 10]. Хорошо известно, что чаще всего это проявляется влажными незвучными хрипами, аускультирующимися над нижними отделами легких. Однако могут быть и другие варианты симптоматики, что существенно затрудняет дифференциальную диагностику. У больных, находящихся большую часть времени в горизонтальном положении, хрипы достаточно часто распространяются на все отделы грудной клетки, что необходимо дифференцировать с развивающимся отеком легких. Появление жидкости в альвеолах дает крепитацию, а накопление в тканях может приводить к сдавлению с сужением просвета бронхов мелкого калибра, что сопровождается обструктивными свистящими хрипами. Такая ситуация оказывается наиболее сложной, поскольку развивается вся характерная для бронхообструктивного синдрома симптоматика: экспираторная одышка со свистящим выдохом и достоверные признаки обструкции по результатам проведенной оценки функции внешнего дыхания. Отличительным признаком, на который следует обращать особое внимание, является незначительный или неполный эффект от стандартно применяемых в таких ситуациях бронхолитиков. В некоторых случаях, за счет развивающейся на их фоне тахикардии и закономерной ишемии миокарда, происходит ухудшение самочувствия с нарастанием одышки или болевым синдромом.
В качестве иллюстрации другого варианта нетипичного, но вместе с тем закономерного течения кардиологической патологии привожу клинический пример № 2.
Мужчина К., 39 лет, обратился к терапевту с жалобами на приступообразный сухой кашель, одышку при ходьбе в умеренном темпе смешанного характера, головокружения.
Из анамнеза: ухудшение самочувствия отмечает в течение 3 недель, когда появилось покашливание, утомляемость при ходьбе. Самостоятельно принимал растительные отхаркивающие препараты, но без эффекта. Ранее подобные симптомы беспокоили при острых респираторных заболеваниях. Однако, в отличие от предыдущих эпизодов, в этот раз ни насморка, ни болей в горле, ни повышения температуры тела не было. Курение и другие вредные привычки отрицает. Аллергических реакций не было. Хронической патологии ранее не выявляли.
При осмотре состояние ближе к среднетяжелому. Температура тела — 36,7 °C. Вес избыточный (122 кг при росте 182 см) Умеренная пастозность ног. Кожные покровы слегка бледные, цианоз губ. Аускультативно дыхание жесткое, проводится во все отделы, рассеянные свистящие хрипы в небольшом количестве, в нижних отделах — влажные незвучные хрипы с обеих сторон. Частота дыхательных движений — 22 в минуту. Тоны сердца приглушенные, аритмичные, частота сердечных сокращений — 106 ударов в минуту. Артериальное давление — 128/92 мм рт. ст. Живот мягкий, печень +2 см от края реберной дуги.
Предварительный диагноз: острый обструктивный бронхит.
Назначено дополнительное обследование, терапия: азитромицин 500 мг в сутки, пробиотики, ингаляции с Беродуалом 4 раза в день, Лазолван 90 мг в сутки.
По полученным данным определено: в анализе крови клиническом — без патологических отклонений; в биохимическом — холестерин общий — 6,8 ммоль/л, липопротеиды низкой плотности — 4,9 ммоль/л, триглицериды — 4,2 ммоль/л, креатинин — 145 мкмоль/л, мочевина — 12,3 мкмоль/л. На рентгенограмме отмечается усиление сосудистого рисунка, признаки застойных явлений в малом круге кровообращения, выраженное увеличение сердца в поперечнике: кардиоторакальный индекс = 72%.
На фоне лечения через 5 дней пациент отмечает ухудшение самочувствия, в связи с чем проводится дальнейшее обследование с целью определения состояния сердца.
На ЭКГ зарегистрирован неправильный суправентрикулярный ритм с частотой 102–140 в минуту, фибрилляция предсердий, нарушение реполяризации (депрессия ST до 1,5 мм) в боковых отделах.
По результатам эхокардиографии, фракция выброса левого желудочка (по Тейхольцу) 44%, выраженная дилатация предсердий, умеренная дилатация желудочков. Данных за порок сердца нет.
С учетом выявленных изменений поставлен диагноз: фибрилляция предсердий неизвестной давности, кардиомиопатия (?) неясной этиологии, недостаточность кровообращения II Б стадии по Стражеско–Василенко, III функционального класса по NYHА [1, 10]. Восстановление ритма не показано в связи с дилатацией предсердий.
Назначено лечение в соответствии с полученными данными: ривароксабан, карведилол начиная с малых доз; спиронолактон, торасемид, поддерживающая доза дигоксина с коррекцией по частоте сердечных сокращений. На фоне этой терапии самочувствие пациента значительно улучшилось. Кашель и головокружения не беспокоят. Бытовые физические нагрузки переносит значительно лучше.
При осмотре через 3 недели: состояние удовлетворительное. Отеков нет. Кожные покровы обычной окраски. Аускультативно: дыхание везикулярное, хрипов нет. Частота дыхательных движений — 16 в минуту. Тоны сердца приглушенные, аритмичные, частота сердечных сокращений — 70 ударов в минуту. Артериальное давление — 118/82 мм рт. ст. Печень +1 см от края реберной дуги.
В ходе дальнейшего обследования была проведена магнитно-резонансная томография сердца с контрастированием, которая подтвердила наличие у пациента дилатационной кардиомиопатии.
Представленный пример показывает возможность нетипичных для кардиологической патологии симптомов, закономерно сопровождающих тяжелую патологию сердца в отсутствие какого-либо значимого иного заболевания.
Таким образом, кардиологические заболевания закономерно могут протекать с симптомами патологии других органов и систем. Правильный диагноз возможно поставить при тщательном анализе данных анамнеза, осмотра и результатов дополнительного обследования.
Литература
Т. А. Руженцова, доктор медицинских наук
ФБУН ЦНИИ эпидемиологии Роспотребнадзора, Москва
Редкие и атипичные синдромы и заболевания
Редкие (орфанные) заболевания — это группа патологий с небольшой распространенностью каждой из них в общей популяции.
Орфанные заболевания характеризуются широким разнообразием симптомов и признаков, причем у пациентов, страдающих одной и той же редкой патологией, симптомы и признаки могут сильно различаться. Несмотря на низкую распространенность в общей популяции какой-то одной редкой болезни, группа орфанных патологий включает около 7 000 заболеваний. Таким образом, в совокупности, редкими болезнями и синдромами во всем мире страдают сотни тысяч людей.
Распространенность каждого орфанного заболевания в общей популяции не превышает 1 пациента на 2 000 человек — это критерий, принятый в Европейском союзе. В России редкими предлагается считать заболевания «с распространенностью не более 10 случаев на 100 000 населения» — 1 пациент на 10 000 человек.
Многие редкие заболевания являются генетическими и, следовательно, наблюдаются уже в момент рождения ребенка или в раннем детстве (хондродисплазии, проксимальная спинальная мышечная атрофия, нейрофиброматоз, несовершенный остеогенез, муковисцидоз, синдром Ретта). Однако более 50% орфанных заболеваний проявляются в зрелом возрасте, например: болезнь Хантингтона, болезнь Крона, боковой амиотрофический склероз, саркома Капоши, рак щитовидной железы. Существуют и редкие заболевания, которые имеют инфекционную природу, например: некоторые аутоиммунные патологии и редкие виды рака.
На сегодняшний день причины возникновения большинства орфанных заболеваний неизвестны. Лечения для многих редких синдромов и болезней также не существует. Тем не менее, в последние годы медицина достигла значительных успехов в диагностике, лечении и даже предотвращении некоторых из них.
Значимость орфанных заболеваний определяется не только большим количеством страдающих от них людей, но и высокой стоимостью лекарств для патогенетической терапии. Однако для подавляющего числа редких болезней и синдромов лекарственных препаратов, воздействующих на причину их развития, не существует. Поэтому многие пациенты вынуждены ограничиваться симптоматической терапией, что говорит о высокой социальной значимости орфанных заболеваний. Кроме того, летальность некоторых редких патологий — например, с выраженными нарушениями метаболизма — достигает высоких показателей, и часть пациентов с такими нарушениями не доживает до совершеннолетия.
Нередко нетипичная клиническая картина, недостаточная осведомленность части врачей о проявлениях орфанных заболеваний, трудности с адекватным лабораторным тестированием приводят к поздней диагностике редких болезней и синдромов и их неправильному лечению.
В своей практике врач любой специальности может столкнуться как с редкими заболеваниями, так и с атипичными проявлениями часто встречающейся патологии. Так, хирург может столкнуться с атипичным характером болевого синдрома при остром аппендиците в случае тазового расположения аппендикса, гастроэнтеролог или терапевт — с нетипичными проявлениями гастроэзофагеальной рефлюксной болезни (чувство комка в горле, кашель, нарушения сердечного ритма), кардиолог — с атипичным болевым синдромом при инфаркте миокарда (боль в области нижней челюсти, в верхних отделах живота). В связи с этим, задачей врача любой специальности является своевременное распознавание атипичных и редких синдромов и определение дальнейшей тактики ведения.
Врачи клиники Рассвет уделяют большое внимание самоподготовке и изучению сложных и редких заболеваний, что позволяет своевременно диагностировать и лечить орфанные патологии и, в то же время, выявлять частые заболевания с атипичной (необычной) картиной течения.
Атипичные клетки – это рак или нет?
Атипичные клетки – это такие клетки, которые под воздействием различных неблагоприятных факторов из обычной нормальной клетки человеческого организма преобразовались в нехарактерную структуру, изменили свой размер и форму. Организм в свою очередь теряет контроль над такими клетками, поэтому существует риск перерождения атипических клеток, что может привести к образованию рака.
Что может повлиять на образование атипичных клеток:
Это некоторые факторы, которые могут привести к образованию атипичных клеток. К сожалению, точной причины их возникновения сказать никто не может. Даже какой-то незначительный сбой в организме может привести к возникновению не одной и даже не двух таких клеток, а тысяч.
Как происходит перерождение атипичных клеток в рак
Давно известно, что образование клеток с измененной ДНК появляются постоянно. Но появление атипичных клеток не всегда приводят к раку. В нашем организме есть защитный механизм, процесс старение и уничтожение клеток, так называемый апоптоз. Он отвечает за то, чтобы аномальные клетки исчезали из организма. Но любая система может дать сбой, и в результате атипичные клетки затаятся в организме. При таком раскладе есть вероятность их перерождения в раковые клетки.
Что делать, если обнаружили атипичные клетки во время биопсии? Рак это или нет?
В такой ситуации лучше перестраховаться, чем что-то пропустить. Ведь ранняя диагностика рака может спасти вам жизнь.
Иногда врач назначает какое-то конкретное лечение, чтобы постараться остановить образование атипичных клеток. Либо может понадобиться еще один образец ткани – дополнительная биопсия, чтобы быть уверенным в отсутствии рака или какого-то другого заболевания.
«Я потерял нюх к жизни…», или Как возникает зáпаховая слепота при новой коронавирусной инфекции
«Я потерял нюх к жизни…», или Как возникает зáпаховая слепота при новой коронавирусной инфекции
коллаж автора статьи
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: До появления нового коронавируса SARS-CoV-2 сложно было представить себе, каково это — не ощущать ароматы самых привычных нам вещей: утреннего кофе, полевых цветов, любимых духов. Явление частичной или полной потери обоняния (гипо- и аносмия) наблюдается у 2/3 пациентов с COVID-19. Поскольку обоняние — это важный инструмент взаимодействия с окружающим миром, лишение этого чувства также называют обонятельной, или зáпаховой, слепотой. Попробуем разобраться, каким же образом новый вирус лишает нас самого древнего в эволюционном плане чувства.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Как устроена система обоняния
Обоняние — крайне важное чувство, позволяющее животным ориентироваться и выживать в окружающем мире. Для большинства животных это чувство имеет первостепенную важность: такие организмы называют макросматиками, поскольку они обладают развитым обонянием. Существуют и такие животные, у которых обоняние практически отсутствует (например дельфины). Человека, приматов и грызунов считают микросматиками из-за слабо развитой обонятельной системы. Для нас важны зрение, слух и осязание, и только потом — обоняние. Однако лишившись способности воспринимать ароматы, мы понимаем, какую огромную роль в нашей жизни играет это чувство. Для начала разберемся, как устроена система обоняния.
Чувство обоняния наряду с чувством вкуса относится к системе хеморецепции, то есть восприятию химических веществ из окружающей среды [1]. Структуры, участвующие в восприятии и анализе запахов, вместе составляют обонятельную сенсорную систему (рис. 1).
Рисунок 1. Как работает обонятельная система человека
коллаж автора статьи, изображения из открытых источников и из [12]
Каждый аромат имеет сотни пахучих молекул, которые улавливаются обонятельными рецепторами, причем каждый обонятельный сенсорный нейрон распознает несколько разных одорантов, а каждый одорант активирует несколько разных нейронов. Выходит так, что каждый одорант активирует определенную комбинацию рецепторов, будто воспроизводит аккорд на нашей обонятельной «клавиатуре». В результате ароматы звучат как целый оркестр в нашем головном мозге [2].
Для того чтобы рецепторные нейроны качественно выполняли свою функцию, в обонятельном эпителии содержатся стентакулярные (поддерживающие, или опорные) и базальные (горизонтальные и шаровидные) клетки. Первые удаляют мертвые нейроны, токсичные агенты и поддерживают водный и солевой баланс в слизи. Стоит нарушить этот баланс — и распознавание одоранта ресничками не произойдет. Функция базальных клеток не менее важна — они ответственны за регенерацию обонятельного эпителия (как в норме, так и при повреждении), то есть непрерывно производят новые обонятельные клетки, продолжительность жизни которых составляет 6–8 недель.
Вернемся к обонятельным рецепторам. После связывания одоранта с рецепторами обонятельных нейронов нервный импульс распространяется по аксону, чтобы передать информацию дальше в центры головного мозга. Аксоны проходят сквозь слой соединительной ткани (lamina propria), затем через отверстия решетчатой кости, отделяющей носовую полость от полости черепа, и достигают обонятельной луковицы, которая служит первым центром обработки обонятельной информации в головном мозге [3]. Здесь разветвленные окончания аксонов обонятельных нейронов взаимодействуют с дендритами нейронов второго порядка, формируя сферические структуры — клубочки. За обработку сигналов всех обонятельных клеток одного типа отвечает один и тот же клубочек обонятельной луковицы. Этот важный факт установили ученые Линда Бак и Ричард Эксел, получившие в 2004 году Нобелевскую премию за исследования обонятельных рецепторов млекопитающих.
К нейронам второго порядка относят крупные митральные и более мелкие пучковые клетки, несущие информацию о запахах по обонятельному тракту в кору головного мозга. Можно представить себе масштабность процесса проведения нервного импульса в обонятельной системе, узнав численное соотношение разных участников этой эстафеты. У человека имеется около 2000 клубочков, в каждом из которых формируются контакты между 25 000 аксонов обонятельных рецепторов и дендритами 45 митральных и 60 пучковых клеток [1].
По обонятельному тракту информация о запахе распространяется к высшим центрам обработки информации — к различным структурам переднего мозга (переднему обонятельному ядру, миндалине, ядрам перегородки, ядрам гипоталамуса, гиппокампу, препириформной коре и др.), большинство из которых рассматриваются как ассоциативные центры. Они связывают обонятельную систему с другими сенсорными системами, тем самым организуя сложные формы поведения — пищевого, полового, оборонительного и т.д. [1]. Не раз мы на собственном опыте убеждались, что ароматы способны пробуждать эмоции и воспоминания.
Выделяют три центра обработки обонятельной информации в головном мозге: древнюю обонятельную систему (обеспечивает рефлексы на запаховые раздражители), старую (отвечает за выбор пищи, пригодной к употреблению, и за отказ от токсических веществ) и новую (отвечает за осознанное восприятие и анализ обонятельной информации) [1].
Как возникает зáпаховая слепота при COVID-19
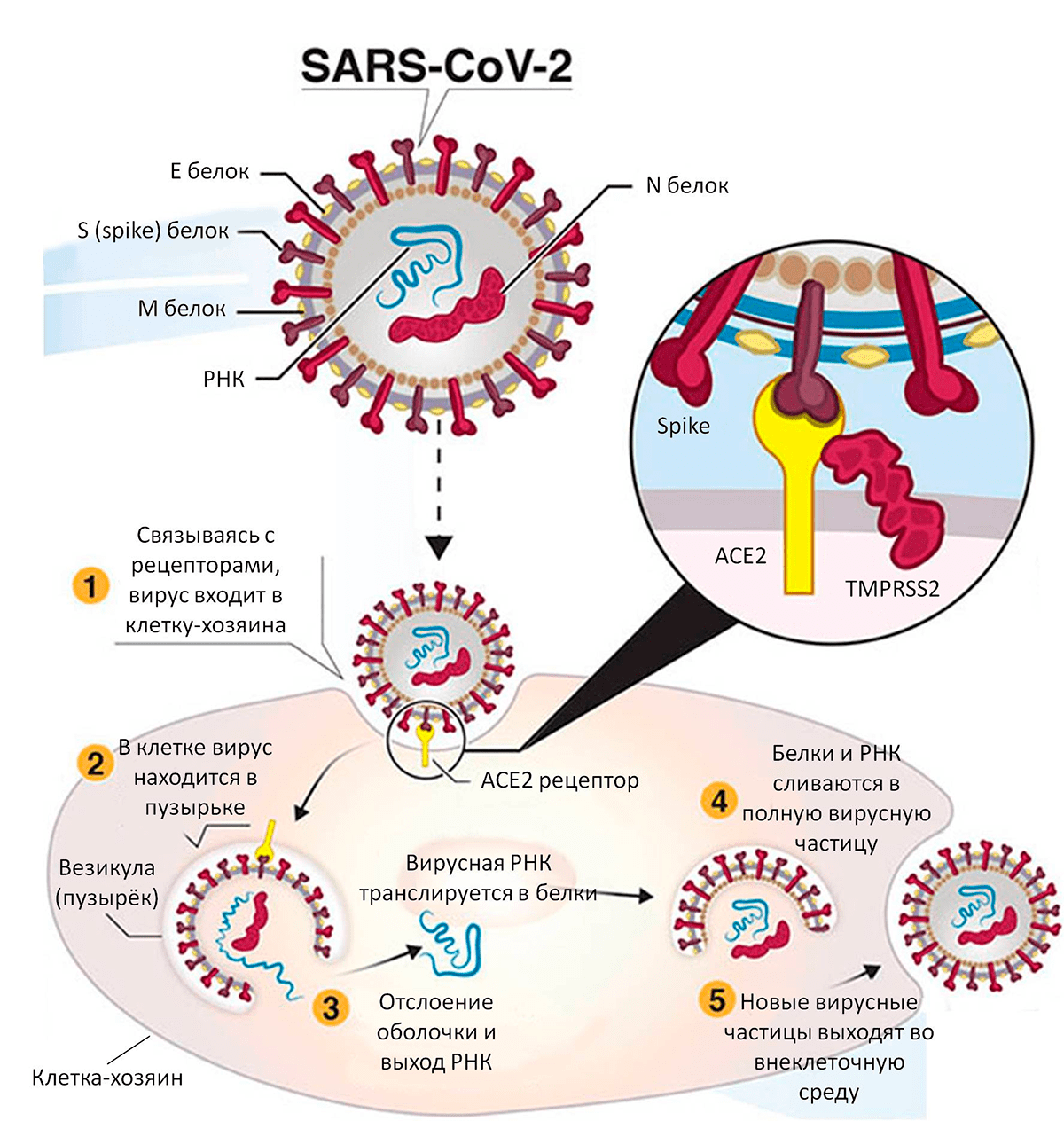
Больше года назад появились сообщения о вспышке острой респираторной инфекции в Китае, возбудителем которой оказался новый коронавирус SARS-CoV-2. Болезнь назвали коронавирусной инфекцией 2019 года (COVID-19). Подробнее об этом, а также строении и жизненном цикле вируса вы можете прочитать в статьях «Биомолекулы» [4], [5] (рис. 2).
Рисунок 2. Жизненный цикл SARS-CoV-2, вызывающего COVID-19. SARS-CoV-2 передается воздушно-капельным путем от инфицированных людей и попадает в слизистую оболочку полости рта и дыхательных путей. Вход в клетку-мишень (увеличенное изображение) осуществляется через взаимодействие белка Spike и рецептора ACE2 с последующим расщеплением первого мембранной протеазой TMPRSS-2.
SARS-CoV-2 — это содержащий одноцепочечную РНК вирус с похожими на зубцы короны S-гликопротеинами на поверхности. У 85,6% инфицированных вирусом SARS-CoV-2 людей наблюдается нарушение обонятельной функции [6], или зáпаховая (обонятельная) слепота, — она может проявляться в виде утраты чувства обоняния (аносмии) или его снижения (гипосмии).
В современной неврологии обонятельная дисфункция описана при нейродегенеративных заболеваниях: при болезни Альцгеймера, болезни Паркинсона, хорее Хантингтона [7]. При воздействии других респираторных вирусов также может наблюдаться потеря или снижение обоняния, однако механизм этого явления совершенно другой. Чаще всего при ОРВИ мы не чувствуем запахов из-за отека и воспаления слизистой носа.
Каким же образом злосчастный вирус SARS-CoV2 лишает нас обоняния? На каком этапе проведения информации о тех или иных пахучих веществ от обонятельного эпителия к высшим центрам обработки сигналов он действует? Несмотря на большое число исследований, эти вопросы до сих пор остаются не до конца выясненными.
Важнейшим механизмом обонятельной дисфункции считают вирусное повреждение клеток обонятельного эпителия [8]. Вирус проникает в клетку, связываясь с определенными рецепторами на поверхности клеток. ACE2 (ангиотензинпревращающий фермент-2) служит рецептором, который связывается с вирусным S-белком (Spike) и облегчает проникновение вируса в клетку [8]. При их взаимодействии белок S расщепляется под действием поверхностной протеазы TMPRSS2 (трансмембранная сериновая протеаза-2), но здесь могут быть задействованы и другие ферменты (такие как фурин, катепсин B и L, CTSB/CTSL) [8].
Интересно, что в обонятельном эпителии рецепторы ACE2 и TMPRSS2 экспонируются на поверхности не всех клеток, а только стентакулярных и горизонтальных базальных клеток, а также клеток Боуменовых желез [8]. Однако многие вирусы, в том числе и коронавирусы (включая SARS-CoV-2), попадают из носового эпителия в обонятельную луковицу и далее в другие отделы мозга и могут повреждать нервную ткань [9]. Рецепторы ACE2 и TMPRSS2 также обнаружены на поверхности обонятельной луковицы на перицитах сосудов (это клетки соединительной ткани, которые обслуживают кровеносные капилляры мозга) [8].
Повреждение обонятельного эпителия — это, вероятно, основной механизм обонятельной слепоты, возникающий при нарушениях нормальной структуры и функции эпителия, а косвенное воздействие вируса на обонятельную луковицу происходит при повреждения поддерживающих клеток. Однако не так давно был обнаружен еще один путь проникновения вируса в клетки через рецептор нейропилин-1 (NRP1), который синтезируется обонятельными сенсорными нейронами и их клетками-предшественниками [10]. Нейропилины (трансмембранные рецепторы) участвуют во многих физиологических процессах, включая развитие нейронов, ангиогенез и регуляцию иммунных реакций. Этот путь проникновения вируса может напрямую повреждать нейроны и вызывать перенос вирусных частиц к обонятельной луковице по аксонам, объясняя, почему у некоторых пациентов с COVID-19 обонятельная функция долго не восстанавливается [10].
Таким образом, есть несколько возможных и не исключающих друг друга механизмов потери обоняния у пациентов с COVID-19 [8–10]:
Особенности зáпаховой слепоты при COVID-19 и прогнозы выздоровления
Запаховая слепота при COVID-19 имеет ряд особенностей [6], [11]. Например, на частоту ее возникновения влияет гендер: женщины страдают аносмией/гипосмией чаще мужчин [6]. Помимо этого, обонятельная дисфункция встречается у пациентов с легкой или умеренной формами болезни. В 11,8% случаев аносмия возникает до, в 65,4% случаев — после, в 22,8% случаев — одновременно с общими или ЛОР-симптомами коронавирусной инфекции [6]. В 18,2 % случаев аносмия наблюдается без назальных симптомов (нарушения носового дыхания, повышения назальной секреции). Большинство пациентов с нарушениями обоняния (79,6%) страдают аносмией, остальные 20,4% — гипосмией. Часть заболевших жаловалась на внезапное появление нетипичных запахов серы, нашатыря, уксуса, гари и т.д. Такие симптомы относят к фантосмии (то есть ощущению фантомных запахов, или обонятельным галлюцинациям) и паросмии (искаженному ощущению запаха) [11]. К сожалению, обонятельные иллюзии говорят о повреждении центральных структур анализа запахов.
Многих волнует вопрос, как долго длится это состояние запаховой слепоты. К счастью, у большинства пациентов с COVID-19 работа обоняния восстанавливается спустя примерно 2–4 недели после нарушения [11] или, по другим данным, в течение 8 дней после выздоровления (то есть при отсутствии общих и ЛОР-симптомов) [6]. Для лечения обонятельной слепоты нос орошают физиологическим раствором и растворами кортикостероидов, принимают витамины и микроэлементы [6].
Быстрое избавление от аносмии указывает на то, что целью SARS-CoV-2 являются не сами обонятельные сенсорные нейроны, а стентакулярные клетки. Но все же остается небольшой процент пациентов, у которых нарушение обоняния длится месяцы. Пока нет однозначного ответа, почему у одних людей восстановление обоняния занимает несколько дней, а у других растягивается на месяцы, а возможно и годы. Также неясно, будут ли сохраняться нарушения обоняния у пациентов в течение жизни, и если да, то, как долго. Вероятно, при повреждении вирусом значительной части базальных клеток и/или обонятельных сенсорных нейронов, времени на восстановление обонятельного эпителия может понадобиться гораздо больше.
Заключение
Зачастую мы не придаем особого значения способности обонять — ровно до тех пор, пока не лишаемся ее. Кажется невозможным, если мир вдруг перестанет пахнуть, а еда станет безвкусной. Новый вирус показал нам, каково это — вдруг потерять такую важную связь с окружающим миром. К счастью, шансы на выздоровление высоки. Не теряйте нюх к жизни!
.gif)
.gif)
.gif)