Свойства лития как металла
ЛИТИЙ — в космосе, на земле, под водой
«По значимости в современной технике литий является одним из важнейших редких элементов».
Краткая химическая энциклопедия.
Из четырех процентов
История открытия лития началась с …математики. Химик Арфведсон анализировал минерал с рудника Уто. Ученый определил, что это обычный алюмосиликат, и содержание в нем алюминия, кремния и кислорода составляет 96%. Настырный химик задумался — что с оставшимися 4%. Отделив основные составляющие и растворив остаток, он получил раствор со щелочными свойствами. Логично было предположить, что открыт новый элемент.
Описанием минерала, из которого извлекли новый элемент, служат слова: «обычный булыжник». Потому и назвали новый металл литием (litos по латыни камень).
Свойства лития

Характеристики:
Химические свойства:
Месторождения
В природе литий содержится в солевых растворах (подземных водах). Твердые источники часто расположены в пегматитовых рудах. Минералы: сподумен, лепидолит, эльбаит, ядарит.
В России 16 месторождений, но добыча не производится.
Добыча
В добыче литиевого рассола есть пара проблем — география и надежность.
Рассол выкачивают в «бассейны» — специальные пруды, где естественным выпариванием концентрируется содержание элемента. Нужна постоянно высокая температура (география) и время — процесс занимает до года. Дальше концентрированная рапа (1-2% Li) отправляют на обработку на химзавод.
Твердые источники разрабатываются традиционными методами бурения и переработки.
В мире четыре производителя контролируют 85% добычи (основные — Аргентина и Чили).
Производство
Способы получения лития зависит от исходного материала.
Солевые растворы (рапа) выпаривают, затем осаждают литиевое соединение.
Твердые минералы вначале обогащают (с помощью магнитной сепарации, гравитационных методов, а при добыче крупных кристаллов сподумена просто вручную). Производство происходит в основном гидрометаллургическим способом.
Применение
Литий и его соединения используют:
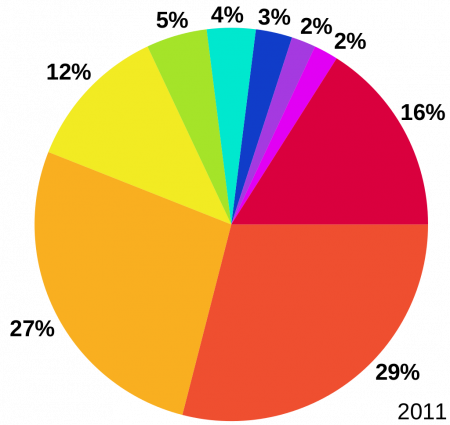
Мировое применение легкого металла распределяется так:
Плюсы и минусы литиевых батарей 🔋
Эти аккумуляторы и батареи просты в эксплуатации, они постоянно готовы к эксплуатации.
Стоимость
Цена лития марки ЛЭ-1 (99,9%) за килограмм 15 000 рублей.
Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Свойства и характеристики металла литий
Металл литий обладает уникальными химическими и физическими свойствами. Он отличается от остальных щелочных металлов, что расширяет его возможности применения в разных сферах деятельности. Он очень важен для правильной работы организма.

Краткое описание
Литий — щелочной металл, который имеет выраженные пластичные свойства, серебристый цвет, характерный металлический блеск. Его легко обрабатывать, он имеет низкую температуру плавления — 180°C. Если сравнивать его с другими щелочными металлами, он обладает самой низкой плотностью. Поскольку она ниже чем у воды, материал всплывает на поверхность.
Структура и характеристики
Структура кристаллической решетки металлического лития — кубическая, объемноцентрированная. Ее параметры — 3,490 Å. Данные характеристики соблюдаются только при комнатной температуре.
Атом лития имеет две оболочки — внешнюю и внутреннюю. На внешней расположены электроны. Они участвуют в образовании химических связей.
История открытия и изучения
Первый образец металлического лития был получен благодаря работе Гемфри Дэви. С помощью электрического тока он разложил расплав гидроксида этого щелочного металла. Через некоторое время Леопольд Гмелин проэкспериментировал с литиевосодержащими солями. Он смог выявить, что они окрашивают пламя в темный цвет.
Основная заслуга в открытии нового химического элемента и росте его популярности принадлежит Иоганну Августу. В 1817 году он нашел новое вещество в составе петалита, алюмосиликата. Через некоторое время литий нашли и в других минеральных образованиях. Такое название он получил из-за того, что впервые был найден в камнях. Название камня по гречески — «литос».
Петалит (Фото: Instagram / lopatkin_oleg)
Месторождения и добыча
Литий содержится в разных минералах. Самые богатые по содержанию этого щелочного металла камни — слюда лепидолит, пироксен сподумен. Литий можно найти в разных породообразующих минералах. В них он замещает кальций.
Основные месторождения этого металла находятся в Боливии, Чили, Аргентине, США, Китае, Конго, Сербии, Бразилии, Австралии, России.
Промышленное получение
Для получения лития промышленными способами сначала происходит подготовка расходного сырья — минералов или солевых растворов, которые добываются из соляных озер. Независимо от способа добычи расходного сырья, на выходе получается Li2CO3, который будет проходить промышленную обработку.
Способы получения расходного сырья:
Выбор промышленного способа получения щелочного металла зависит от наличия оборудования, требуемого результата, вида расходного сырья.
Свойства
Свойства элемента известны ученым давно. По сравнению с другими щелочными металлами он имеют ряд уникальных особенностей, по которым определяются основные сферы применения этого вещества.
Химические
Литий проявляет стабильность находясь на воздухе. Из группы щелочных металлов он наименее активный. Про взаимодействии с сухим воздухом и кислородом практические не реагирует (при условии соблюдения комнатной температуры).
Взаимодействие лития с водой проходит относительно спокойно. При контакте с водой он начинает образовывать щелочь, выделять кислород. Металл плавает на поверхности жидкости, быстро растворяясь и издавая характерное шипение.
При влажном воздухе металл вступает в реакции с газами, которые содержатся в нем (особенно с азотом). Оксидная пленка покрывает поверхности лития при нагревании до 100–300°C. Пленка защищает металл от окислительных процессов.
При реакции с серой образуется сульфид (при условии нагревания до 130°C). С кремнием вступает в реакцию при нагревании до 700°C. Растворяется в жидком аммиаке, образуя раствор синего цвета.
Литий нельзя хранить в керосиновой жидкости. Из-за малой плотности материал всплывет на поверхность. Для хранения подойдет минеральное масло, газолин, парафин. Емкость лучше выбирать из жести. Она должна герметично закрываться.
Физические
Показатель относительного удлинения — 70%.
Литий — мягкий, пластичный металл. Проще всего обрабатывается с помощью прокатки, прессования.
Сферы применения
Используется при изготовлении:
Основные сферы применения:
Перхлорат щелочного металла используется в качестве окислителя.
Соединения с литием
Соединения на основе щелочного металла
Литий — щелочной металл с уникальными свойствами. Он применяется в разных сферах деятельности. Добывается из разных минералов и проходит дополнительную обработку.
Литий
(молярная масса)
(первый электрон)
Литий (Li, лат. lithium ) — химический элемент первой группы, второго периода периодической системы с атомным номером 3. Как простое вещество представляет собой мягкий щелочной металл серебристо-белого цвета.
Содержание
История и происхождение названия
Литий был открыт в 1817 году шведским химиком и минералогом Иоганном Арфведсоном сначала в минерале петалите (Li,Na)[Si4AlO10], а затем в сподумене LiAl[Si2O6] и в лепидолите K2Li3Al5[Si6O20](F,OH)4. Металлический литий впервые получил Гемфри Дэви в 1818 году.
Своё название литий получил из-за того, что был обнаружен в «камнях» (греч. λίθος — камень). Первоначально назывался «литион», современное название было предложено Берцелиусом.
Физические свойства
Литий — серебристо-белый металл, мягкий и пластичный, твёрже натрия, но мягче свинца. Его можно обрабатывать прессованием и прокаткой.
При комнатной температуре металлический литий имеет кубическую объёмноцентрированную решётку (координационное число 8), пространственная группа I m3m, параметры ячейки a = 0,35021 нм, Z = 2. Ниже 78 К устойчивой кристаллической формой является гексагональная плотноупакованная структура, в которой каждый атом лития имеет 12 ближайших соседей, расположенных в вершинах кубооктаэдра. Кристаллическая решётка относится к пространственной группе P 63/mmc, параметры a = 0,3111 нм, c = 0,5093 нм, Z = 2.
Из всех щелочных металлов литий характеризуется самыми высокими температурами плавления и кипения (180,54 и 1340 °C, соответственно), у него самая низкая плотность при комнатной температуре среди всех металлов (0,533 г/см³, почти в два раза меньше плотности воды). Вследствие своей низкой плотности литий всплывает не только в воде, но и, например, в керосине.
Маленькие размеры атома лития приводят к появлению особых свойств металла. Например, он смешивается с натрием только при температуре ниже 380 °C и не смешивается с расплавленными калием, рубидием и цезием, в то время как другие па́ры щелочных металлов смешиваются друг с другом в любых соотношениях.
Химические свойства
Литий является щелочным металлом, однако относительно устойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. По этой причине литий является единственным щелочным металлом, который не хранят в керосине (к тому же плотность лития столь мала, что он будет в нём плавать); он может непродолжительное время храниться на воздухе.
Во влажном воздухе медленно реагирует с азотом и другими газами, находящимися в воздухе, превращаясь в нитрид Li3N, гидроксид LiOH и карбонат Li2CO3.
Поэтому длительно литий хранят в петролейном эфире, парафине, газолине и/или минеральном масле в герметически закрытых жестяных коробках.
В кислороде при нагревании горит, превращаясь в оксид Li2O.
Интересная особенность лития в том, что в интервале температур от 100 °C до 300 °C он покрывается плотной оксидной плёнкой и в дальнейшем не окисляется. В отличие от остальных щелочных металлов, дающих стабильные надпероксиды и озониды; надпероксид и озонид лития — нестабильные соединения.
В 1818 немецкий химик Леопольд Гмелин установил, что литий и его соли окрашивают пламя в карминово-красный цвет, это является качественным признаком для определения лития. Температура самовоспламенения находится в районе 300 °C. Продукты горения раздражают слизистую оболочку носоглотки.
Спокойно, без взрыва и возгорания, реагирует с водой, образуя LiOH и H2.
Реагирует также с этиловым спиртом (с образованием этанолята):
Вступает в реакцию с водородом (при 500—700 °C) с образованием гидрида лития:
Реагирует с аммиаком при нагревании, при этом сначала образует амид лития (220 °C), а затем имид лития (400 °C):
Реагируя с галогенами (с йодом — только при нагревании, выше 200 °C) образует соответствующие галогениды:
При 130 °C реагирует с серой с образованием сульфида:
В вакууме при температуре выше 200 °C реагирует с углеродом (образуется ацетиленид):
При 600—700 °C литий реагирует с кремнием с образованием силицида:
Химически растворим в жидком аммиаке (−40 °C), образуется синий раствор.
В водном растворе ион лития имеет самый низкий стандартный электродный потенциал (−3,045 В) из-за малого размера и высокой степени гидратации иона лития.
Металлический литий вызывает ожоги при попадании на влажную кожу, слизистые оболочки и в глаза.
Нахождение в природе
Геохимия лития
Основные минералы лития — слюда лепидолит — KLi1,5Al1,5[Si3AlO10](F, OH)2 и пироксен сподумен — LiAl[Si2O6]. Когда литий не образует самостоятельных минералов, он изоморфно замещает калий в широко распространённых породообразующих минералах.
Месторождения лития приурочены к редкометалльным гранитным интрузиям, в связи с которыми развиваются литиеносные пегматиты или гидротермальные комплексные месторождения, содержащие также олово, вольфрам, висмут и другие металлы. Стоит особо отметить специфические породы онгониты — граниты с магматическим топазом, высоким содержанием фтора и воды и исключительно высокими концентрациями различных редких элементов, в том числе и лития.
Другой тип месторождений лития — рассолы некоторых сильносолёных озёр.
Месторождения
Месторождения лития известны в Чили, Боливии (Солончак Уюни — крупнейшее в мире), США, Аргентине, Конго, Китае (озеро Чабьер-Цака), Бразилии, Сербии, Австралии.
В России более 50 % запасов сосредоточено в редкометалльных месторождениях Мурманской области.
Изотопы лития
Природный литий состоит из двух стабильных изотопов: 6 Li (7,5 %) и 7 Li (92,5 %); в некоторых образцах лития изотопное соотношение может быть сильно нарушено вследствие природного или искусственного фракционирования изотопов. Это следует иметь в виду при точных химических опытах с использованием лития или его соединений. У лития известны 7 искусственных радиоактивных изотопов ( 4 Li − 12 Li) и два ядерных изомера ( 10m1 Li и 10m2 Li). Наиболее устойчивый из них, 8 Li, имеет период полураспада 0,8403 с. Экзотический изотоп 3 Li (трипротон), по-видимому, не существует как связанная система.
7 Li является одним из немногих изотопов, возникших при первичном нуклеосинтезе (то есть в период от 1 секунды до 3 минут после Большого Взрыва) в количестве не более 10 −9 от всех элементов. Некоторое количество изотопа 6 Li, как минимум в десять тысяч раз меньшее, чем 7 Li, также образовано в первичном нуклеосинтезе.
Примерно в десять раз больше 7 Li образовались в звёздном нуклеосинтезе. Литий является промежуточным продуктом реакции ppII, но при высоких температурах активно преобразуется в два ядра гелия-4 (через 8 Be).
В космосе
Аномально высокое содержание лития наблюдается в звёздных образованиях, состоящих из красного гиганта (или сверхгиганта), внутри которого находится нейтронная звезда — объектах Ландау — Торна — Житкова.
Также имеется большое количество звёзд-гигантов с необычно высоким содержанием лития, что объясняется попаданием лития в атмосферу звёзд при поглощении ими экзопланет-гигантов.
Получение
Исходным сырьём для лития служат два источника: минеральное сырьё (например, сподумен) и солевые растворы из соляных озёр, богатые солями лития. В обоих случаях результатом работы является карбонат лития Li2CO3.
Сподумен (силикат лития и алюминия) можно перерабатывать несколькими способами. Например, спеканием с сульфатом калия получают растворимый сульфат лития, который осаждают из раствора содой:
Солевые растворы предварительно выпаривают. В солевых растворах содержится хлорид лития LiCl. Однако вместе с ним содержатся большие количества других хлоридов. Для увеличения концентрации лития из выпаренного раствора осаждают карбонат лития Li2CO3, например по схеме
Металлический литий чаще всего получают электролизом расплава солей или восстановлением из оксида.
При электролизе используется хлорид лития. Его получают из карбоната по схеме:
Поскольку температура плавления хлорида лития близка к температуре кипения лития, применяют эвтектическую смесь с хлоридом калия или бария, что понижает температуру расплава и позволяет избавиться от необходимости улавливать пары металла. Расход электроэнергии до 14 кВт∙ч на 1 кг лития. На другом электроде получают газообразный хлор.
2Li2O + Si ⟶ 4Li↑ + SiO2 Рафинирование
Полученный литий очищают методом вакуумной дистилляции, последовательно выпаривая разные металлы из сплава при определённых температурах.
Добыча
В 2015 году в мире добыли 32,5 тыс. тонн лития и его соединений в пересчёте на металл. Крупнейшие страны по добыче — Австралия, Чили и Аргентина. В России собственная добыча лития была полностью утрачена после распада СССР, но в 2017 году Россия запустила экспериментальную установку, позволяющую добывать литий из бедных руд с небольшими затратами.
Большая часть добывается из естественных водных линз в толще соляных озёр, в насыщенных соляных растворах которых концентрируется хлорид лития. Раствор выкачивается и выпаривается на солнце, полученная смесь солей перерабатывается. Содержание лития в растворе колеблется от 0,01 % до 1 %. Также значительная доля добычи приходится на минеральное сырьё, например, минерал сподумен.
Применение
Термоэлектрические материалы
Сплав сульфида лития и сульфида меди — эффективный полупроводник для термоэлектропреобразователей (ЭДС около 530 мкВ/К ).
Химические источники тока
Из лития изготовляют аноды химических источников тока (аккумуляторов, например, литий-хлорных аккумуляторов) и гальванических элементов с твёрдым электролитом (например, литий-хромсеребряный, литий-висмутатный, литий-окисномедный, литий-двуокисномарганцевый, литий-иодсвинцовый, литий-иодный, литий-тионилхлоридный, литий-оксидванадиевый, литий-фторомедный, литий-двуокисносерный элементы), работающих на основе неводных жидких и твёрдых электролитов (тетрагидрофуран, пропиленкарбонат, метилформиат, ацетонитрил).
Кобальтат лития и молибдат лития показали лучшие эксплуатационные свойства и энергоёмкость в качестве положительного электрода литиевых аккумуляторов.
Гидроксид лития используется как один из компонентов для приготовления электролита щелочных аккумуляторов. Добавление гидроксида лития к электролиту тяговых железо-никелевых, никель-кадмиевых, никель-цинковых аккумуляторных батарей повышает их срок службы в 3 раза и ёмкость на 21 % (за счёт образования никелатов лития).
Алюминат лития — наиболее эффективный твёрдый электролит (наряду с цезий-бета-глинозёмом).
Лазерные материалы
Монокристаллы фторида лития используются для изготовления высокоэффективных (КПД 80 %) лазеров на центрах свободной окраски и для изготовления оптики с широкой спектральной полосой пропускания.
Окислители
Перхлорат лития используют в качестве окислителя.
Дефектоскопия
Сульфат лития используют в дефектоскопии.
Пиротехника
Нитрат лития используют в пиротехнике для окрашивания огней в красный цвет.
Сплавы
Сплавы лития с серебром и золотом, а также медью являются очень эффективными припоями. Сплавы лития с магнием, скандием, медью, кадмием и алюминием — новые перспективные материалы в авиации и космонавтике (из-за их лёгкости). На основе алюмината и силиката лития создана керамика, затвердевающая при комнатной температуре и используемая в военной технике, металлургии, и, в перспективе, в термоядерной энергетике. Огромной прочностью обладает стекло на основе литий-алюминий-силиката, упрочняемого волокнами карбида кремния. Литий очень эффективно упрочняет сплавы свинца и придаёт им пластичность и стойкость против коррозии.
Электроника
Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития LiNbO3 и танталат лития LiTaO3 являются нелинейными оптическими материалами и широко применяются в нелинейной оптике, акустооптике и оптоэлектронике.
Литий также используется при наполнении осветительных газоразрядных металлогалогеновых ламп.
Гидроксид лития добавляют в электролит щелочных аккумуляторов для увеличения срока их службы.
Металлургия
В чёрной и цветной металлургии литий используется для раскисления и повышения пластичности и прочности сплавов. Литий иногда применяется для восстановления методами металлотермии редких металлов.
Металлургия алюминия
Карбонат лития является важнейшим вспомогательным веществом (добавляется в электролит) при выплавке алюминия, и его потребление растёт с каждым годом пропорционально объёму мировой добычи алюминия (расход карбоната лития 2,5—3,5 кг на тонну выплавляемого алюминия).
Введение лития в систему легирования позволяет получить новые сплавы алюминия с высокой удельной прочностью.
Добавка лития снижает плотность сплава и повышает модуль упругости. При содержании лития до 1,8 % сплав имеет низкое сопротивление коррозии под напряжением, а при 1,9 % сплав не склонен к коррозионному растрескиванию. Увеличение содержания лития до 2,3 % способствует возрастанию вероятности образования рыхлот и трещин. Механические свойства при этом изменяются: пределы прочности и текучести возрастают, а пластические свойства снижаются.
Наиболее известны системы легирования Al-Mg-Li (пример — сплав 1420, применяемый для изготовления конструкций летательных аппаратов) и Al-Cu-Li (пример — сплав 1460, применяемый для изготовления ёмкостей для сжиженных газов).
Ядерная энергетика
Изотопы 6 Li и 7 Li обладают разными ядерными свойствами (сечение поглощения тепловых нейтронов, продукты реакций) и сфера их применения различна. Гафниат лития входит в состав специальной эмали, предназначенной для захоронения высокоактивных ядерных отходов, содержащих плутоний.
Литий-6
Применяется в термоядерной энергетике.
При облучении нуклида 6 Li тепловыми нейтронами получается радиоактивный тритий 3 H:
Благодаря этому литий-6 может применяться как замена радиоактивного, нестабильного и неудобного в обращении трития как в военных (термоядерное оружие), так и в мирных (управляемый термоядерный синтез) целях. В термоядерном оружии обычно применяется дейтерид лития-6 6 LiD.
Перспективно также использование лития-6 для получения гелия-3 (через тритий) с целью дальнейшего использования в дейтерий-гелиевых термоядерных реакторах.
Литий-7
Применяется в ядерных реакторах. Благодаря очень высокой удельной теплоёмкости и низкому сечению захвата тепловых нейтронов жидкий литий-7 (часто в виде сплава с натрием или цезием) служит эффективным теплоносителем. Фторид лития-7 в сплаве с фторидом бериллия (66 % LiF + 34 % BeF2) носит название «флайб» (FLiBe) и применяется как высокоэффективный теплоноситель и растворитель фторидов урана и тория в высокотемпературных жидкосолевых реакторах, и для производства трития.
Сушка газов
Высокогигроскопичные бромид LiBr и хлорид лития LiCl применяются для осушения воздуха и других газов.
Медицина
Соли лития обладают нормотимическими и другими лечебными свойствами. Поэтому они находят применение в медицине.
Смазочные материалы
Стеарат лития («литиевое мыло») используется в качестве загустителя для получения пастообразных высокотемпературных смазок машин и механизмов. См. напр.: Литол, ЦИАТИМ-201.
Регенерация кислорода в автономных аппаратах
Гидроксид лития LiOH, пероксид Li2O2 применяются для очистки воздуха от углекислого газа; при этом последнее соединение реагирует с выделением кислорода (например, 2Li2O2 + 2CO2 → 2Li2CO3 + O2), благодаря чему используется в изолирующих противогазах, в патронах для очистки воздуха на подлодках, на пилотируемых космических аппаратах и т. д.
Силикатная промышленность
Литий и его соединения широко применяют в силикатной промышленности для изготовления специальных сортов стекла и покрытия фарфоровых изделий.
Прочие области применения
Соединения лития используются в текстильной промышленности (отбеливание тканей), пищевой (консервирование) и фармацевтической (изготовление косметики).
Весьма перспективно использовать литий в качестве наполнителя поплавка батискафов — этот металл имеет плотность, почти в два раза меньшую, чем вода (точнее, 534 кг/м³), это значит, что один кубический метр лития может удерживать на плаву почти на 170 кг больше, чем один кубический метр бензина. Однако литий — щелочной металл, активно реагирующий с водой, следует каким-то образом надёжно разделить эти вещества, не допустить их контакта.
Из лития изготавливают аноды химических источников тока (например, литий-хлорных аккумуляторов) и гальванических элементов с твёрдым электролитом (например, литий-хромсеребряный, литий-висмутатный, литий-окисномедный, литий-двуокисномарганцевый, литий-иодсвинцовый, литий-иодный, литий-тионилхлоридный, литий-оксидванадиевый, литий-фторомедный, Литий-двуокисносерный элементы), работающих на основе неводных жидких и твёрдых электролитов (тетрагидрофуран, пропиленкарбонат, метилформиат, ацетонитрил). Кобальтат лития и молибдат лития показали лучшие эксплуатационные свойства и энергоёмкость в качестве положительного электрода литиевых аккумуляторов. Гидроксид лития используется как один из компонентов для приготовления электролита щелочных аккумуляторов. Добавление гидроксида лития к электролиту тяговых железо-никелевых, никель-кадмиевых, никель-цинковых аккумуляторных батарей повышает их срок службы в 3 раза и ёмкость на 21 % (за счёт образования никелатов лития). Алюминат лития — наиболее эффективный твёрдый электролит (наряду с цезий-бета-глинозёмом). Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития LiNbO3 и танталат лития LiTaO3 являются нелинейными оптическими материалами и широко применяются в нелинейной оптике, акустооптике и оптоэлектронике. Литий также используется при наполнении осветительных газоразрядных металлогалогеновых ламп. Гидроксид лития добавляют в электролит щелочных аккумуляторов для увеличения срока их службы.
Биологическое значение лития
Литий в небольших количествах необходим организму человека (порядка 100 мкг/день для взрослых). Преимущественно в организме находится в щитовидной железе, лимфоузлах, сердце, печени, лёгких, кишечнике, плазме крови, надпочечниках.
Литий принимает участие в важных процессах:
Препараты лития широко используются в терапии психических расстройств.
Выделяется литий преимущественно почками.
По состоянию на конец 2007 — начало 2008 года, цены на металлический литий (чистота 99 %) составляли 63—66 долларов за 1 кг.