Торакокардиальный индекс как считать
Что такое кардиоторакальный индекс, его нормальное значение
Что это такое простыми словами, как высчитывается, нормы, границы
Человеческий организм – чётко работающий механизм, отлаженный самой природой. Все органы и ткани в теле развиваются вместе из одного зародыша, поэтому размеры и параметры каждой части тела подходят под размеры соседних органов, как детали в мозаике.
Но что же происходит, когда какой-то орган меняет свои размеры по той или иной причине? Такой орган может начать давить на окружающие ткани, мешая их функционированию, или наоборот, образующаяся пустота на месте уменьшенного органа может лишить окружающие структуры поддержки. Изменение размеров органа может быть важным симптомом или причиной различных заболеваний.
Именно поэтому измерение размеров различных частей человеческого тела является важным инструментом диагностики. Одним из таких инструментов является кардиоторакальный индекс.
Рентгенография
Основой для вычисления кардиоторакального индекса является прямая рентгенография грудной клетки. Рентгенография – это исследование внутреннего устройства объектов без их вскрытия, при помощи пропускания сквозь объект рентгеновских лучей.
Различные материалы поглощают эти лучи с различной интенсивностью, поэтому полученная запись оставшегося излучения может примерно передать расположение этих материалов внутри объекта. Отсюда и взялось слово «рентгенография» – это сочетание фамилии учёного Рентген и латинской частицы «-графия» – «запись».
Немецкий физик Вильгельм Конрад Рентген первым обнаружил не только эффект засвечивания фотоплёнки рентгеновскими лучами, но и первым же догадался сунуть под эти лучи свою руку. Типичный учёный. Обнаруженный после этого на фоточувствительной пластине снимок костей в просвеченной руке перевернул не только мир медицины, но и представления о мировом устройстве в целом.
Рентгенография, благодаря своей неинвазивности, открыла множество перспектив диагностики для врачей. При помощи такого лучевого обследования можно получать информацию не только о размере органов, но и об их тонусе, общем состоянии, правильности движений.
Чаще всего рентгенография используется как метод диагностики при переломах костей и прочих подобных травмах, из-за простоты и однозначности диагностики – кости особенно хорошо поглощают рентгеновское излучение, формируя на снимке чёткий и ясный след.
Но в целом подобный метод исследования хорошо подходит и для обследования любых полостей – полых органов, таких, как лёгкие или кишечник, или же полостей не природного происхождения – например, кариес в зубах.
К сожалению, в наше время рентгенография является устаревшим и неточным методом исследования тканей и органов пациента. Двухмерная проекция снимка не даёт полной информации, в отличие от послойного сканирования тела томографии, а иногда рентгеновский снимок и вовсе не даёт никакой полезной информации.
Если ткани органа похожи по плотности и составу друг на друга, то такой снимок будет сплошной кашей.
Рентгенокардиометрия
Естественно подходящей зоной для рентгенографии является самая большая полость в нашем теле – грудная клетка. Помимо исследования лёгких, которое проходит регулярно практически каждый человек для профилактики туберкулёза, важнейшей целью диагностики в грудной клетке является сердце.
Сердечно-сосудистые заболевания – безусловный чемпион по смертности населения. Сердце, работающее на протяжении всей жизни человека, требует пристального внимания, и изменение его размеров может служить симптомом различных заболеваний или патологических изменений. Для исследования этих размеров и используют кардиоторакальный индекс.
Кардиоторакальный индекс
«Кардио» это сердце, «торакс» это грудь. Получаем, что кардиоторакальный индекс – это соотношение размеров сердца к груди.
Для вычисления этого индекса измеряется размер тени сердца, видимой на рентгенографическом снимке. Для этого измерения берутся две самые удалённые от центра точки слева и справа на контуре пятна, оставленного сердцем на снимке. Расстояние между этими точками и считается размером сердца при данном исследовании.
Полученный размер сравнивается с размером грудной клетки. Для грудной клетки точно так же берутся две самые удалённые точки, но находящиеся на внутренней стороне рёбер прямо над куполом диафрагмы. Длинная прямая линия между этими точками и будет размером грудной клетки.
Кардиоторакальный индекс – это процентное отношение размера сердца по отношению к размеру грудной клетки. Это отношение выражают или прямо в процентах, например, КТИ=50%, или в десятых долях единицы, например, КТИ=0,5.
В норме КТИ у взрослого человека будет около 0,5, у новорождённых до 0,6. Увеличение же размеров сердца свыше 0,6 может говорить о патологиях: увеличении жировой клетчатки или о кардиомегалии – синдроме увеличенного сердца.
Торакокардиальный индекс как считать
Актуальность патологии органов кровообращения подтверждается статистическими данными заболеваемости, согласно которым общая заболеваемость системы кровообращения выросла за период 2016–2017 гг. на 2,3 % [1].
Сердечно-сосудистая система – это одна из важнейших систем жизнеобеспечения, осуществляющая доставку всего необходимого клеткам организма. Сердце, по существу, выполняет насосную функцию по перекачке крови. Насосная функция сердца может быть проанализирована с позиций механической систолы (эхокардиография – ФВ левого желудочка) и с позиций электрической систолы (ЭКГ – индекс ФП). При этом следует учитывать, что ФВ левого желудочка зависит не только от состояния систолической функции левого желудочка, но и от состояния клапанного аппарата сердца. Электрическая же систола желудочков (Q-T) отображает в конечном счете сократительную способность кардиомиоцитов миокарда в целом, нарушение которой является источником формирования сердечной недостаточности. Оценка систолической функции миокарда желудочков сердца с помощью электрокардиографии при использовании систолического показателя (СП), длительности интервала Q-T, объединении нескольких методов проводилась и ранее [5–7]. Однако эти способы (одни без должного обоснования со стороны биофизики, электрофизиологии и гидродинамики, другие из-за высокой трудоемкости, ограниченной доступности) не получили широкого применения в медицинской практике.
В современной медицине оценка систолической функции миокарда левого желудочка традиционно проводится в основном с помощью эхокардиографии, при этом применяется показатель механической систолы желудочков – фракция выброса (ФВ) левого желудочка [8, 9]. Однако эхокардиография имеет свои ограничения в виде отсутствия широкой доступности для всего населения, зависимости от профессионализма специалиста, расположения электродов, что влияет на точность измерения. Также существует сложность измерения ФВ в условиях тахикардии, что затрудняет точную оценку динамики систолической функции миокарда левого желудочка. Поэтому актуальными являются поиск и обоснование оценки систолической функции миокарда левого желудочка с помощью показателей электрической систолы, регистрируемой на ЭКГ, которая лишена приведенных выше недостатков эхокардиографии.
Учитывая, что в 40–49 % случаев у лиц с клиническими проявлениями сердечной недостаточности регистрируются нормальные показатели ФВ [10, 11], необходим дополнительный показатель, который позволял бы не только регистрировать состоявшуюся сердечную недостаточность, но и оперативно отслеживать динамику этой функции миокарда в процессе течения и лечения болезни. Целью настоящего исследования являлась необходимость обоснования дополнительного критерия в изучении систолической функции миокарда левого желудочка с помощью электрокардиографии, имеющей широкую доступность и простоту использования, высокую достоверность результатов и лишенной субъективного влияния на измерение при любой ЧСС.
Материалы и методы исследования
В исследование были включены результаты обследования людей различного возраста (от 4 до 78 лет), которым были выполнены эхокардиография и электрокардиография. Для исследования были отобраны 140 человек, которые были разделены на две группы, состоящие из лиц с нормальными показателями ФВ (УЗИ) и электрической систолы желудочков Q-T (ЭКГ) в количестве 100 человек и лиц с нарушением ФВ и Q-T в количестве 40 человек.
В процессе исследования, используя УЗИ сердца и ЭКГ, определяли фазу выброса левого желудочка (ФВ по Симпсону), фазу изгнания (ФИ) в ЭКГ, фазу плато (ФП) в потенциале действия (ПД) с проекцией на ЭКГ и проводили их анализ на совпадение получаемых результатов в оценке систолической функции желудочков сердца.
Результаты исследования и их обсуждение
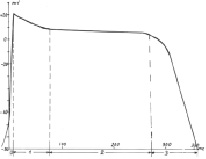
Деятельность сердца осуществляется с использованием электрических механизмов формирования сердечных сокращений. Для одиночного кардиомиоцита его активность представлена в виде потенциала действия, отображенного на рис. 1.
Рис. 1. ПД одиночного кардиомиоцита
0 – Фаза деполяризации потенциала действия одиночного кардиомиоцита – (ПД). Фаза деполяризации мембраны одиночного кардиомиоцита длится от 1–2 до 5 мс.
1 – Фаза начальной быстрой реполяризации ПД. Длительность фазы начальной быстрой реполяризации в ПД обусловлена длительностью деполяризации всех кардиомиоцитов, отображаемых на ЭКГ комплексом QRS, и занимает всю фазу 1 ПД. Деполяризация начинается с верхушки и распространяется к основанию сердца, формируя комплекс QRS, который в свою очередь отображает фазу напряжения миокарда в цикле гемодинамики сердечного сокращения.
2 – Деполяризация всего миокарда желудочков сердца в виде комплекса QRS занимает в среднем от 50 до 100 мс, в цикле гемодинамики этот период называется фазой напряжения.
3 – Фаза медленной реполяризации, или фаза плато (ФП) ПД. Длительность ФП составляет в среднем для спокойного ритма около 250 мс. В этот период осуществляется изгнание крови из желудочков сердца в аорту, при этом выполняется насосная функция сердца. Фаза изгнания состоит из двух частей: фазы быстрого изгнания, совпадающей с фазой плато (до 120 мс), которая на ЭКГ отображается сегментом ST, и фазы медленного изгнания (до 130 мс), отображаемой на ЭКГ зубцом T, где вторая его половина совпадает с фазой конечной быстрой реполяризации ПД. В норме зубец Т обычно симметричный. Сократительную способность миокарда обеспечивают ионы Ca, максимально поступающие из внеклеточного пространства и из внутриклеточных структур, содержащих депо Ca, преимущественно в фазу плато. Конец фазы плато приходится на середину зубца Т. Поскольку сокращение миокарда возможно только при посредничестве Ca и его основной метаболизм совершается в фазе плато ПД, имеется возможность оценки сократительной функции миокарда через определение процентной доли фазы плато в фазе изгнания в целом.
4 – Фаза быстрой конечной реполяризации ПД. В эту фазу ПД снижается до –95, формируя потенциал покоя и завершая фазу медленного изгнания крови. Заключительная фаза медленного изгнания совпадает с фазой конечной быстрой реполяризации ПД и отображается на ЭКГ второй половиной зубца Т.
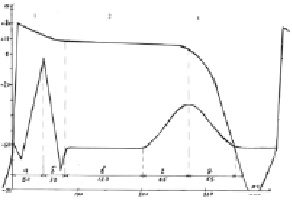
Электрическая систола желудочков, отображаемая на ЭКГ интервалом Q-T, по сути своей отображает потенциал действия (ПД) всех кардиомиоцитов, формируя определенное соответствие между ПД и ЭКГ, которое представлено на рис. 2.
Рис. 2. Сопряжение фаз ПД с фазами гемодинамики систолы желудочков и элементов ЭКГ
Отрезок (а). Фаза асинхронного напряжения миокарда, отображаемая на ЭКГ зубцами Q и вершиной восходящего колена зубца R, длительностью 50 мс.
Отрезок (б). Фаза изометрического напряжения миокарда, отображаемая на ЭКГ нисходящим коленом зубца R и зубцом S, длительностью 30 мс.
Отрезок (а + б). Фаза напряжения миокарда, обусловленная деполяризацией кардиомиоцитов всего миокарда, отображаемая на ЭКГ комплексом QRS, а на графике ПД она совпадает с фазой быстрой начальной реполяризации с длительностью от 50 до 100 мс в зависимости от ЧСС.
Отрезок (в). Фаза асинхронного сокращения миокарда, длящаяся по времени в среднем 120 мс. Отображается на ЭКГ сегментом ST.
Отрезок (г + д). Фаза изометрического сокращения миокарда, длящаяся по времени 130 мс и отображаемая на ЭКГ зубцом Т. Граница фазы плато с фазой быстрой конечной реполяризации проходит посередине зубца Т.
Отрезок (в + г). Часть фазы изгнания, находящейся в границах фазы плато.
Отрезок (в + г + д). Вся фаза изгнания, сопряженная с фазами ПД (фаза плато и фаза конечной быстрой реполяризации), с длительностью, зависящей от ЧСС; на ЭКГ представлена интервалом S-T.
Максимальное перемещение крови из желудочков в кровеносное русло осуществляется в фазу плато и завершается в фазу быстрой конечной реполяризации ПД. Основной пул кальция и действие механизма его внутриклеточного обмена приходится на фазу плато, занимающую определенную долю в фазе изгнания, обеспечивающую выполнение сократительной функции миокарда. Зная долю фазы плато в фазе изгнания, можно оценивать состояние систолической функции миокарда желудочков сердца, используя индекс фазы плато (индекс ФП). Индекс ФП позволяет оценивать физиологический баланс между электрической активностью кардиомиоцитов (ФП) и сердечной гемодинамикой (фаза изгнания).
Индекс ФП = (ФП/ФИ) * 100 %,
где ФП (фаза плато) = Q-T-QRS-1/2T и ФИ (фаза изгнания) = Q-T-QRS.
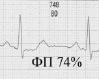
Основной задачей сердечной деятельности является обеспечение организма должным кровотоком в зависимости от его потребности. Это достигается удержанием насосной функции в стабильном состоянии вне зависимости от изменения ЧСС, что может быть продемонстрировано примерами электрокардиограмм при разных ЧСС.
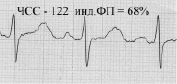
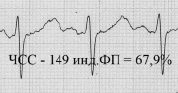
Пример 1. Две ЭКГ одного человека с ЧСС 122 и 149, отображающие постоянство индекса ФП вне зависимости от ЧСС
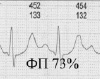
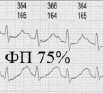
Пример 2. Три ЭКГ одного человека, отображающие постоянство индекса ФП вне зависимости от ЧСС
Как видно из приведенных примеров, при изменении ЧСС сохраняется временной баланс между фазой плато и фазой изгнания, отображенный в индексе ФП.
Обязательным условием, ведущим к высокой достоверности оценки систолической функции миокарда желудочков сердца с помощью ЭКГ, является нормативный баланс между фактической и должной величиной интервала Q-T (Q-T/Q-Td * 100 = 100 ± 10 %) [12].
Вышеприведенная формула расчета индекса ФП ориентирована на лиц с нормальным показателем соотношения фактического и должного интервала Q-T.
Использование для оценки систолической функции желудочков сердца индекса ФП показало высокую корреляцию с показателями фракции выброса – ФВ. В сравнительном анализе корреляции ФВ с индексом ФП приняли участие 100 человек с нормативным значением ФВ и нормальным соотношением длительности фактической электрической систолы желудочков (Q-T) с должным значением Q-T (табл. 1).
Данные сравнения усредненных значений систолической функции левого желудочка по УЗИ и ЭКГ у лиц с исходно нормальной ФВ и нормальным интервалом Q-T
Соотношение SpO2 / FiO2 при поступлении в больницу является показателем раннего развития острого респираторного дистресс-синдрома у пациентов из группы риска
Индекс оксигенации (oxygenation index, OI; PF ratio – PF соотношение; респираторный индекс, PaO2 / FiO2 ) — это параметр, используемый в анестезиологии-реаниматологии и интенсивной терапии для оценки функции обмена кислорода в легких. Расчет индекса оксигенации производят по формуле, как соотношение PaO2 / FiO2 (отношение парциального напряжения кислорода в артериальной крови к фракции кислорода на вдохе). Данный критерий относится к международным шкалам, которые ежедневно используются в рутинной практике анестезиолога. Однако не всегда есть возможность исследования артериальной крови, в данной статье описывается возможность оценки соотношения насыщения кислородом к фракции вдыхаемого кислорода (SpO (2) / FiO (2)) как прогностического маркера в плане развития острого респираторного дистресс-синдрома (ОРДС)
ЦЕЛЬ: Отношение насыщения кислородом к фракции вдыхаемого кислорода (SpO (2) / FiO (2) ) было подтверждено в качестве суррогатного маркера парциального давления кислорода к доле вдыхаемого кислорода у механически вентилируемых пациентов с острым респираторным дистресс-синдромом (ОРДС). Достоверность измерений SpO (2) / FiO (2) при прогнозировании ОРДС не изучалась. Недавно был разработан показатель прогнозирования травм легких (LIPS- Lung Injury Prediction Score), чтобы помочь идентифицировать пациентов с риском развития ОРДС.
МЕТОДЫ: Это был вторичный анализ когорты LIPS-1. Многофакторная логистическая регрессия включала все установленные переменные для LIPS, оценки острой физиологии и хронического здоровья, возраста и сопутствующих состояний, которые могут влиять на SpO (2) / FiO ). Первичным результатом было развитие ОРДС в стационаре. Вторичные исходы включали в себя смертность в больнице, больничный день развития ОРДС и больничный день смерти.
Коэффициент атерогенности: маркер агрессии холестерина
Как холестерин влияет на сосуды сегодня широко известно. И большинство знакомы с анализом крови «на холестерин». Однако не все знают, что только общего анализа недостаточно для выводов о поражении сосудов. Так как же получить полную картину «холестериновой агрессии»? Кому актуален такой анализ? И чем понизить коэффициент атерогенности?
Что покажет коэффициент атерогенности
Коэффициент атерогенности – это отношение «плохого» холестерина к «хорошему». И именно это соотношение и отражает риск развития или степень поражения сосудов.
Но почему для выводов недостаточно оценки только «плохого» холестерина? Ведь, по сложившемуся мнению, именно его повышение – маркер риска сосудистых патологий.
Все дело в том, что деление холестерина на плохой и хороший крайне условно. И обе фракции одинаково необходимы для здоровья.
Липопротеины высокой плотности (ЛПВП)
считаются «хорошими», поскольку:
Здесь холестерин, как вещество ценное, используется для синтеза витамина D и желчи.
А, помимо прочего, холестерин:
Очевидно, что холестерин очень нужен организму, но его избыток в крови вредит и повышает риски сосудистых заболеваний.
Липопротеины низкой и очень низкой плотности (ЛПНП и ЛПОНП)
получили статус «вредных» за способность легко отдавать холестерин тканям.
А тот, в свою очередь:
В сосудах такие «заплатки» снижают возможности растяжения, то есть расширения и снижения давления. И чем больше таких участков и их площадь, тем меньше эластичность сосудистой стенки.
И если повышается и «хороший», и «плохой» холестерин (коэффициент атерогенности 2-3) – организм пока справляется с поражением, площадь пораженных участков не велика, излишки холестерина удаляются вовремя, а само нарушение легко поддается коррекции.
А преобладание «плохих» фракций (значение коэффициента атерогенности больше 3,5) говорит о масштабном нарушении липидного обмена. Что может привести к развитию атеросклероза и высокому риску инфаркта и инсульта.
Кому актуален анализ
Что может исказить результат
Как уже было отмечено, холестерин служит «скелетом» множества соединений и «цементом» всех клеточных стенок. И именно по этой причине повышение холестерина и его отдельных фракций может быть связано не только с патологией сосудов.
Так, повышение коэффициента атерогенности наблюдается при:
Снижение показателя клинического значения не имеет, однако имеет место при:
Как понизить коэффициент атерогености
Способы нормализации показателя полностью определяются его исходным уровнем и причиной повышения. В любом случае улучшить показатели липидного обмена может:
Роль холтеровского мониторирования в обследовании больных без ишемической болезни сердца
Главные технические компоненты методики – регистратор, на котором осуществляется длительная запись электрокардиограммы и дешифратор, проводящий анализ полученной записи. Минимальный вес наиболее современных регистраторов коммерческих систем, составляет 80 гр. Используются и кассетные и твердотельные регистраторы. Последними современными цифровыми системами являются дисковые регистраторы, имеющие объем памяти 80-200 Мбайт и “событийные “ регистраторы (event recorder), позволяющие записывать только определенные участки ЭКГ.
Всем больным при ХМ рекомендуется вести дневник активности с записью возникающей в процессе исследовании симптоматики, в котором необходимо отражение характера основной активности в период исследования (прогулки, вождение автомобиля, учебные занятия, стрессы и т.п.), время приема пищи и лекарственных препаратов, возникающей симптоматики. Стандартно рекомендуется проведение суточного, 24 часового исследования. При редко, но регулярно встречающихся симптомах (1-2 раза в неделю), возможно удлинение времени 24 часовой регистрации до 48 часов.При более редко возникающих симптомах применяются событийные, транстелефонные или имплантированные регистраторы.
Принципы построения клинических показаний к проведению Холтеровского и других видов амбулаторного мониторирования делятся на три класса. К I Классу относятся состояния при которых использование методики является очевидно необходимым для постановки правильного диагноза, назначения терапии и оценки ее эффективности. II Класс показаний подразумевает состояние когда использование методики может вызывать расхождение мнения специалистов в оправданности и эффективности ее применения. Данный Класс разделяется на два подкласса: IIa подразумевает большую предпочтительность в использовании методики, а IIb – менее явную необходимость ее применения. III Класс включает показания когда, согласно общему мнению специалистов, применение методики может достаточно мало добавить информации, влияющей на постановку диагноза, прогноз и тактику лечения больного и должно иметь специальное обоснование для проведения исследования в этой группе. Ниже приведены используемые в нашем центре показания к проведению ХМ у больных без ишемической болезни сердца, детей, подростков и лиц молодого возраста, сформированные на основании последних рекомендаций ведущих международных кардиологических организаций и длительного отечественного опыта в этой области.
ПОКАЗАНИЯ К ПРОВЕДЕНИЮ ХОЛТЕРОВСКОГО МОНИТОРИРОВАНИЯ У БОЛЬНЫХ БЕЗ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА, ДЕТЕЙ И ПОДРОСТКОВ.
1. Обследование больных с высоким риском развития жизнеугрожающих сердечных аритмий и внезапной сердечной смерти: синдром удлиненного интервала QT; синдром Бругада; идиопатическая желудочковая тахикардия; брадикардия менее 50 уд/мин; первичная легочная гипертензия; АВ блокада 3 степени; аритмогенная дисплазия правого желудочка; частая желудочковая экстрасистолия; сибсы внезапно погибших на первом году жизни детей; дилатационная и гипертрофическая кардиомиопатия.
2. Синкопе, предсинкопе или головокружения у больных с выявленной сердечной патологией, ранее документированной аритмией, искусственным водителем ритма или на фоне физической нагрузки.
3. Возникновение синкопе или предсинкопе на фоне приема препаратов с проаритмогенным эффектом.
4. Синкопе или предсинкопе, причина которых не выявлена другими методами.
5. Сердцебиение у больных оперированных по поводу врожденного порока сердца или с выраженной недостаточностью кровообращения.
6. Оценка эффективности антиаритмической терапии.
1. Синкопе, предсинкопе или жалобы на частое сердцебиение в отсутствии выявленных сердечных заболеваний
2. Оценка ритма сердца после назначения антиаритмических препаратов с высоким риском проаритмогенного эффекта.
3. Асимптоматическая АВ блокада 2 степени.
4. Транзиторная АВ блокада 1 степени после хирургической коррекции врожденного порока сердца или катетерной радиочастотной аблации.
5. Оценка вариабельности ритма сердца у больных с кардиальной патологией.
6. Пароксизмальная суправентрикулярная тахикардия.
1. Оценка асимптоматических больных оперированных по поводу врожденного порока сердца, прежде всего с высокой степенью недостаточности кровообращения или аритмиями.
2. Дети младше 3 лет с любыми аритмиями.
3. Больные с постоянной суправентрикулярной тахикардией.
4. Желудочковая экстрасистолия на ЭКГ покоя или стресс тесте.
5. Обследование детей из семей где регистрировались случаи внезапной смерти в молодом возрасте у родственников первой линии.
1. Синкопе, предсинкопе явно некардиальной природы.
2. Боли в груди без выявленных заболеваний сердца.
3. Рутинное обследование спортсменов.
4. Короткие сердцебиения без выявленных заболеваний сердца.
5. Асипмтоматический феномен Вольфа-Паркинсона-Уайта.
6. Оценка вариабельности ритма сердца.
Норма при ХМ
Таблица 1. Показатели динамики ЧСС по данным холтеровского мониторирования у детей первого года жизни.
| Период суток | Возраст | |||
| 1 мес | 2-3 мес | 4-5 мес | 6-12 мес | |
| Бодрствование | 156,7±7,3 | 150,5±0,7 | 147,4±5,7 | 146,7±6,4 |
| Дневной сон | 134,9±8,5 | 128,1±7,6 | 121,4±8,4 | 123,3±6 |
| Ночной сон | 137±12,8 | 124,3±8,4 | 121,2±5,6 | 118,2±8,8 |
| Среднесуточная | 143,8±5,2 | 135,4±8 | 130,9±5,2 | 130,2±6,1 |
Таблица 2. Нормальные показатели половозрастной динамики ЧСС (уд/мин) при ХМ у здоровых детей от до 15 лет
| Авторы | n | Возраст (лет) | Пол | Ср. Дневная ЧСС (уд/мин) | Ср. ночная ЧСС (уд/мин) |
| Brodsky M. | 50 | 22 ± 0,7 | M | 80 | 56 |
| Stein Рh. | 30 | 33 ± 4 | Ж | 86 | 64 |
| Stein Ph. | 30 | 33 ± 4 | Ж | 86 | 65 |
| Stein Ph. | 30 | 67 ± 3 | М | 79 | 62 |
| Stein Ph. | 30 | 67 ± 3 | Ж | 83 | 65 |
Кроме средних значений, при оценке результатов исследования, важное значение имеет знание пограничных параметров ЧСС, выход за которые можно считать признаками патологии. Критерии брадикардии при ХМ следующие: новорожденные > 0,1 мв, регистрируемые продолжительностью не менее 1 мин. Максимальной чувствительностью (89%) в выявлении ишемических изменений в миокарде является отведение СМ5. Результаты последних исследований подтверждают высокий риск гипердиагностики ишемии миокарда по анализу только результатов ХМ. По результатам наших исследований, максимальный подъем сегмента ST до + 4 мм отмечался у 5-25% здоровых детей в различных возрастных группах.
Интервал QT является одним из наиболее клинически значимых параметров ЭКГ. Основным методом измерения QT является вычисление корригированного интервала QT (QTc) по формуле Bazett QTc = QT/ Ц RR. При данном методе расчета, QTc не должен превышать 440 мс у взрослых и 460 мс у детей раннего возраста. При ХМ отмечено, что максимальное значение QT, независимо от ЧСС не выходит за определенные краевые параметры: в 0 – 1 г до 400 мс; в 2-3 года до 430 мс; в 4-7 лет до 460 мс; в 8-15 лет до 480 мс и старше 15 лет до 500 мс. У всех здоровых лиц при ХМ регистрируются короткие паузы ритма, не превышающая предшествующий RR более, чем в 2 раза.
Cуммируя данный раздел можно объединить основные показатели «нормальной» суточной ЭКГ, к которым относятся:
короткие паузы ритма от 1000 мс у новорожденных до 1750 мс у взрослых;
подъем сегмента ST до 1 мм у детей старше 10 лет и взрослых;
изменения амплитуды Т зубца в положительном диапазоне;
максимальная продолжительность интервала QT от 400 мс у новорожденных до 500 мс у взрослых, независимо от уровня ЧСС;
наличие коротких периодов изменения амплитуды Р зубца, выскальзывающих суправентрикулярных и узловых ритмов.
Выявление при ХМ единичных суправентрикулярных и желудочковых экстрасистол, ночных периодов АВ блокады 1 степени, не требует у «практически» здоровых лиц дообследования и/или специфической антиаритмической терапии, однако является ранним проявлением риска развития функциональных кардиопатий и неспецифических вегетативных дисфункций. Выявление более сложных нарушений ритма сердца требует дообследования, для исключения органического поражения сердца и более сложных видов аритмии.
Методы анализа ХМ
Современные системы ХМ позволяют кроме ЭКГ анализировать вариабельность ритма сердца (ВРС), проводить выявление поздних желудочковых потенциалов. Среди методов оценки ВРС наиболее информативными при ХМ являются методы геометрического и временного (time domain) анализа. К первым относится оценка интервальных и дифференциальных гистограмм RR интервалов и пульсограмм (тренда ЧСС) суточного ритма сердца. Оценка параметров ВРС позволяет определить характер вегетативной регуляции ритма сердца. Снижение ВРС, как правило, свидетельствует о более неблагоприятном прогнозе заболевания.
Последним принципиальным рубежом ЭКГ мониторирования является использование имплантируемых регистраторов ритма с петлеобразной системой записи, позволяющих проводить непрерывную регистрации ЭКГ до 14 месяцев. Суть методики заключается в подкожной имплантации в субпекторальную область портативного устройства, регистрирующего ЭКГ по петлевому типу (запись, затем стирание, если через определенное время не активирована функция запоминания записи). Размеры регистрирующего устройства 61 х 19 х 8 мм, вес – 17 г. При возникновении синкопе или других симптомов больной с помощью специального прибора активируют запись ЭКГ за определенное время до и после активации (в последних моделях, функция записи активируется автоматически).
В настоящее время клинический опыт применения данной методики мониторирования в России невелик. Но полученные результаты свидетельствуют о высокой перспективности ее использования при обследовании больных с редкими синкопальными состояниями, причина которых не выявляется другим способом. В 1999 г. в нашей клинике была произведена первая в России имплантация данных регистраторов. Показаниями к проведению исследования были редкие (1 раз в 4-6 месяцев) синкопе, у детей без выявленной причины обмороков по результатам неврологического, эндокринологического и стандартного кардиологического обследования. Через 13 мес. после имплантации регистратора у одной больной во время единственного синкопе выявлена асистолия 3,88 с, сопровождающаяся синкопе. До этого она в течение 4 лет лечилась от эпилепсии. Применение данной методики оправдано при формировании показаний к имплантации постоянных антиаритмических устройств (кардиостимуляторов и дефибрилляторов) у больных с невыявленными другими способами причинами потенциально жизнеугрожающей симптоматики или синкопе.
Заключение по результатам ХМ
Значительной практической проблемой является формирование финального заключения по результатам ХМ. Формального универсального протокола в настоящее время не существует. Основные позиции предполагаемого оптимальный протокола по результатам ХМ, подробно отражены в нашем руководстве 2000 г. Основными его позициями являются:
• Отражение основной динамики ЧСС в сравнении с возрастной нормой
(среднесуточная, средняя дневная, средняя ночная ЧСС, циркадный индекс)
: аритмии и основные ЭКГ феномены, время их возникновения и симптомы, оценка изменений сегмента ST и других параметров ЭКГ во время жалоб, циркадный тип аритмии
• Результаты дополнительных методов
— ВРС, которая включает кроме традиционных методов временного или частотного анализа (в зависимости от опций в конкретной коммерческой системе), оценку структуры ночного сна по анализу тренда ЧСС, ЦИ (оценку функций концентрации и разброса) у больных с несинусовым ритмом;
— поздние потенциалы желудочков;
— динамика интервала QT (на минимальной ЧСС, среднесуточный корригированный и другие параметры);
Оценка работы ИВР (обязательное указание типа ИВР и режима его программирования – VVI, DDD и т.д.).
В каждом дополнительном разделе данные интерпретируются в соответствие с техническими возможностями используемой коммерческой системы ХМ. Пример типового финального заключения по результатам ХМ, используемого в нашем центре приведен ниже.
Тип аппарата: OXFORD MEDILOG
Дима Л. Возраст 15 лет
Продолжительность исследования: 11:00 – 10:00 (23 часа)
: Желудочковая тахикардия. Аритмогенная дисплазия правого желудочка? Синкопе.
Класс показаний к ХМ
Максимальная ЧСС (син. ритм) 130 уд/мин в 11:15, минимальная ЧСС 45 уд/мин в 04:36, циркадный индекс = 1,6 (норма 1,24-1,44).
Частая правожелудочковая экстрасистолия, всего 2350 за 23 часа, максимально в период 12-15 часов (200-300/час), минимально с 03 до 06 часов (0-23/час). Единичные суправентрикулярные экстрасистолы (всего 22), максимально 5 в 09-10 часов. Парные желудочковые экстрасистолы, всего 12 (максимально в 13-14:00), залпы мономорфной правожелудочковой тахикардии с частотой 140-160 уд/мин от 3 до 34 комплексов, всего 524, максимально в периоды 12-13 (80) и 14-15 (72) часов, минимально 22-23/час (1).
При оценке ритма в режиме суперимпозиции в отведении СМ1 (V1) транзиторные нарушения внутрижелудочкового проведения по типу эпсилон волны, более выраженные в ночное время.
Частые паузы ритма 1500-1700 мс, максимальная пауза ритма за счет синусовой аритмии 1763 мс (норма до 1500 мс).
Автоматический анализ QT-интервала.