какие реакции являются экзотермическими
Классификация реакций
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно сложное вещество. Примеры:
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами. Часто обмен происходит анионами/катионами:
AgF + NaCl = AgCl↓ + NaF
Окислительно-восстановительные реакции (ОВР)
Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО, принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Примеры необратимых реакций:
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)
Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой, твердой и газообразной.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество, твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
Реакции и их тепловой эффект
NaOH + HCl = NaCl + H2O + 56 кДж
К экзотермическим реакциям часто относятся реакции горения, соединения.
Исключением является взаимодействие азота и кислорода, при котором тепло поглощается:
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания» в реакции вместо явного +Q при экзотермической реакции могут написать ΔH 0, так как внутренняя энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)
Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик») является примером экзотермического разложения, при котором тепло выделяется.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
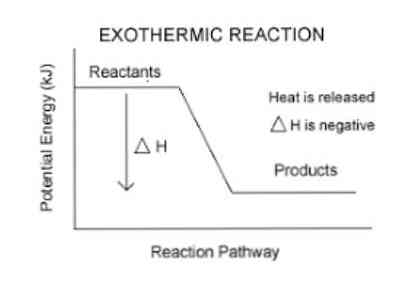
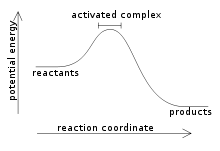
Экзотермическая реакция
Экзотермическая реакция.
Экзотермическая реакция – это химическая реакция, сопровождающаяся выделением теплоты. Экзотермическая реакция отдает тепловую энергию внешней среде. То есть энергия, необходимая для инициирования химической реакции, меньше выделяемой энергии.
Экзотермическая реакция:
Экзотермическая реакция отдает тепловую энергию внешней среде. То есть энергия, необходимая для инициирования химической реакции, меньше выделяемой энергии.
Абсолютное количество энергии в химической системе чрезвычайно трудно измерить или рассчитать. Однако, изменение энтальпии (ΔH) химической реакции намного легче сосчитать.
Для измерения ΔH используют калориметры.
В экзотермической реакции, по определению, изменение энтальпии (ΔH) имеет отрицательное значение:
При сгорании водорода в кислороде (на воздухе), например:
Примеры экзотермических реакций:
– добавление концентрированной серной кислоты в воду,
Процесс экзотермической реакции, типы и примеры
экзотермическая реакция это тип химической реакции, при которой происходит передача энергии, главным образом в форме выделения тепла или света. Название происходит от греческого префикса экзо, что означает «за границей»; и термин «термический», который относится к теплу или температуре.
В этом смысле экзотермические реакции могут передавать другие виды энергии в окружающую среду, где они генерируются, например, при взрывах и способе передачи кинетической и звуковой энергии, когда вещества, находящиеся в газовой фазе при высоких температурах, расширяются. насильственный путь.
Таким же образом, в случае использования батарей, также проводится экзотермическая реакция, только в этом случае транспортируется электрическая энергия..
процесс
Ранее было упомянуто, что когда происходит экзотермическая реакция, происходит выделение энергии, которое можно легче визуализировать в следующем уравнении:
Реагенты (ы) → Продукт (ы) + Энергия
Таким образом, для количественного определения энергии, поглощаемой или выделяемой системой, используется термодинамический параметр, называемый энтальпией (обозначается буквой «H»). Если в системе (в данном случае, химической реакции) происходит выделение энергии в окружающую среду, то изменение энтальпии (выраженное как ΔH) будет иметь отрицательное значение.
В противном случае, если изменение этой меры является положительным, оно отражает поглощение тепла из окружающей среды. Кроме того, величина изменения энтальпии системы является выражением количества энергии, передаваемой в окружающую среду или из нее..
Чем больше величина ΔH, тем больше выделение энергии из системы в окружающую среду.
Это происходит потому, что в этих реакциях чистая энергия, которая выделяется при создании новых связей, больше, чем чистая энергия, используемая при фрагментации связей.
Из вышесказанного можно сделать вывод, что такого рода реакции очень распространены, поскольку продукты реакции имеют количество энергии, запасенное в связях, больше, чем то, что содержится в реагентах..
тип
Существуют различные виды экзотермических реакций в различных областях химии, будь то в лаборатории или в промышленности; некоторые выполняются спонтанно, а другие требуют особых условий или какого-либо типа вещества, такого как катализатор, который будет произведен.
Ниже приведены наиболее важные виды экзотермических реакций:
Реакции горения
Реакции горения представляют собой реакции окислительно-восстановительного типа, которые происходят, когда одно или несколько веществ вступают в реакцию с кислородом, обычно приводя к выделению света и тепловой энергии, то есть света и тепла, когда возникает пламя..
Реакции нейтрализации
Реакции нейтрализации характеризуются взаимодействием между кислотой и щелочным веществом (основанием) с образованием соли и воды, которые проявляют экзотермическую природу..
Реакции окисления
Существует много реакций такого типа, которые демонстрируют экзотермическое поведение, потому что окисление кислорода вызывает выделение большого количества энергии, как это происходит при окислении углеводородов..
Термитная реакция
Эта реакция может давать температуру около 3000 ° C, и из-за высокого сродства алюминиевого порошка с большим количеством оксидов металлов его используют при сварке стали и железа.
Реакция полимеризации
Этот тип реакции возникает тогда, когда реагирует определенное количество химических веществ, называемых мономерами, которые представляют собой единицы, которые при объединении повторяются в цепочках с образованием макромолекулярных структур, называемых полимерами..
Реакция ядерного деления
Этот процесс относится к разделению ядра атома, считающегося тяжелым, то есть с массовым числом (А), превышающим 200, для получения фрагментов или ядер меньшего размера с промежуточной массой..
В этой реакции, где образуются один или несколько нейтронов, выделяется большое количество энергии, потому что ядро с большим весом имеет более низкую стабильность, чем его продукты..
Другие реакции
Существуют также другие экзотермические реакции, имеющие большое значение, такие как обезвоживание некоторых углеводов при взаимодействии с серной кислотой, поглощение воды, в которой гидроксид натрия находится на открытом воздухе, или окисление металлических частиц во многих реакциях коррозии..
примеров
Ниже приведены некоторые примеры экзотермических реакций, которые вызывают изменение энтальпии, которое имеет отрицательное значение из-за того, что они выделяют энергию, как упомянуто выше..
Например, сгорание пропана является спонтанной экзотермической реакцией:
Другой случай экзотермического поведения показан реакцией нейтрализации между карбонатом натрия и соляной кислотой:
Представлено также окисление этанола в уксусную кислоту, используемое в алкотестерах, полная реакция которых показана в следующем уравнении:
Другим классом экзотермической реакции является так называемая термитная реакция, в которой алюминий объединяется с оксидом металла, как показано ниже:
В дополнение к объясненным выше примерам существует множество различных реакций, которые также считаются экзотермическими, такие как разложение определенных органических отходов для компостирования..
Это также подчеркивает окисление люциферинового пигмента под действием фермента люциферазы, чтобы произвести биолюминесценцию, характерную для светлячков, и даже дыхание, среди многих других реакций.
Экзотермические реакции
Экзотермическая реакция — химическая реакция, сопровождающаяся выделением теплоты. Противоположна эндотермической реакции.
Полное количество энергии в химической системе чрезвычайно трудно измерить или подсчитать. С другой стороны, изменение энтальпии ΔH в химической реакции гораздо легче измерить или сосчитать. Для этих целей используют калориметры. Измеренное значение ΔH соотносится с энергией связи молекул следующим образом:
ΔH = энергия, потраченная на разрыв связей (Энергия разрыва химической связи)— энергия, выделенная при образовании связей продуктов реакции.
Для экзотермических реакций эта формула даёт отрицательное значение для ΔH, так как большее значение вычитается из меньшего значения. При сгорании водорода, например:
изменение энтальпии равно ΔH = −483.6 кДж на один моль O2.
Примеры
См. также
Полезное
Смотреть что такое «Экзотермические реакции» в других словарях:
Экзотермические реакции — (от экзо. и греч. therme тепло), биохимические реакции, сопровождающиеся потерей энергии (например, диссимиляция углеводов при дыхании, гидролиз жиров). Ср. Эндотермические реакции. Экологический энциклопедический словарь. Кишинев: Главная… … Экологический словарь
экзотермические реакции — – реакции, протекающие с выделением тепловой энергии. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Экзотермические реакции — – химическая реакция, при которой из реагирующей системы в окружающую среду выделяется тепло. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ и м. А. А. Гвоздева, Москва, 2007 г. 110 стр.] Рубрика… … Энциклопедия терминов, определений и пояснений строительных материалов
экзотермические реакции — [exothermic reactions] химические реакции с выделением теплоты (ΔH Энциклопедический словарь по металлургии
реакции метанирования — Экзотермические реакции процесса газификации [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN methanation reactions … Справочник технического переводчика
Реакции химические — Химическая реакция превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции). В отличие от ядерных реакций, при химических реакциях ядра атомов не меняются … Википедия
Реакции — [reactions]: Смотри также: эндотермические реакции химические реакции экзотермические реакции радиационно химические реакции … Энциклопедический словарь по металлургии
экзотермические реакция — – химические реакции, идущие с выделением тепла. Словарь по аналитической химии [3] … Химические термины
Реакции химические — превращения одних веществ в другие, отличные от исходных по химическому составу или строению. Общее число атомов каждого данного элемента, а также сами химические элементы, составляющие вещества, остаются в Р. х. неизмененными; этим Р. х … Большая советская энциклопедия
Химические реакции — Этим термином называется тот процесс, во время которого взятые тела превращаются в новые, ранее не существовавшие. В русском языке мы имеем два слова для выражения этого понятия: X. взаимодействие и X. превращение. Из них нужно отдать… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Экзотермическая реакция: процесс, виды и примеры
Содержание:
Вэкзотермическая реакция Это тип химической реакции, в которой происходит передача энергии, в основном в форме выделения тепла или света. Например, любая реакция горения, при которой что-то горит, происходит экзотермической реакцией.
В повседневной жизни часто можно наблюдать, как различные экзотермические реакции протекают естественным путем или вызываются изменениями температуры в разных местах. Эти изменения температуры можно измерить с помощью термометра.
В этом смысле экзотермические реакции могут передавать другие типы энергии среде, в которой они возникают, как это происходит при взрывах и их способах передачи кинетической и звуковой энергии, когда вещества, находящиеся в газовой фазе при высоких температурах, расширяются из насильственный способ.
Таким же образом, в случае использования батарей, также осуществляется реакция экзотермического типа, только в этом случае переносится электрическая энергия.
Этим реакциям противостоят эндотермические, поглощающие энергию.
Процесс экзотермической реакции
Ранее было упомянуто, что когда происходит экзотермическая реакция, происходит выделение энергии, что легче визуализировать с помощью следующего уравнения:
Реагент (ы) → Продукт (ы) + Энергия
Таким образом, для количественной оценки энергии, поглощаемой или выделяемой системой, используется термодинамический параметр, называемый энтальпией (обозначается как «H»). Если в системе (в данном случае химической реакции) происходит выделение энергии в окружающую среду, то изменение энтальпии (выраженное как ΔH) будет иметь отрицательное значение.
В противном случае, если отклонение этого измерения положительное, оно отражает поглощение тепла из окружающей среды. Точно так же величина изменения энтальпии системы является выражением количества энергии, которая передается в окружающую среду или из нее.
Чем больше величина ΔH, тем больше отдача энергии из системы в окружающую среду.
Это происходит потому, что в этих реакциях чистая энергия, выделяемая при создании новых связей, превышает чистую энергию, используемую при фрагментации связей.
Из вышеизложенного можно сделать вывод, что этот класс реакций очень распространен, потому что продукты реакции имеют количество энергии, хранящейся в связях, больше, чем та, которая изначально содержалась в реагентах.
Типы экзотермической реакции
Существуют разные виды экзотермических реакций в различных областях химии, будь то в лаборатории или в промышленности; некоторые из них выполняются спонтанно, а другие требуют определенных условий или какого-либо вещества в качестве катализатора.
Наиболее важные типы экзотермических реакций перечислены ниже:
Реакции горения
Реакции нейтрализации
Реакции нейтрализации характеризуются взаимодействием между кислыми частицами и щелочным веществом (основанием) с образованием соли и воды, которые проявляют экзотермический характер.
Реакции окисления
Есть много реакций этого типа, которые демонстрируют экзотермическое поведение, потому что окисление кислорода вызывает выделение большого количества энергии, как это происходит при окислении углеводородов.
Термитная реакция
Эта реакция может привести к температуре около 3000 ° C, и из-за высокого сродства алюминиевого порошка с большим количеством оксидов металлов он используется при сварке стали и железа.
Реакция полимеризации
Этот тип реакции возникает, когда в реакцию вступает определенное количество химических частиц, называемых мономерами, которые представляют собой единицы, которые при объединении повторяются в цепях с образованием макромолекулярных структур, называемых полимерами.
Реакция ядерного деления
Этот процесс относится к разделению ядра атома, считающегося тяжелым, то есть с массовым числом (A) больше 200, для образования более мелких фрагментов или ядер с промежуточной массой.
В этой реакции, когда образуется один или несколько нейтронов, выделяется большое количество энергии, потому что ядро с большим весом имеет меньшую стабильность, чем его продукты.
Другие реакции
Существуют также другие экзотермические реакции, имеющие большое значение, такие как дегидратация некоторых углеводов при взаимодействии с серной кислотой, поглощение воды, представленной гидроксидом натрия на открытом воздухе, или окисление металлических частиц во многих реакциях коррозии.
Примеры экзотермических реакций
Ниже приведены некоторые примеры экзотермических реакций, которые вызывают изменение энтальпии, имеющее отрицательное значение из-за того, что они выделяют энергию:
Зажженная свеча
Процесс сгорания парафина и фитиля свечи вызывает экзотермическую реакцию, которая генерирует тепло и свет.
Поджечь фосфор
Когда спичка горит, возникает реакция между химическими веществами, из которых она состоит, и кислородом, присутствующим в воздухе. Таким образом возникает экзотермическая реакция, которая производит свет и тепло.
Дыхание
Процесс дыхания вызывает экзотермическую реакцию внутри клеток во время газообмена. Таким образом глюкоза вместе с кислородом превращается в углекислый газ и тепло.
Горящие дрова
Сжигание древесины вызывает экзотермическую реакцию, в которой образующийся продукт проявляется в виде тепла и температуры.
Сжигание пропана
Другой случай экзотермического поведения демонстрирует реакция нейтрализации между карбонатом натрия и соляной кислотой:
NaHCO3(водн.) + HCl (водн.) → NaCl (водн.) + H2О (л) + СО2(грамм)
Окисление этанола до уксусной кислоты
Также представлено окисление этанола до уксусной кислоты, используемое в алкотестерах, полная реакция которого показана в следующем уравнении:
Термитная реакция
Стальная стружка + уксус
Эта смесь работает как форма медленного горения, при которой сталь подвергается процессу окисления под действием уксуса.
«Собачий лай»
Эта реакция получила такое название, так как издает звук, похожий на лай собаки.
Реакция протекает в лабораторной пробирке, где смешиваются закись азота, оксид азота и бисульфат углерода.
Стеклянная бутылка + алкоголь
Подобно реакции, вызванной вышеупомянутым экспериментом, стеклянную бутылку протирают спиртом таким образом, чтобы возникло пламя.
Стиральный порошок + вода
Когда мыло стирального порошка растворяется, может наблюдаться экзотермическая реакция. Это один из наиболее легко наблюдаемых примеров экзотермических реакций в домашних условиях.
Зубная паста слона
Этот эксперимент обычно используется для объяснения динамики экзотермических реакций.Он заключается в растворении перекиси водорода в некоторой мыльной среде, в результате чего образуется большое количество пены.
В эту смесь добавляется катализатор (йодид калия), который способствует быстрому разложению пероксида.
Серная кислота + сахар
Процесс обезвоживания сахара вызывает очевидную экзотермическую реакцию. Когда вы смешиваете серную кислоту с сахаром, она обезвоживается, и появляется столб черного дыма, из-за чего окружающая среда пахнет обожженными костями.
Натрий + вода
Натрий или любая щелочная среда сильно реагирует с водой. При добавлении в воду щелочного металла (лития, натрия, калия, рубидия или цезия) он должен вступить в реакцию.
Чем выше номер элемента в периодической таблице, тем сильнее будет реакция.
Ацетат натрия
Ацетат натрия известен как горячий лед. Этот материал начинается с кристаллизации замороженных растворов, которые вместо холода выделяют тепло.
Из-за своего внешнего вида он называется «лед», но кристаллизованный ацетат натрия на самом деле является одним из наиболее распространенных материалов, используемых для изготовления грелок для рук.
Сода + уксус
Джинн в бутылке
В этом эксперименте перекись водорода (перекись водорода) смешивается с перманганатом калия. Таким образом, перманганат разрушает перекись водорода, вызывая выделение большого количества дыма и тепла.
Взрывоопасные мармеладные мишки
Молния в трубке
Эта реакция возникает, когда едкая кислота смешивается со спиртом или ацетоном.
Таким образом, можно увидеть бурную химическую реакцию, которая приводит к генерации света в трубке, подобного свету молнии.
Заморозить воду
Во время этого процесса вода выделяет энергию в виде тепла, поэтому, когда кубики воды замерзают, происходит экзотермическая реакция.
Коррозия металлов
Чистые металлы, то есть в их естественном состоянии, когда они вступают в контакт с воздухом, вызывают реакцию окисления вместе с выделением тепла, поэтому этот процесс считается экзотермическим.
Процесс сжигания газа
Другие
В дополнение к ранее объясненным примерам, существует большое разнообразие реакций, которые также считаются экзотермическими, например, разложение определенных органических веществ в отходах для компостирования.
Это также подчеркивает окисление пигмента люциферина под действием фермента люциферазы, вызывающее характерную для светлячков биолюминесценцию и даже дыхание среди многих других реакций.
Ссылки
Долихоцефалия: причины, симптомы, диагностика, лечение