Реактив ларионовой как приготовить
Определение белка (унифицированный метод Брандберга—Робертса—Стольникова)
В основу метода положена кольцевая проба Геллера, заключающаяся в том, что на границе азотной кислоты и мочи при наличии белка происходит его коагуляция и появляется белое кольцо.
Необходимый реактив
30%-ный раствор азотной кислоты (относительная плотность 1,2) или реактив Ларионовой.
Приготовление реактива Ларионовой: 20—30 г хлорида натрия растворяют при нагревании в 100 мл дистиллированной воды, дают остыть, фильтруют. К 99 мл фильтрата приливают 1 мл концентрированной азотной кислоты.
Ход исследования
В пробирку наливают 1—2 мл азотной кислоты (или реактива Ларионовой) и осторожно, по стенке пробирки, наслаивают такое же количество профильтрованной мочи. Появление тонкого белого кольца на границе двух жидкостей между 2 и 3-й минутой указывает на наличие белка в концентрации примерно 0,033 г/л. Если кольцо появляется раньше 2 мин после наслаивания, мочу следует развести водой и провести повторное наслаивание уже разведенной мочи. Степень разведения мочи подбирают в зависимости от вида кольца, т.е. его ширины, компактности и времени появления.
При нитевидном кольце, появившемся ранее 2 мин, мочу разводят в 2 раза, при широком — в 4 раза, при компактном — в 8 раз и т.д. Концентрацию белка при этом вычисляют путем умножения 0,033 на степень разведения и выражают в граммах на 1 л (г/л).
Иногда белое кольцо получается при наличии больших количеств уратов. В отличие от белкового кольца уратное появляется немного выше границы между двумя жидкостями и растворяется при легком нагревании.
Определение белка в моче методом Брандберга – Робертса – Стольникова
Метод Брандберга–Робертса–Стольникова относится к полуколичественным методам определения общего белка в моче. В основу метода положена кольцевая проба Геллера, заключающаяся в том, что на границе азотной кислоты и мочи при наличии белка происходит его коагуляция и появляется белое кольцо.
Реактивы
50% раствор азотной кислоты или реактив Ларионовой.
Приготовление реактива Ларионовой: готовят насыщенный раствор хлорида натрия (20 – 30 г соли растворяют в 100 мл воды при подогревании, дают отстояться до охлаждения). Надосадочную жидкость сливают, фильтруют. К 99 мл фильтрата добавляют 1 мл концентрированной азотной кислоты. Вместо азотной кислоты можно добавить 2 мл концентрированной соляной кислоты.
Ход определения
В пробирку наливают 1 – 2 мл азотной кислоты (или реактива Ларионовой), дают кислоте стечь со стенок пробирки (5 – 8 минут), иначе при наслаивании белковой мочи образуется муть вследствие смешения азотной кислоты на стенках пробирки с мочой, что мешает образованию отчетливого кольца. Поэтому следует предварительно приготовить серию пробирок с кислотой. Пипеткой осторожно по стенке пробирки наслаивают такое же количество профильтрованной прозрачной мочи, стараясь не взбалтывать жидкость в пробирке. Появление тонкого белого кольца на границе двух жидкостей между 2-й и 3-й минутой указывает на наличие белка в концентрации примерно 0,033 г/л. Время наслаивания считают за четверть минуты.
Если кольцо появляется раньше 2 мин после наслаивания, мочу следует развести водой и провести повторное наслаивание уже разведенной мочи. Степень разведения мочи подбирают в зависимости от вида кольца, т. е. его ширины, компактности и времени появления. При нитевидном кольце, появившемся раньше 2 мин, мочу разводят в 2 раза, при широком – в 4 раза, при компактном – в 8 раз и т. д. Разведение мочи делают в мерной центрифужной пробирке, наливая мочу до метки 1 мл и доливают водой до той метки, во сколько раз делается разведение. Содержимое пробирки тщательно перемешивают пастеровской пипеткой с баллоном. Если при разведении мочи появляется муть, то смесь нужно вновь отфильтровать и только прозрачный фильтрат наслаивать на азотную кислоту. Концентрацию белка при этом вычисляют путем умножения 0,033 на степень разведения и выражают в граммах на литр (г/л). Подбирают такое разведение мочи, чтобы при наслаивании ее на азотную кислоту кольцо появилось на 2 – 3-й минуте.
В случае, если с неразведенной или разведенной мочой кольцо образуется между 1-й и 4-й минутой, можно пользоваться поправкой Эрлиха-Альтгаузена, для того, чтобы не разводить мочу дополнительно (это экономит время). Авторы предложили определить время появления нитевидного кольца и внести в расчет поправку на время. В этом случае количество белка рассчитывают, умножая 0,033 г/л на степень разведения и на поправку.
При образовании кольца до истечения 1 минуты необходимо сделать одно дробное разведение, а именно в 1,5 раза (две части мочи и 1 часть воды). Это разведение также учитывается при расчете количества белка в моче.
Пример определения общего белка в моче методом Брандберга-Робертса-Стольникова.
При наслоении мочи на реактив сразу образуется широкое кольцо. Разводят мочу в 4 раза (1 часть мочи + 3 части воды), наслаивают; получается сразу нитевидное кольцо. Нужно имеющееся разведение развести еще в 2 раза; при наслаивании этого разведения образуется кольцо через 1,5 минут. Дальше можно не разводить.
Расчет белка: мочу развели в 4 и 2 раза, следовательно, в 8 раз. Количество белка равно 0,033*8*1 1 /4 = 0,33 г/л
Недостатки метода Брандберга-Робертса-Стольникова:
Литература:
Похожие статьи
Кольцевая проба Геллера
Кольцевая проба Геллера относится к качественным реакциям определения белка в моче. Так как она основана на реакции коагуляции, то исследуемая моча должна соответствовать определенным требованиям: быть прозрачной и иметь кислую реакцию.
Раздел: Анализ мочи
Определение белка в моче пробой с 20% сульфосалициловой кислотой
Проба с 20% сульфосалициловой кислотой относится к качественным реакциям определения белка в моче. Так как она основана на реакции коагуляции, то исследуемая моча должна соответствовать определенным требованиям: быть прозрачной и иметь кислую реакцию.
Раздел: Анализ мочи
Качественные методы определения общего белка в моче
Все качественные пробы на белок в моче основаны на способности белков к денатурации под влиянием различных физических и химических факторов. При наличии белка в исследуемом образце мочи появляется либо помутнение, либо выпадение хлопьевидного осадка.
Раздел: Анализ мочи
Полуколичественные методы определения общего белка в моче
В настоящее время для определения белка в моче все чаще используются диагностические полоски. Для полуколичественного определения белка в моче на полоске в качестве индикатора чаще всего используется краситель бромфеноловый синий в цитратном буфере. О содержании белка в моче судят по интенсивности сине-зеленой окраски, развивающейся после контакта реакционной зоны с мочой.
Раздел: Анализ мочи
Кетоновые тела в моче. Методы определения
Принцип обнаружения кетоновых тел в моче. Нитропруссид натрия в щелочной среде реагирует с кетоновыми телами, образуя комплекс, окрашенный в розовато-сиреневый, сиреневый или фиолетовый цвет. Чувствительность проб около 50 мг/л кетоновых тел. Полуколичественную оценку результатов можно дать в интервале от 150 до 1500 мг/л.
Раздел: Анализ мочи
Кольцевая проба Геллера
Кольцевая проба Геллера относится к качественным реакциям определения белка в моче. Так как она основана на реакции коагуляции, то исследуемая моча должна соответствовать определенным требованиям: быть прозрачной и иметь кислую реакцию.
Реактивы
Концентрированная (или 50%-я) азотная кислота или реактив Ларионовой. Приготовление реактива Ларионовой: готовят насыщенный раствор хлорида натрия (20 – 30 г соли растворяют в 100 мл воды при подогревании, дают отстояться до охлаждения). Надосадочную жидкость сливают, фильтруют. К 99 мл фильтрата добавляют 1 мл концентрированной азотной кислоты. Вместо азотной кислоты можно добавить 2 мл концентрированной соляной кислоты.
Ход определения
В пробирку наливают 1 – 1,5 мл азотной кислоты или реактива Ларионовой и пипеткой осторожно по стенке пробирки наслаивают такое же количество мочи, стараясь не взбалтывать жидкость в пробирке. При наличии белка на границе двух жидкостей появляется белое кольцо. Реакцию оценивают на черном фоне и учитывают время появления нитевидного кольца. Чувствительность пробы 0,033 г/л. При таком содержании белка на границе жидкостей появляется белое нитевидное кольцо между 2-й и 3-й минутами.
Недостатки пробы Геллера
Проба Геллера с реактивом Ларионовой
Более четкий результат пробы Геллера получается, если использовать реактив Ларионовой. Проба с реактивом Ларионовой имеет ряд преимуществ:
Литература:
Похожие статьи
Определение белка в моче пробой с 20% сульфосалициловой кислотой
Проба с 20% сульфосалициловой кислотой относится к качественным реакциям определения белка в моче. Так как она основана на реакции коагуляции, то исследуемая моча должна соответствовать определенным требованиям: быть прозрачной и иметь кислую реакцию.
Раздел: Анализ мочи
Определение белка в моче методом Брандберга – Робертса – Стольникова
Метод Брандберга–Робертса–Стольникова относится к полуколичественным методам определения общего белка в моче. В основу метода положена кольцевая проба Геллера, заключающаяся в том, что на границе азотной кислоты и мочи при наличии белка происходит его коагуляция и появляется белое кольцо.
Раздел: Анализ мочи
Качественные методы определения общего белка в моче
Все качественные пробы на белок в моче основаны на способности белков к денатурации под влиянием различных физических и химических факторов. При наличии белка в исследуемом образце мочи появляется либо помутнение, либо выпадение хлопьевидного осадка.
Раздел: Анализ мочи
Неорганизованные осадки мочи
Неорганизованные осадки мочи состоят из различных солей, органических соединений и лекарственных веществ, осевших в моче в виде кристаллов или аморфных тел. Однако чаще неорганизованный осадок состоит преимущественно из солей.
Раздел: Анализ мочи
Кетоновые тела в моче. Методы определения
Принцип обнаружения кетоновых тел в моче. Нитропруссид натрия в щелочной среде реагирует с кетоновыми телами, образуя комплекс, окрашенный в розовато-сиреневый, сиреневый или фиолетовый цвет. Чувствительность проб около 50 мг/л кетоновых тел. Полуколичественную оценку результатов можно дать в интервале от 150 до 1500 мг/л.
Раздел: Анализ мочи
Качественное определение белка в моче
Оснащение рабочего места
В состав рабочего места по определению белка в моче входят следующие элементы:
Методики определения белка в моче
Все методики, применяющиеся для качественного определения белка в моче, основаны на свертывании белка. Свертывание белка проявляется выраженным в разной степени помутнением (от опалесценции до большой мутности) или выпадением хлопьев.
Качественное определение белка в моче может быть проведено одним из следующих способов:
Перед качественным определением белка в моче проводят следующую подготовительную работу:
1. Мутную мочу фильтруют через бумажный фильтр. Если получить прозрачный фильтрат не удается, производят повторное фильтрование через тот же фильтр или же смешивают мочу с небольшим количеством инфузорной земли или талька, после чего ее фильтруют.
2. Если моча имеет щелочную реакцию, ее подкисляют 10% раствором уксусной кислоты до слабокислой реакции под контролем лакмусовой или универсальной индикаторной бумажки.
3. При малом содержании солей (светло-желтая или бледно-желтая моча с малым удельным весом) к каждой
пробе добавляют несколько капель насыщенного раствора поваренной соли, так как недостаток солей обусловливает свертывание белка.
4. Степень помутнения наблюдают с помощью черного фона. В качестве фона используют черный картон или черную бумагу, применяемую в фотографии. Учет реакции на черном фоне позволяет выявить малейшую степень помутнения.
В отдельном штативе располагают пронумерованные пробирки. В них производят одну из описанных ниже реакций.
1. Проба кипячением с 10% раствором уксусной кислоты. Для постановки этой пробы необходим 10% раствор уксусной кислоты, который готовят следующим образом: 10 мл ледяной уксусной кислоты помещают в цилиндр и доливают дистиллированной водой до метки 100 мл.
Техника определения белка. В химическую пробирку помещают 10—12 мл отфильтрованной мочи слабокислой реакции. Затем верхнюю часть пробирки с мочой осторожно нагревают до кипения и добавляют в нее 8—10 капель 10% раствора уксусной кислоты. Пробирку с мочой рассматривают на черном фоне в проходящем свете. При наличии белка в моче появляется мутность разной степени (от опалесценции до большой мутности) или выпадают хлопья. Контролем служит нижняя часть пробирки, не подвергавшаяся нагреванию. Этой пробой обнаруживают количество белка, начиная с 0,015%о (%о — promille).
2. Реакция с 20% раствором сульфосалициловой кислоты. 20 % раствор сульфосалициловой кислоты готовят следующим образом: 20 г сульфосалициловой кислоты растворяют в 70-80 мл дистиллированной воды, переводят в цилиндр емкостью 100 мл и доливают дистиллированной водой до метки. Приготовленный реактив хранят в посуде из темного стекла.
Техника определения белка. В две пробирки одинакового диаметра помещают по 2—3 мл отфильтрованной мочи слабокислой реакции, в одну из пробирок к моче прибавляют 3—4 капли 20% раствора сульфосалициловой кислоты, другая пробирка служит контролем. При наличии белка в пробирке с реактивом появляется мутность или выпадают хлопья свернувшегося белка. В контрольной пробирке жидкость остается прозрачной. Сульфосалициловая кислота наряду с белком сыворотки осаждает альбумозы (пептиды), представляющие собой продукт распада белка. С целью уточнения причины помутнения мочи пробирку с мочой подогревают. Мутность, причиной образования которой оказались сывороточные белки, усиливается, мутность же, обусловленная присутствием альбумоз, исчезает. Эта проба имеет ту же чувствительность, что и предыдущая.
3. Реакция с 50 % раствором азотной кислоты (проба Геллера). 50% раствор азотной кислоты готовят следующим образом: к 50 мл азотной кислоты удельного веса 1,2-1,4 приливают 50 мл дистиллированной воды (разведение 1:1).
Техника определения белка. В узкую небольшую пробирку (тина агглютинационной) наливают 1 мл 50% азотной кислоты. В пипетку с узким оттянутым концом набирают 1 мл отфильтрованной исследуемой мочи, наслаивают на реактив и пробирку переводят в вертикальное положение. При наличии белка на границе жидкостей появляется белое кольцо. Время появления кольца, его свойства зависят от количества белка: если белка мало, то кольцо появляется не сразу, поэтому за его появлением следят в течение 2,5-3 минут. Минимальное количество белка, определяемое этим методом, 0,033°/оо. При меньшем содержании белка в моче кольцо не образуется. Учет результатов реакции производят на черном фоне в проходящем свете.
Техника определения белка такая же, как и при реакции с 50% раствором азотной кислоты (проба Геллера), но вместо 1 мл 50% раствора азотной кислоты в пробирку наливают 1 мл реактива Ларионовой и на него наслаивают 1 мл мочи. Появление белого кольца на границе жидкостей указывает на наличие белка в исследуемой моче. Проба по Ларионовой так же чувствительна, как и проба Геллера.
5. Колориметрическая (сухая) проба качественного определения белка. Колориметрическая (сухая) проба качественного определения белка в моче основана на воздействии, которое оказывает белок на цвет индикатора в буферном растворе.
Техника определения белка. Кусочек индикаторной бумаги, предназначенный для определения белка погружают в мочу на короткое время. Пробу считают положительной, если бумажка окрашивается в сине-зеленый цвет.
Количественное определение белка в моче
Количественное определение белка в моче основано на том, что при наслаивании мочи, содержащей белок, на 50% раствор азотной кислоты или реактив Ларионовой на границе двух жидкостей образуется белое кольцо, причем если четкое белое кольцо появляется к 3 минутам, то содержание белка равно 0,033%о или 33 мг в 1000 мл мочи. Появление кольца ранее 3 минут свидетельствует о большем содержании белка в моче.
При количественном определении белка в моче выполняют следующие правила:
При наслаивании мочи в зависимости от количества белка может появиться компактное, широкое или нитевидное кольцо. Компактное, широкое кольцо появляется тотчас же после наслаивания мочи на реактив. Нитевидное кольцо может появиться сразу, до истечения одной минуты, или в промежутке от одной до 4 минут.
При появлении нитевидного кольца в пределах от одной до 4 минут производить разведение мочи не нужно!
Для вычисления количества белка в этом случае достачно использовать предложенную авторами таблицу-план (табл. 1).
Пример 1. При наслаивании мочи на реактив нитевидное кольцо образовалось через 2 минуты. Если бы кольцо образовалось к 3 минутам, то количество белка было было бы равно 0,033%о.
В данном же случае кольцо образовалось раньше. Соответственная поправка, согласно таблице-плану, для времени в 2 минуты равна 1+1/8. Это значит, что белка в данной порции мочи будет в 1+1/8 раза больше, чем 0,033°/оо, т. е. 0,033%о X(1+1/8) = 0,037°/оо.
При появлении нитевидного кольца до 1 минуты, т. е. через 40-60 секунд, производят одно разведение мочи в 1,5 раза (2 части мочи + 1 часть воды), а затем вновь наслаивают разведенную мочу на реактив и регистрируют появление кольца. При расчете результатов учитывают, что моча была разведена в 1,5 раза.
Пример 2. После наслаивания разведенной в 1,5 раза мочи нитевидное кольцо появилось к 2 минутам. Если бы кольцо появилось к 3 минутам, то белка было бы 0,033%. Соответственная поправка согласно таблице-плану, для времени в 2 минуты равна 1+1/8. Белка в моче содержится 0,033%оX1,5X(1+1/8) = 0,056%о.
Если нитевидное кольцо появляется сразу, мочу разводят в 2 раза (1 часть мочи + 1 часть воды). Разведенную мочу вновь наслаивают на реактив и отмечают появление кольца по истечении 1 минуты.
Пример 3. При наслаивании разведенной в 2 раза мочи на реактив нитевидное кольцо появилось через 1 минуту 15 секунд. Тогда количество белка в исследуемой моче по аналогии с прежними расчетами будет равно
0,033%оХ2Х(1+3/8) = 0,091%.
В случае появления широкого кольца мочу разводят в 4 раза (1 часть мочи + 3 части воды).
При последующем наслаивании разведенной мочи нитевидное кольцо может образоваться как до, так и по истечении одной минуты. В таких случаях расчет количества белка производят по аналогии с предыдущими примерами, т. е. 0,033% о умножают на степень разведения и на соответственную поправку.
Пример 1. Кольцо после разведения мочи в 4 раза появилось сразу же. Мочу разводят в 2 раза. После наслаивания мочи, разведенной в 8 раз (4X2), нитевидное кольцо образовалось через 1,5 минуты. В таком случае количество белка равно 0,033%оХ8X1,25 = 0,33%о и т. д.
При появлении компактного кольца мочу разводят в 8 раз (1 часть мочи+ 7 частей воды). При последующем наслаивании разведенной мочи на реактив может образоваться либо компактное, либо широкое, либо нитевидное кольцо.
Пример 2. При наслаивании мочи на азотную кислоту тотчас же образовалось компактное кольцо. Мочу разводят в 8 раз (1 часть мочи + 7 частей воды) и вновь производят ее наслаивание. При этом опять получилось компактное кольцо. Тогда мочу разводят еще в 8 раз (для этого в цилиндр или в пробирку берут 1 часть разведенной мочи и прибавляют к ней 7 частей воды). После очередного наслаивания разведенной мочи нитевидное кольцо образовалось сразу. Мочу разводят в 2 раза (1 часть мочи + 1 часть воды). После очередного наслаивания разведенной мочи нитевидное кольцо образовалось к 2 минутам. Расчет количества белка данной порции мочи производят так: 0,033,%оX8X8X2X(1+1/8) = 4,8%о.
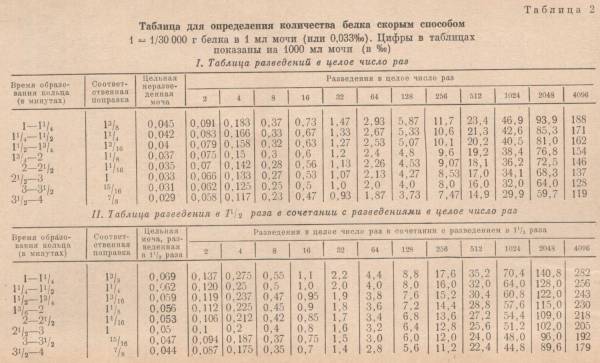
Помимо таблицы-плана, имеется таблица с рассчитанными цифрами белка (табл. 2). Если моча не разведена, то количество белка отыскивают в графе «Цельная неразведенная моча». При разведении мочи в целое число раз (8,4,2) используют табл. 1. При разведении мочи в 1,5 раза используют табл. 2.
Техника пользования таблицей для определения содержания белка в моче
В соответствующих графах таблицы наводят время появления кольца и степень разведения мочи.
Цифра, находящаяся в точке пересечения горизонтальной и вертикальной линий, проведенных от этих двух показателей, указывает на количество белка в исследуемой моче (%о).
Возможно, что при положительной качественной пробе на белок кольцо при наслаивании на 50% раствор азотной кислоты не образуется. Это значит, что в моче белка меньше 0,033%о. В таких случаях количество белка в бланке анализа обозначают термином «следы».
Если белок определен количественно, в бланке анализа мочи отмечают содержание белка в promille, например «белок — 0,66%о».
ПРОВЕДЕНИЕ АНАЛИЗА ПО ИССЛЕДОВАНИЮ МОЧИ У ЖИВОТНЫХ
ПРОВЕДЕНИЕ АНАЛИЗА ПО ИССЛЕДОВАНИЮ МОЧИ
1. Определение pH
Приготовление рабочего раствора индикатора бромтимолового синего.
Содержимое банки с бромтимоловым синем перенести в фарфоровую ступку и растереть его и добавить 40 мл 96% этилового спирта ректификата, подогретого до температуры 30 0 С, и тщательно перемешать до полного растворения. После охлаждения до комнатной температуры (18-250С) содержимое ступки перенести в мерный стакан или колбу, довести до дистиллированной водой до 200 мл и тщательно перемешать.
1.1. Ход исследования К 1—2 мл свежесобранной мочи добрить 1-5 капли рабочего раствора индикатора бромтимолового синего:
оранжево-желтый цвет соответствует кислой реакции, рН5,0;
• желтый цвет соответствует слабокислой реакции, рН 6,0-6,5;
• травянистый цвет соответствует нейтральной реакции, рН-7,0; буровато-зеленый цвет соответствует слабо щелочной реакции, рН- 8,0;
• сине-зеленый цвет соответствует щелочной реакции» рН-9,0.
Диапазон измерений рН находится в пределах 5,0-9,0
Примечание: мочу исследуют в первые 2—3 часа после мочеиспускания.
2. Определение содержания белка
2.1. Ход исследования
В две стеклянные химические пробирки внести по 1,0-2,0 мл профильтрованной или от центрифугированной мочи. В одну пробирку (опытную) внести 2-3 капли 0,85 моль/л раствора сульфосалициловой кислоты. Избыток сульфосалициловой кислоты приводит к растворению белка. Вторая пробирка является контрольной.
На темном фоне сравнить прозрачность обеих пробирок: помутнение в опытной пробирке указывает на наличие белка в исследуемой моче (положительная проба). Нижний предел обнаружение белка в моче составляет 0,033 г/л.
Примечание: Если реакция мочи щелочная, то перед исследованием ее следует подкислить 2-3 каплями раствора уксусной кислоты 5,2 моль/л (30%).
3. Количественное определение (метод БрандбергаРобертса-Стольникова в модификации с реактивом Ларионовой)
Приготовление реактива Ларионовой
Содержимое банки или пакета с хлористым натрием перенести в стеклянную колбу вместимостью 750 мл, добавить 500 мл дистиллированной воды и растворить при нагревании на водяной бане с температурой 50-70 0 С. Полученный раствор охладить до комнатной температуры и профильтровать; к 490 мл фильтрата добавить содержимое бутылки с азотной кислотой и тщательно перемешать.
Появление тонкого белого кольца на границе двух жидкостей между 2-й и 3-й минутами указывает на наличие белкам 0,033 г/л в исследуемой моче.
Если кольцо появляется раньше, мочу следует развести дистиллированной водой и провести повторное определение белка
Степень разведения мочи подбирается в зависимости от вида первичного кольца: ширины, компактности, времени его появления.
Количество белка вычислить, умножая 0,033 г/л на степень разведения.
Примечание: Иногда белое или желтое кольцо появляется при наличии в анализируемом образце большого количества уратов. В отличие от белкового кольца уратное кольцо появляется немного выше границы между двумя жидкостями и растворяется при легком нагревании.
4. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ
Приготовление реактива Гайнеса
Приготовление раствора меди (II) сернокислой 5-водной.
Содержимое банки с медью (II) сернокислой 5-водной перенести в стеклянную колбу вместимостью 750 мл, и добавить 400 мл дистиллированной воды и тщательно перемешать до полного растворения.
Приготовление раствора натрия гидроокиси
Содержимое банки с натрия гидроокисью перенести в стеклянную колбу вместимостью 750 мл, добавить 400мл дистиллированной воды и тщательно перемешать до полного растворения.
Приготовление раствора глицерина
Содержимое бутылки с глицерином перенести в стеклянную колбу вместимостью 250 мл, добавить 200 мл дистиллированной воды и тщательно перемешать.
Приготовление реактива
В стеклянную колбу вместимостью 1000 мл перенести растворы меди сернокислой и натрия гидроокиси, сразу же добавить раствор глицерина и тщательно перемешать.
4.1.Ход исследования
В химическую пробирку ввести 3—4 мл реактива Гайнеса, прибавить, 8-12 капель мочи, встряхнуть, прокипятить или поставить в водяную баню на 5 минут. В присутствии сахара появляется зеленая, желтая, оранжевая или коричневая окраска жидкости и осадок. Синий цвет указывает на отсутствие сахара.
При необходимости экономии реактива допускается постановка реакции в следующей модификации: 1 каплю мочи и 9 капель, реактива Гайнеса внести в химическую пробирку, довести до кипения или выдержать в кипящей бане 5 минут.
Примечание: моча больных диабетом должна исследоваться в первую очередь, т. к. ферменты бактерий и дрожжевых грибов частично или полностью разлагают глюкозу. То же самое наблюдается при бактериурии.
Нижний предел обнаружения глюкозы в моче составляет 5,55 ммоль/л.
5. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ БИЛИРУБИНА
Приготовление раствора бария хлористого 0,7 моль/л (15%)
75-г бария хлористого перенести в мерную колбу вместимостью 500 мл, добавить 250 мл дистиллированной воды, тщательно перемешать до полного растворения, довести дистиллированной водой до метки и вновь тщательно перемешать.
Приготовление реактива Фуше
1,35 моль/л (20%) раствор трихлоруксусной кислоты перенести в стеклянную колбу или стакан вместимостью 200 мл, добавить 0,39 моль/л (10%) раствор железа треххлористого и тщательно перемешать.
5.1. Ход исследования
В химическую пробирку внести 10 мл мочи и 5 мл раствора бария хлористого, тщательно перемешать и профильтровать. Хлористый барий осаждает билирубин
Вынутый из воронки фильтр поместить в чашку Петри и на него нанести каплю реактива Фуше. Появление на этом месте фильтра сине-зеленого, голубовато-зеленого или изумрудного пятна свидетельствует о присутствии билирубина в моче.
Примечание: Если реакция мочи щелочная, то необходимо подкислить ее несколькими каплями уксусной кислоты 5,2 моль/л (30%).
6. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ УРОБИЛИНОИДОВ (бензальдегидная проба Нейбауэра)
Приготовление реактива Эрлиха
Содержимое банки с n-диметиламинобензальдегидом перенести во флакон с соляной кислотой и тщательно перемешать до полного растворения.
6.1. Ход исследования В химическую пробирку внести 1-2 мл свежевыпущенной мочи, охлажденной до комнатной температуры, добавить 1—2 капли реактива Эрлиха из расчета 1 капля реактива Эрлиха на 1 мл мочи, тщательно перемешать и включить секундомер.
Окрашивание мочи в красный цвет в течение 30 сек. после добавления реактива Эрлиха свидетельствует о повышенном содержании уробилиногенов; если окрашивание развивается через 60 сек. или вообще не появляется, то концентрация уробилиногенов в моче в норме.
Примечание. 1. Если определение уробилиногена проводится в длительно стоявшей моче, то реакция может быть отрицательной из-за окисления уробилиногенов в уробилин.
2. Билирубин может мешать определению уробилиногенов, поэтому, если он обнаружен, его следует предварительно удалить, осадив раствором хлористого бария; в химическую пробирку внести 10 мл мочи, добавить 5 мл раствора хлористого бария, тщательно перемешать и профильтровать.
Нижний предел обнаружения уробилиноидов составляет 3 ммоль/л.
7. КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КЕТОНОВ
На фильтровальную бумагу насыпать небольшое количество (на кончике ножа) порошка Лестраде, нанести на него 2-3 капли анализируемой мочи и включить секундомер. При наличии кетонов через 2 мин. порошок окрашивается в розовый, сиреневый или темно-фиолетовый цвет в зависимости от содержания кетонов в моче.
Нижний предел обнаружения кетонов составляет 0,5 ммоль/л.